Производные оксадиазолилалкилпурина, проявляющие противокашлевую активность
Номер патента: 2467
Опубликовано: 15.09.1995
Авторы: Деже Корбонитш, Вера Гергели, Шандор Вираг, Петер Кермеци, Золтан Варгаи, Гергели Хейа, Андреа Болеховски, Агнеш Готтшеген, Габор Ковач, Габор Хорват, Ласло Тардош, Каталин Мармароши, Йене Мартон, Эмиль Минкер, Лоранд Дебрецени, Шандор Антуш
Формула / Реферат
Изобретение касается гетероциклических веществ, в частности производных оксадиазолилалкилпурина общей ф-лы:
проявляющих противокашлевую активность, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез, например, 3,7-дигидро-З-метил-7- [( 5-хлорметил- -1,2,4-оксадиазол-3-ил)метил]-1Н-пурин-2,6-диона ведут ацилированием 2-[3-метилксантин-7-ил] ацетамидооксима хлорацетилхлоридом в присутствии Na2CO3 в среде безводного ацетона. Новые соединения при токсичности ЛД50 - 250-700 мг/кг имеют более высокую противокашлевую активность при меньшей дозе, чем известные соединения, и они не оказывают блокирующего дыхание действия и значительно улучшают дыхание.
Текст
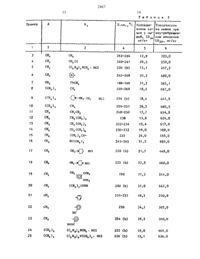
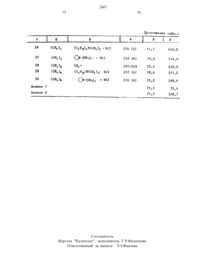
Изобретение относится к новн про изводным оксадназолнлалкнлпурнна формулы 1ПРОЯЕЛЯЮЩВ ПРОТНБОКЭЩЛЕВУЮ ЗКТНБНОСТЬ и которые могут найти применение в ме дицине при заболевании органов дынат НИЛЦель изобретения изыскание в рят ду пронзводнык оксадназолнлапкнлпурнт на новых соединений, проявляющих бо лее ВЫСОКУЮ ПРОТНВОКЗШПЕВУЮ ЗКТНБНОСТЬа. 350 г (О,25 ноль) 3 метнпксан тина растворяют в 81,4 мл (025 Моль) 102 ного раствора гидроокиси натрия,кристаллизация происходит в течение нескольких минут. Воду отгоняют приляют азеотропной перегонкой с толуо лом. Остаток суспенднруют В 350 Млднметилформамнда, после чего при 100 Спри перенешваннн добавляют по каплямраствор 19,0 г (025 моль) хлорацето ннтрнла н 80 мл днметнпфорнамнда. Реи акцнонную смесь перемешивают еще 1 ч ПРИ 10000, фильтруют в горячем состоят ним, осадок (хлористый натрий) промьг ваюг горячим дннетилформанидом И сое диненные растворы сгущают досуха при пониженном давлении. Остаток растирают с 100 мл ацетона, кристаллы фильтруют и основательно промывают ацето номъ Полученньт таким путем 7-цвано метнл 3 тнетнлксантин можно непосредственно перерабатывать дальше, тпл. 285-2 в 7 с.Ь. К раствору 3,2 г гндроксиланин гидрохлорида и 36 мл воды добавляют частями 2,5 г карбоната натрия. К поч лученному таким путем раствору попав ляют 10,0 г 7 тпианометнл 3 метнлксан тина и 30 мл этанола. Реакционную смесь перемешивают 3 ч при 80 С и зат тем охлаждают. Осажленньт 2(3-метнл ксантнн 7 тнл)нацетамндоксндоксим фильтруют и промвают небольшим колит честном холодной воды. Вьтод 11,0 гс. Смесь, образованную из 6,76 г натрия Н 290 мл безводного этанола,раствора этнлата натрия, 35,0 г 2(3 тметнлксантнн 7 ил)ацетанндокснма н 43,0 мл этилацетата нагревают до кнпенни при перемешивании в течение 4 ч. Реакционную смесь фильтруют в горячем состоянии н фильтрат сщугают при понженном давлении. Остаток растворяют в 200 мл воды. рН раствора устанавлн вают до 7 при помощ 10 ной соляной кислоты. Осажденный продукт фильтруют и дважды крнсталлнзуют из воды. Получают 18,0 г 3,7 днгнлроЗметнл 7 К 5 нетнл 1,2,4 токсаднаэолЗнл)метнл 1 Нпурнн 2,6 днона, т.пл. 26226 дС.(19,6 нмоль) 3 хлорнетил-5 метнлт 1,2,доксадназола переменвают при 100 С 1,5 ч. Реакционную смесь фильтруют в горячем состояни н к фильтта. Раствор 2,38 г 2(3-метилксантин-7-ил)ацетамидокснна и 45,0 ил уксусного ангидрида перемешивают при 140 С в течение 10 мин. Охлажденньт раствор разбавляют водой до 10-крат ного объема и перемешивают в течение 30 мин. Осажденныи 0-ацетнл-2-(З-не ТНПКСаНТНН 71-П 3 ацгтдмндйксим филь ТВУЮТ Н Проиывают небольшим количеством метанола. Получают 3,60 г продукта с т.пл. выше 220 С (разл)Ь. 2,0 г 0-ацетил-2-(3 метнлксан тин-7-ил)-ацетамидоксима перемешивают в смеси 160 мл буферного раствора Бриттоиа-Робинсона (рн 7) и 200 мл дик нетилформамипа при 95 С в течение 6 ч. Реакционную смесь сгущают при пониженном давлении. После кристаллизации остатка из воды получают 1,22 г 3,7 дНГНдрО-З-ме тил-7- (5 тметил-1 ,2,гь-оксадиазол-3-ил)-метил -1 Нпурнн-2,6 тлиона, т.пл. 262-26 дС, Н р и м е р 4. Раствор 2,38 г 2-(3-метилксантин 7-ил)-ацетамидоксима в 40 мл безводного ацетона ацилируютв присутствии 0,86 г бикарбоната натрия при помоиш раствора 1,13 г хлорацетилхлорила и 5,0 мл ацетона. Получают 2,1 г 0-хлорацетнл-2-(3 метилксантии-7-ил)-ацетамидоксима. Продукт сушат до постоянной массы при 105 С Н при давлении 133 Па в течение 40 Нин. Остаток Крнсталлнзуют из метанола. Получают 1,6 г 3,7 пигидро-3П р и м е р 5. а. Смесь 1,5 г 3-Внетнлксантин 7 ил)метил-5-хлорметил-1,2,д-оксаднавола, 10 ил днэтнл амина и 10 ил толуола нагревают на водяной бане в течение 8 ч при перемешивании в снабженной магнитной мешалкой закрытой колбе. Реакционную смесь сгущают, остаток промвают во дой, растворяют в 5 мл горячего эта нола и осветляют при поыощ активного угля. Гидрохлорид образуют при помощи этанолового хлористого водорода н кристаллнзуют из воды. Получают 1,4 гЬ. 1,41 г 0-хлорацетил-2(3 метилнсантин-7-ил)-ацетамндоксима смешивают по каппян с 15 нл толуола, при сильном перемешивании с 1,5 ил диэтиламнна. Реакционную смесь нагревают до кипения в течение 8 ч и после этого сгущают. Остаток промывают водой. Гидрокпорнл образуют в этаноле и кристаллизуют из воды. Получают 1,2 г 3,7-дигидро-3-метил--К 5-днэтиламинонетил-1,2 Аоксадиаэол-З-ил)-метил-1 Н-пурин-2,6-дионгидрохлоридас. 2,38 г 2-(З-нетилксантнн-7-ил)ацетанидоксниа в 20 мл пиридина пе ренешивают с 3,0 г диэтнламиноацетнпхлорида при температуре, не превогшающей 20 С. Реакционную смесь нагревают на водяной бане 2 ч Н сгущают. Остаток промывают водой. Гилрохлорид образуют с этаноловьщ клористьм водородом и кристаллизуют из воды. Получают 2 1 г 3-(3-иетилксантин-7-ил) метил-5-дивтиламинонетил-124-оксадиаэолгидрохлорида.а. Смесь 2,38 г 2-(3-метилксантин-7-ил)-ацетвмндокснма, 200 мл толуола, 1,36 г зтилата натрия и 3,46 г простого этилового эфира Е -диэтнламинопропноновой кислоты агревают до кипения П течение 12 ч при перемешиоаннн в снабженной водоотделителем колбе. Реакционную смесь сгущают при пониженном давлении, устанавливают рН до 7, осадок промывают водой и сушат. Гидрохлорид образуют в этаноле. Получают 2,0 г 3,7-дигидро-З-метнл-7-(5-дизтиланинометил-1,24-оксапназол-3-ил)-метил-1 Н-пурин-2,6-лионгидрохлорида.П р и м е р 6. 2,38 г 2-(3-метилксантнн-7-ил)-ацетамидоксина в 25 мл этанола нагревают до кипения н течение 20 ч при перемешивании с раствором 0,5 г натрия в 25 ил этанола и с 3,12 г сложного этилового эфира Цнклогексанкарбоповой кислоты. Реакционную смесь сгущают, остаток смешивают с водой и устанавливают рН до 7. Остаток кристаллизуют из водного этанола. Получают 2,51 г 3,7-днгндро-3-метил-7-5-цнклогексил-1,2,4-оксатиазол-3-ил)-метил -1 Н-пут рин-2,6 диона с т.пп. 265-2 д 8 С.ного этилового эфира фенилуксусной кислоты и зтилета натрия в этаноле,получают 2,7 г 3,7-днгидрое-З-ыети.ттт 7 т (5-бензин 2,4 оксаднаеол 3 тнл)тме тнл 1 НПУРнн 26 днона.П р и и е р 8. 2,52 г анндокснма 3(3 метнлксантнн 7-ил)тпропноновой кислоты в 4,0 мл этилацетата нагревают до кипения в течение 5 ч с раствот ром 0,46 г натрия н 25 мл этанола. Реакцонную смесь фильтруют в горячем состоянии, фильтрат выпаривают, оста ток обрабатывают 20 мл воды и уста навливают рн до 7. Осадок кристаллизуют ив воды. Получают 1,7 г 37 тднгнд р 03 метНл 72(5 нетнл,2 д-оксат диавол 3-)тилтэтан-1 нл-1 НтпуринП Р Н Н е р 9. Смесь 2,52 г амндоксима 3(3 тнетнлксантин 7 тил)тпрот пмоновои кислоты, 25 мл толуола, 1,12 г распыленнои гидроокиси калия И 3.70 г сложного этилового эфираБтпнперидннопропионовой кислоты нагревают до кипения в течение ТО ч приперемешивании в снабженной водоотделштелем колбе. Реакционную смесь сгущают. Остаток обрабатывают водой,устанавливают рН до 7, осажденный осадок промывают водой, образуют гид рохлорид в этаноле Получают 2,6 г 3,Ттдигндро-3-метнлт 7-т 5 т(2 пнпе рндиноэтан 1 ил 124 токсадиаэол 3 илтэтант 1 нл 1 Н-пУрин 2,6 днонтгндрохлорида.П р и м е р 10. Раствор 2,66 г анидоксима д(3 метилксаитин 7 нл) масляной кислоты в 4,0 мл этилацетат та нагревают до кипения в течение 6 ч с раствором 0,6 г натрня и 25 ил этанола. Реакционную смесь обрабатыт воют описанным в примере 3 способом. Получают 1,8 г 3,7 днгндро 3 метил 73-(5 метил 1,2,6 оксадиазоп-3 тнл 7 пропан-1 ил 1 Нпурин-26 тдн 0 Нг П р и м е р ы 11 тЗ 1. сведены в табл 1 н получены аналогично описант им примерам.Определяют успокаивающее кашель действие, оказанное не вызванный впры скиваиием 152-ной лноиной кислоты морским свинкам кашель, через 1 ч после перорального назначения тест соединения, и полученные величины 1 В 5 (мгкг) указаны в табл. 2.Из данных табл. 2 видН 0. ЧТО ПРИ оральном назначении тесттсоедннгннг 1 по абсолютной интенсивности успокаи вающего кашель действия значительно превосходит примененные в качестве эталонного соединения тесттсоедннення 2-4 и 6. Производное ксаптнннламидок сима соединение 5 практически не имеет никаких успокаивающих кашель свойств.Успокаивающее кашель действие, оказанное на выэваины впрыскиванием 152 тной лионной кислоты морским овине как кашель, при пероральном назначенин 3,7 тднгндро 3 тнетил 7 нК 5 тнетнл т 124 оксаднаэол 3 нл)метил 1 Н-пурИН 26 тднона (1) следующееНЗМЭВЕННЗЯ на крысах острая ТОКСНЧ ность (внутрмбрюшннное назначение) тестчсоеднненнй следующаяТесттсоедннение Токсичность на крысах ЪВ мг/кг 1 700,0 Аналог 1 529,7 Аналог 2 72,4Соединение 1 (3,7 тдигидро-Этнетнлт 7(5 тметилт 124 оксадиаэол 3 чШЭ-МетнлТ-тн-пурии-бе-дион обладает не только при оральном применении,но н при внутривенозном очень сильной активностью, подавляющей кашель. Оно уменьшает в зависимости от дозы (0,5 8,0 мгкг 1.ч) кашель, вызываемът механическим стимулированием Тгаслеа В 1 Ецгеас 1 о у наркотнэированных нембу талон кроликов.Через 2 мин после внутривенного введения Еддд составляет 2,2 (1,В 5 2,72) мг/кг.Терапевтический индекс соединения 1 в этом опыте в десять раз благопри ятнее терапевтического индекса контрольных соединений.Успокаивающее кашель действие соединении формулы 1 определяют на морских свинках при пероральном на значении. Скрипинговые испытания проводят внутримышечно на мыах. Кашель вызъшают ингаляцией спрея с оодерпа ннем 152 ной лионной кислоты. Бепн чину 105 (ингибнторнал доза 503 от ределяют по дозе, которая может продлить период времени до первого приступа кашля в три раза на 502 тести 2467руеных животным. Каждую дозу испытывают на 10 животным. Основной период времени намеряют 24 ч перед экспериНентан осадиазола. Токсичность определяют также на ныах при внутрнбрюшшннон введении. к Результаты испытаний даны втабл. 3 Таким образом, производные 0 ксадн азолилалкилпурнна проявляют более высокую протнвокашлевую активность в меньшей дозе, чем известные н обладают при этом более низкой токсичностью. Соединения не оказывают никаком го блокирующего дыхания действия, ана общей формулы .
МПК / Метки
МПК: C07D 473/06
Метки: противокашлевую, активность, производные, проявляющие, оксадиазолилалкилпурина
Код ссылки
<a href="https://kz.patents.su/8-2467-proizvodnye-oksadiazolilalkilpurina-proyavlyayushhie-protivokashlevuyu-aktivnost.html" rel="bookmark" title="База патентов Казахстана">Производные оксадиазолилалкилпурина, проявляющие противокашлевую активность</a>