Способ получения пенемкарбонового эфира
Номер патента: 1571
Опубликовано: 15.12.1994
Авторы: Аврора Санфилиппо, Маурицио Фоглио, Джованни Франчески
Формула / Реферат
СПОСОБ ПОЛУЧЕНИЯ ПЕНЕМКАРБОНОВОГО ЭФИРА общей формулы
где R-ацетоксиметильная, пивалоилоксиметильная, метоксиметильная, метоксиэтоксиметильная, фталкдильная, альфаэтоксикарбонилоксиэтильная, ацетамидометильная или бензамилометильная группа, отличающийся тем, что соль соединения общей формулы
подвергают этерификации соединением общей формулы R - X, где R имеет указанные значения; Х - галоген, в присутствии диметиламинопиридина в диметилформамиде при температуре от комнатной до 40°С.
Текст
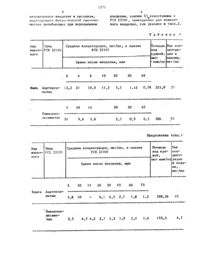
НАЦИОНАЛЬНОЕ ПАТЕНТНОЕ ВЕДОМСТВО ПРИ КАБИНЕТЕ МИНИСТРОВ РЕСПУБЛИКИ КАЗАХСТАН(19 Фармнтална Карло Зрба С.рдЪ.(72) Маурнцио Фоглио Джованни Фран чески (1 Т) н Аврора Санфнлиппо (АТ)(5 А)(57) сносов пплшчвння ПЕНЕМКАР БОНОВОГО ЭФИРА общей формулы-ная или бенэамилометипъ пая группа,соль соеднення общей формулыподвергают этерификации соедннейием общей формулы н-хгдеЕинеетУкаэаннне значния Х - галоген, в присутствии дннетнланимопнридинв в дицетнлфорнамиде при температуре от комнатной др д 0 С.1 1 Изобретение относится к получе ПМРООРНЬ СВс 13 5 РРШ 1-21 нпю новых соединений, а нъченно пе- (5, ЭН, 4191133333 1,33 (1 АЩЗЙ,немкарбонового эфира общей формулы ЗН, снащд 3,75 (да, 1 1,5 6,4 НЕ. - (1 н н 6) 4,23 (ш, хн, снов) дайгьвзЫН 1)З,ВВБ,ЗСЦБЗ 5 ка 1 15,8 Нг, щьосоыълд 5,62 д 135 Н 2 эцр 753 58 ы 5 9 (два а 15 энд ощьосощсн О 000 П р и м с рАцтокшетип-з)тщтьная, фталидильная, 5 альфаэтоксшсарбоннлоксич этнльная, ацетамидометильт Юсоына ная или бензамнпометильная О ы С группа, он - ОШЦелью изобретения является раэ- О Ы работка на основе известного метода - СООСЪЩОСОСНЗ способа получения новыж соединений, 1,3 г (5 в, 6)-2 ар 5 амонлоксиОБЛНДЗЮЩРШ ЦВНПЬМН ФНРМЕКОЛОГНЧеСЧ метилтб- П (К) -окоиэтш 1 -2 пенемкаши свойствами. Зтарбокснлата натрия растворилиП 13 И М Е 13 1- ПРЕВЫШЕ-КЛОКОВ в 30.н.п безводного диметилформамида метнл-(ЭК, б 5)-2 карбамонлоксэшетнпт и обработали раствор 0,65 г ацет-б 1(Н)-оксиэтнп-2 тенн-З-карбок- оксшетнлбромида при комнатной темсилат. К -СН,О-СОС(СН,), пера-туре в течение 3 ч.Затем реакционную смесь разбави ОН . . ли этилацетатом, промыли водой, вы 5 сушили над сульфатом натрия и выгодный парили. Полученное сырое соединениеО Ы . кристадшнзовапн из смеси хлороформаСобью, с щпслогексаном, а затем из горя чего хлороформа температура плавления продукта. 27 С (на шторофорна) 5775 мг (ЗК, ББЪ-Ъчсарбамоипоксн чсарбокснлата Натрия растворили в 15 мл диметилформаммда и обработалипри 4000 В течение д ч. Затем реак- 6,4 На, 1 Н, Н-Б) 4,14 (кпд-ПЕ цнонную смесь разбарнли отипацетатом, 01-1593) 5,08, 5.35 (два а, 1 в промыли водой, высушили-над сУльФгЕд 16,0 Н 2, 28, ЩОСОННД 5,69 том натрия и Быт-жарили растворитель. (а, 1 1,7 На, Ш, Н-Б) 580,5,86 Остаток включал 480 мг чистого целе- (два (1, 1 5,8 112,211, 0006332000) вого соединения. 6,10 (ЬЗ, 2 Н, 15111)г чсъиосн, В ходе проведения эксперимента аналогично примеру 2, но с нспопьзованнсм метоксиметнлбронида вместо ацетоксиметипбромида с достижениеы 652 ного выхода получили целевое соединение.В коде проведения эксперимента аналогично примеру Т, но с использованием метоксиэтокснметнлхлорнда вместо пивалоилокснметилклорида с достижением 58-ного вьжода получили целевое соединение.В ходе проведения эксперимента согласнопримеру 2, но с использованием 3-бромфталнда вместо ацетокснметилбромида с достижением 62-ного вывода получили целевоесоединение.В ходе проведения эксперимента согласно примеру 1, но с использованием клордиэтнлварбоната вместо пивалонлоксиетилклорнда с достигнием дО 2 ного вывода получили целевое соединение.В коде проведения эксперимента аналогично примеру 1, но с нсполъзованнем ацетамидометилклорида вместо пналонлоксиетилхлорида с достиеннем д 5 Х-ного вывода получи-ли целевое соединение.-(ЭК,65)2 карбамоилоксиметил 6 1(33-Оксиэтил-2-пенем 3-карбоксилат. К СН 1- МН - С 0 СдН 5 В ходе проведения экспериента согласно примеру 7, но с использованием бензамндонетнлнлорнда вместо ацетамидонетнлклорнда с достижением 432 ного вывода получили целевое соединение. д .Полученныесоедннения являются активнодействующии агентами против грам-положительныв, грамтотрнцателъч ныш, беталактампродуцнрующнх и анаэробных бактерий, что обуславливает ив полезность в качестве терапевтических и профилактических средств в борьбе с бактериальными заражепнями.В табл.1 приедены уровни плазмы и площадь участка под кривой, построенной длн случая, когда мыам и крысам через рот вводили ацетокснметиловый и пнвалонлокснэтиловый эфиры (5 К 65)2-карбамоилоксметнл 6- 1 (К)-окснзтил 2-пенем-3 карбоновой кислоты в дальнейшем обознаиены как гсв 22101) .для получения результатов, показаннышв табл.1 два эфира ГСЕ 22101 пероральнодевали в растворе кышам н крысам в количестве, эквивалентном тону, которое необходимо для получения до мг РСЕ 22101 на килограмм жнвого веса после ондаемого гидролиза п ч 1 чо.У жнвотны периодически орали пробы крови, которые анализировали на содержание ЕСЕ 22101 по стандартной экспериментальной технике.-данные табп.1 показывают, что сложные эфиры ЕСЕ 22101 усваиваются при приеме через рот, а затеи гидролизуются в крови с образованием актинодействующего лекарственного агента. Этот эффект является особенно ценным, поскольку пенемарбонован кислота н ее натриевая солв не усваиваются в желудочно-кнечном тракте.Терапевтическая эффективность деаствня на мышей, испытанная после5 6 НЕРОВЦГКЪНОГО ВВЕДЕНИЯ В организм, ВВЕДЕНИИ, ПРИЧ-ЕМ ЕВ 5 ОСОПОСТЗВШЧЫ С подтверждена биологической приемле- ГСЕ 22101, прнведенньы для подкожмостью антибиотика при пероральном - нога введения, как указано в табл.2 Т а б л и ц а 1 Вид Эфир 1 Средняя концентрация, мкг/мл, в плазме ощадь Пик конживот РСЕ 22101 СЕ 2210 под 2 центраного крНВОЙч.ЦНН в Время после введения, мин ним/мл мкг/мл. 2 п.нь.-.ь-ь.-.о.-.- .2 4 6 10 20 30 55 Ныъ Ацетокси- 13,5 21 19,5 11,2 3,5 1.12 0,78 253,8 21 метил 5 10 15 20 - 30 45 ПНЗВ НЛОНЛ 31 9,4 3,6 2 з 0,9 0,5 286 рл Продолжение табл.вид Эфир Средняя концентрация, мкг/мл, в плаэм Площадь Пи живот РСЕ 22101 ГСЕ 22101 под крн конного йа ЦеТ здпсг-мин/мл рации Время после введения, иди В ПЛЗ 3 не, мкг/мл 5 по 15 20 за 45 во 75 Крыса АцетоКси --- Т 5,3 по - д,1 6,5 2,7 1,3 1,2 288,36 10 Пиалоип пкснне тид 3,5 4,7 4,2 2, 2,5 1,9 2,1 1,4 155,5 д 7
МПК / Метки
МПК: C07D 499/00
Метки: пенемкарбонового, получения, способ, эфира
Код ссылки
<a href="https://kz.patents.su/5-1571-sposob-polucheniya-penemkarbonovogo-efira.html" rel="bookmark" title="База патентов Казахстана">Способ получения пенемкарбонового эфира</a>
Предыдущий патент: Способ получения макролидных соединений
Случайный патент: Способ купирования гипертензивных кризов, сопровождающихся тахикардией, на догоспитальном этапе