Способ получения производных 2-анилинопиримидина
Формула / Реферат
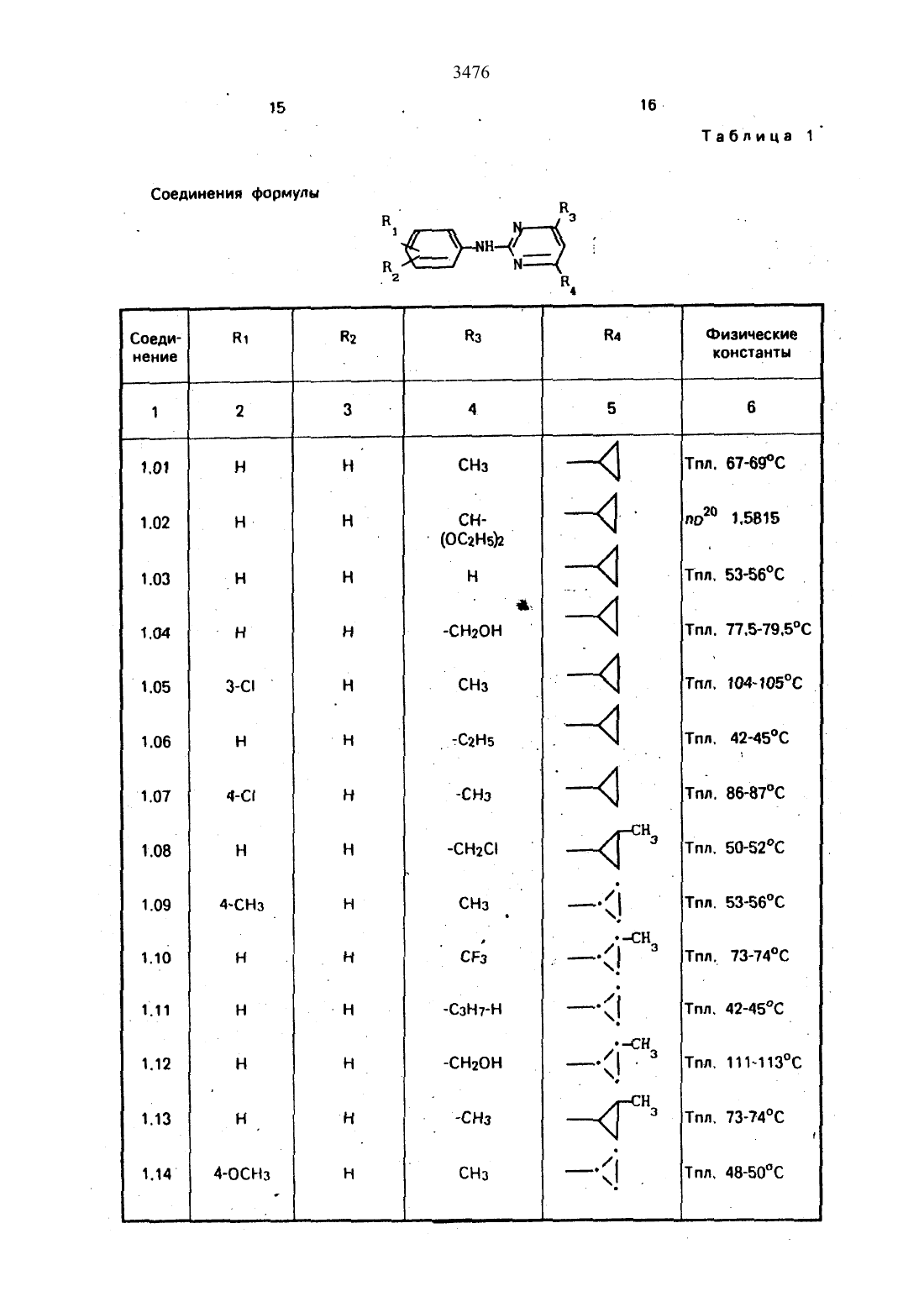
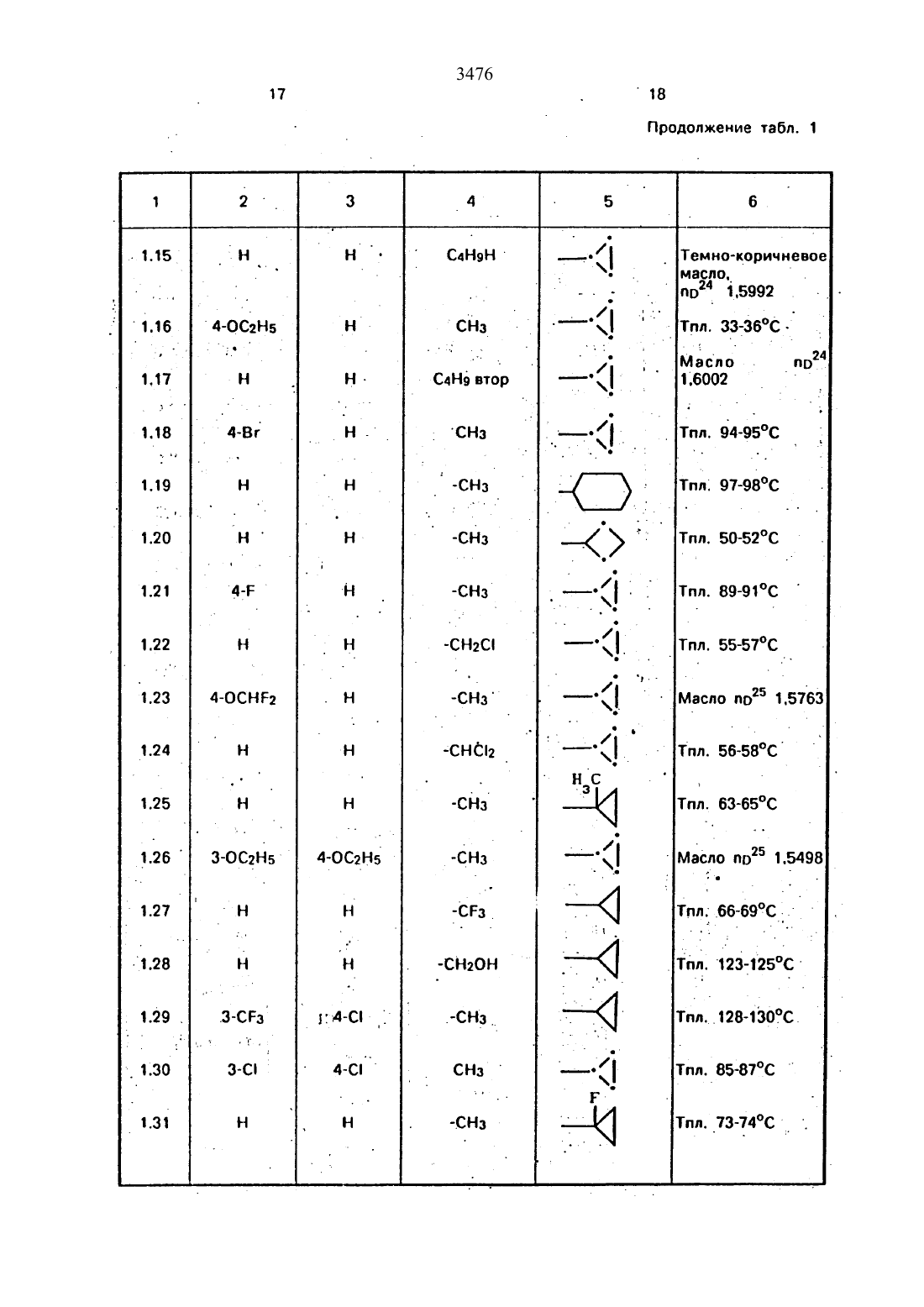
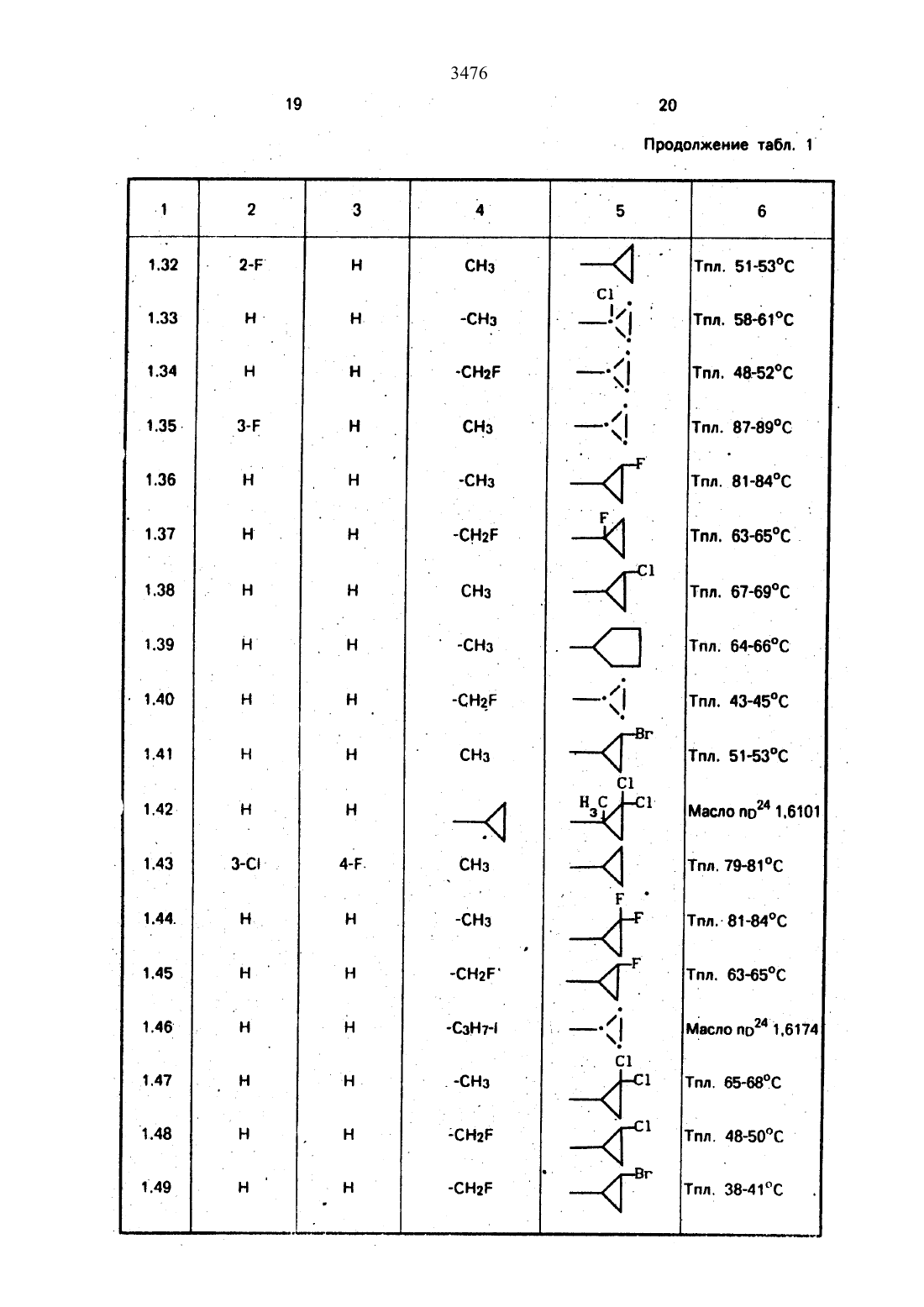
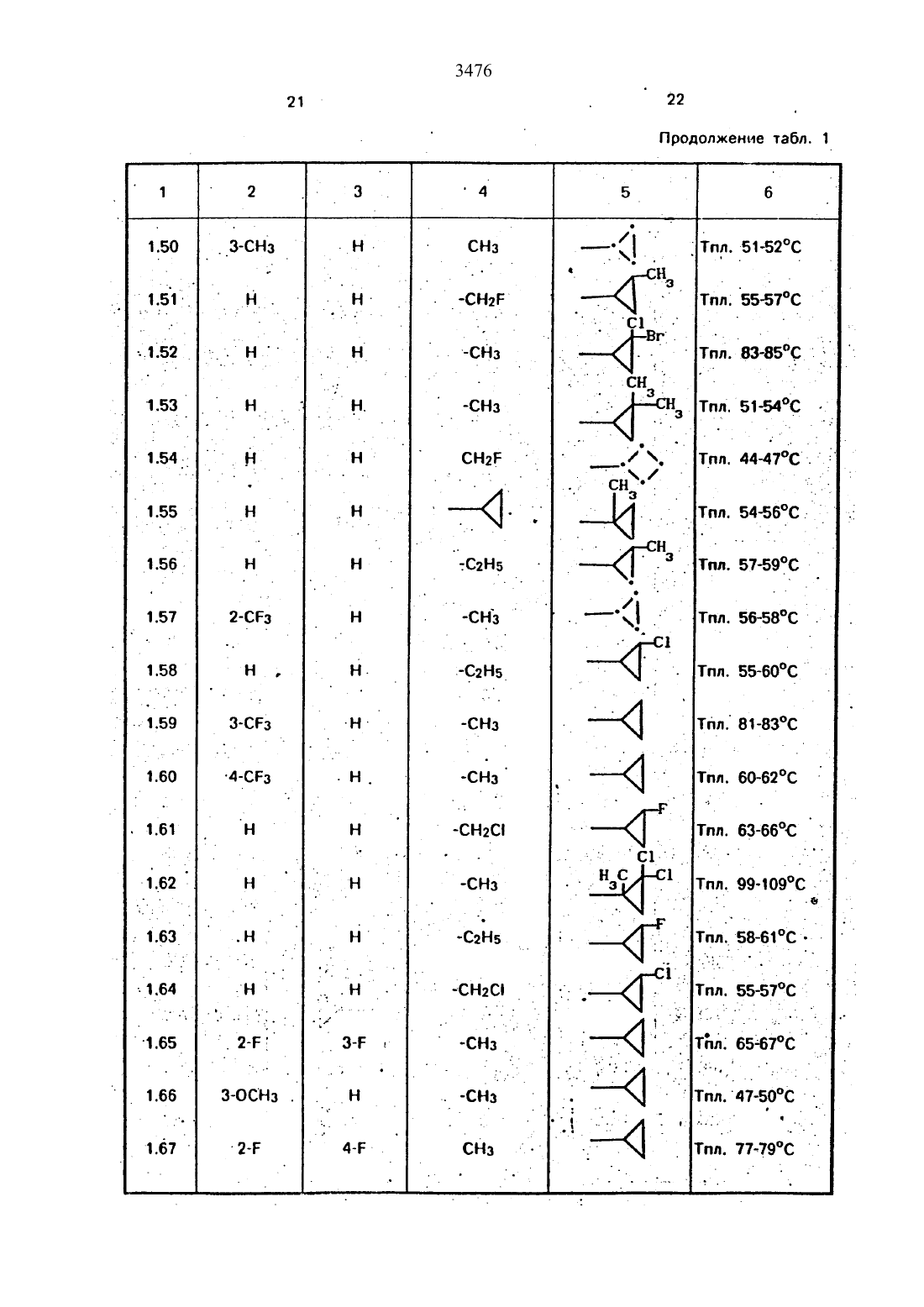
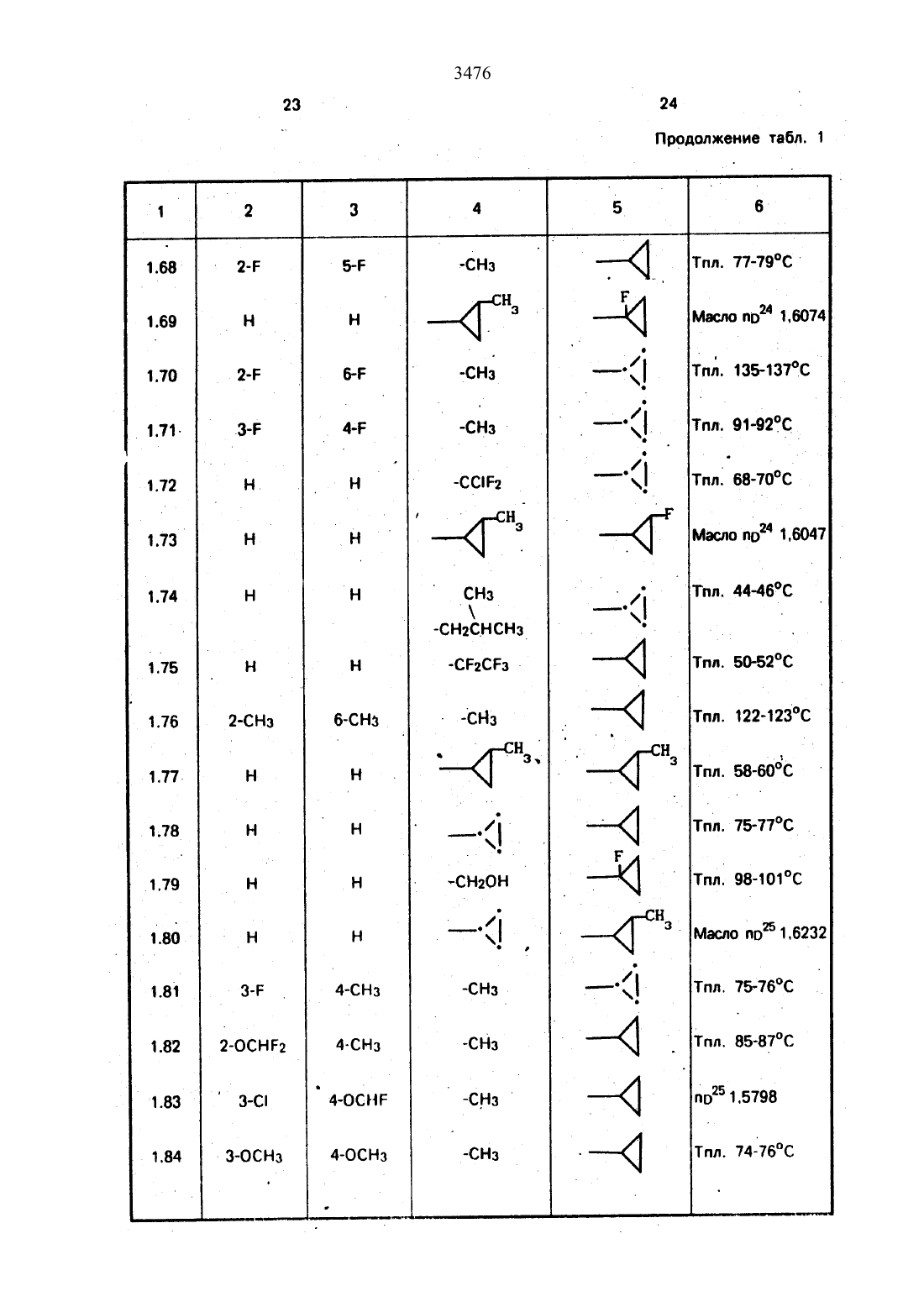
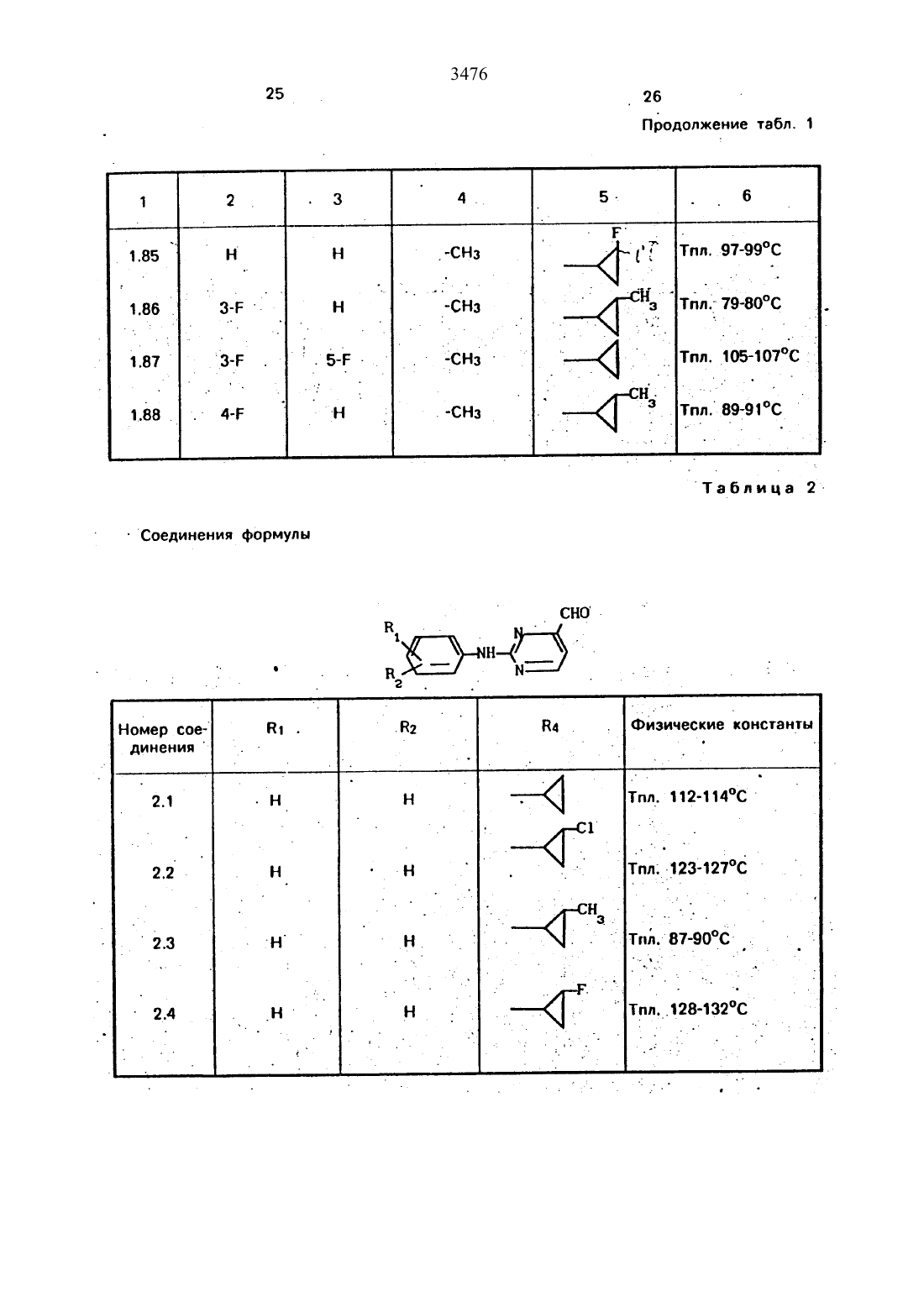
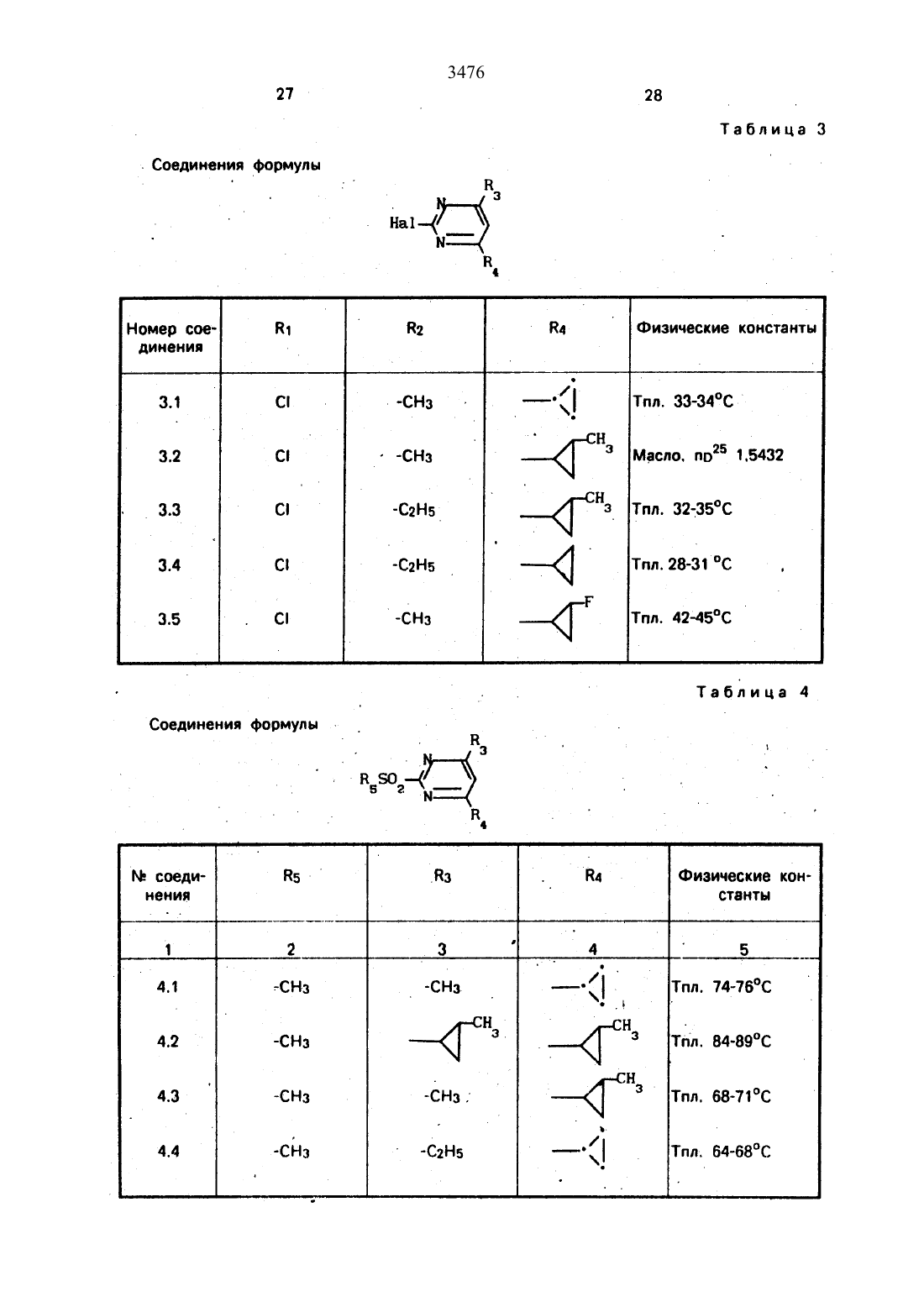
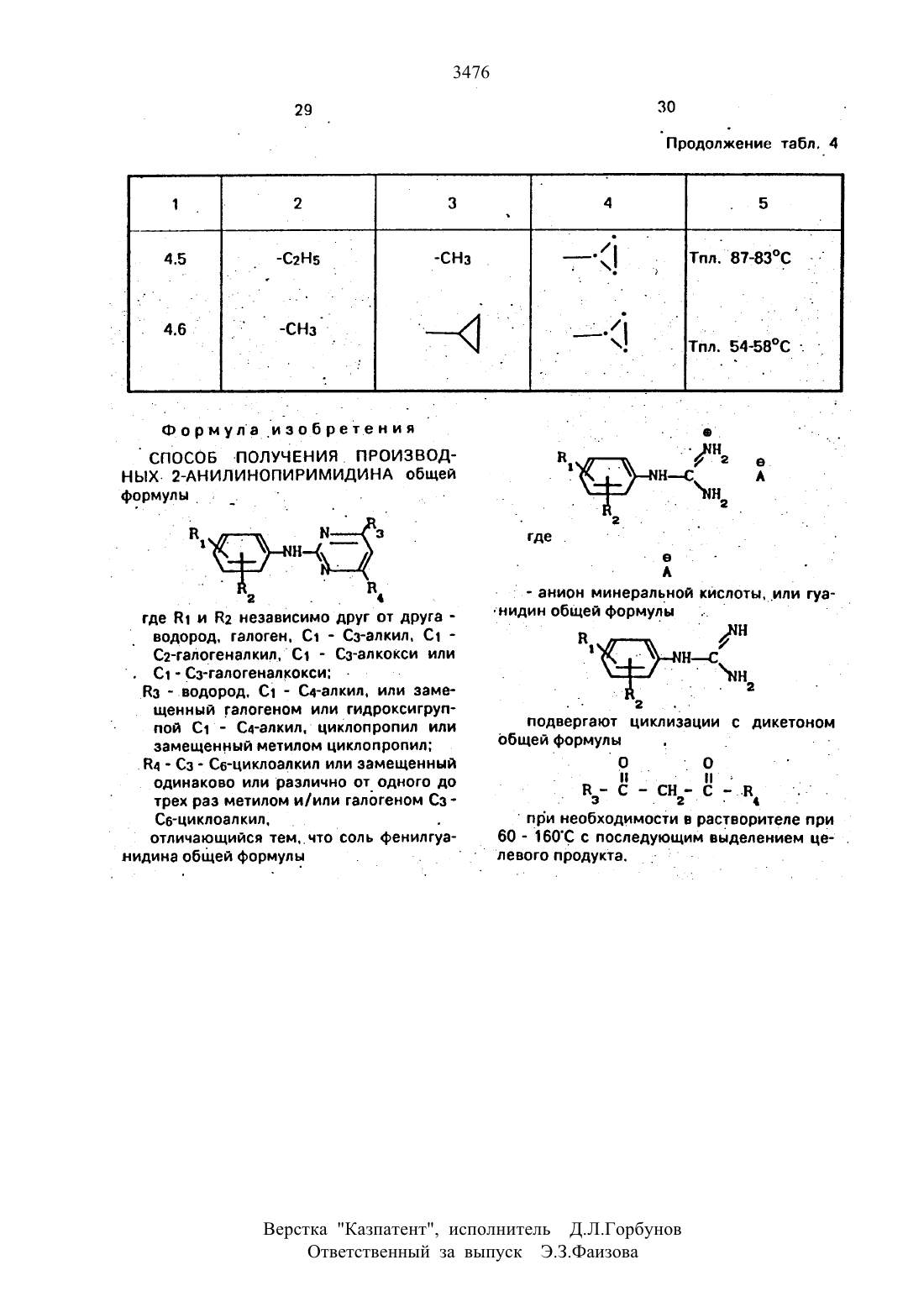
Использование в сельском хозяйстве как обладающие фунгицидной и инсектицидной активностью. Сущность изобретения - способ получения производных 2 - анилинопиримидина общей формулы
водород, галоген С1-С3 -алкил, С1-С2 -галогеналкил, С1-С3 -алкокси или С1-С3 -галогеналкокси, R3 -водород, С1-С4 -алкил, или замещенный гидрокси группой С1-С4 -алкил, циелопропил или замещенный метилом циклопропил; R4-С3-С6 -циклопропил или замещенный одинаково или различно метилом и/или галогеном, вплоть до трехкратного, (С3-С6) -циклоалкил. Реагент 1: соль фенилгуанидина формулы
где А - анион минеральной кислоты или гуанидин формулы
Реагент 2: дикетон: R3C(O)CH2C(O)R4; циклизацию ведут при температуре 60-160°С.
Текст
Изобретение относится к способу получения производных 2-анилинопиримидина новых биологически активных соединений, которые могут найти применение в сельском хозяйстве как обладающие фунгицидной и инсектицидной активноСТЬЮ.Известны М-пиримидиниланилиновые соединения. эффективные против поражающих растения грибов.Однако эти соединения обладают недостаточно высокой фунгицидной активностью, инсектицидная активность у них отсутствует.Цель изобретения способ получения НОВЫХ ПРОИЗВОДНЫХ 28 НИЛИН 0 ПИрИМИдИН 8 малотоксичных. обладающих высокой фунгицидной активностью и проявляющих, кроме того инсектицидное действие.Поставленная цель достигается описываемым способом получения производных З-анилинопиримидина общей формулы.где 81 и 82 независимо друг от друга озна чают водород. галоген. Сг-Сз-алкил. С 1 С 2 галогеналкил, Сг-Сз-алкокси или Сг-Сз-галогеналкоксиКг, водород. Ст-Сл-алкил или замещенный галогеном или гидроксигруппой СгСаалкил. циклопропил или замощенный метилом циклопропилНа СзтСв-циклопропил или замещенный одинаково или различно метилом и/или галогеном. вплоть до трехкратного, Сз- Свциклоалкил. заключающийся в том, что соль фенилгуанидина формулы2 в которой А означает анион минеральной кислоты или гуанидин формулыпри температуре 6 О 16 ОС с последующим выделением целевого продукта. Примеры получения.10 г (51 ммоль) кислого карбоната фенилгуанидина и 9,7 г (77 ммоль) 1-цикпопропил- 1 .3-бутандиона нагревают при перемешивании 6 ч до 110 С. при этом начинающееся выделение двуокиси углерода увеличивается с продолжением реакции. После охлаждения до комнатной температуры темно-коричневую эмульсию смешивают с 50 мл диэтилового эфира. дважды промывают водой порциями по 20 мл. высушивают над сульфатом натрия, фильтруют и испаря ют растворитель. Оставшееся темно-корич невое масло (1 О.1 г) очищают колончатой хроматографией через силикагель (диэтиловый эфир/толуол 53). После испарения элюирующей смеси коричневое масло кристаллизуют и перекристаллизовывают из смеси диэтиловый эфир/петролейный эфир при 3050 С. Получают светло-коричневые кристаллы Т.пл. Б 7-69 С. Выход 855 г (38 ммоль) 04,5 от теории). т11.7 г (592 ммоль) кислого карбоната Фенилгуанидина и 13.3 г (622 ммоль) 1-цик лопропил-З-формилдиэтилацетал ь-1 ,3-про пандиона в 40 мл этанола нагревают при перемешивании до температуры кипения флегмы, при этом выделение двуокиси углерода увеличивается с продолжительностью реакции. После охлаждения до комнатной температуры темно-коричневую эмульсиюдважды промывают водой порциями по 30 мл. высушивают над сульфатом натрия. фильтруют и растворитель испаря ют. Оставшееся темно-коричневое масло (17 г) очищают с помощью-колончатой хроматографии над силикагелем (толуол/этилацетат 52). После испарения элюирующей смеси оста СТСЯ КОЭСНОВЗТОЧСООИЧНВВОЭ МЗСПО С ПОКЭ7 зателем преломления по 20 158.15. Выход 1512.32 г (393 ммоль 2-анилино-4-формил сдизтилацеталь-б-циклопропиппиримидина,. 4 г(39.3 ммоль) концентрированной соляной кислоты и 75 мл воды нагревают при интен сивном перемешиваниип 14 ч при 500 С и после добавления 2 г (19.6 ммоль) концентрированной соляной кислоты перемешива ют еще 24 ч при этой температуре. После охлаждения до комнатной температуры ксуспензии бежевого цвета добавляют 50 мл этилацетата и нейтрализуют добавлением 7 мл 30-ным едким натром. Раствор этилацетата затем отделяют. высушивают над сульфатом натрия, фильтруют и раствори тель испаряют. Для очистки окрашенное вкоричневый цвет твердоевещество перекристаллизовывают из 20 мл иэопропанола при добавлении активированного угля. Желтоватые кристаллы плавятся при 112114 С. Выход 7.9 г (33 ммоль. 84 от теоони) . - о - . П р и ме р 4. Получение 2-анилин-4 гид роксиметил-б-циклопропилпиримидина (соединение 1.04).-а) К 414.1 г (59 ммоль) 2-анилино-4-форЧ мил-б-циклопропилпиримидина в 350 мл абсолютного метанола в течение 15 мин при. перемешивании при комнатной температуре, порциями добавляют 2.3 г(60 ммоль)смесь при выделении водорода нагреваетсядо 28 С Через 4 ч реакционную смесь под 1 кисляот прикапыванием 10 мл концентри рованной соляной кислоты по каплям добавляют 120 мл 10-ногораствора гидрокарбоната натрияби непосредственно после- творяют полностью в 600 мл диэтилового эфира при нагревании. обрабатывают актидвированным углем и фильтруют. Прозрачный фильтрат испаряют до появления мути.разбавляют петролейным эфиром и отфиль 6медленно в течение 30 мин по каплям добавляют 6.8 г (27 ммоль) бортрибромида. непосредственно после . этого удаляютохлаждающую баню и перемешивают еще 2 ч при комнатной температуре. После добавления 150 г воды со льдом выпавший сыройЗОВНВЗЮТ ИЗ МЗТЗНОЛЗ при применении ЭКтивированного угля. Светло-желтые . кристаллы плавятся при 124-126 С. Выход(50 ммоль) пиридина в 350 мл диэтилового эфира по каплям добавляют 30 мин при перемешивании 15.6 г (75 ммоль) тионилбромида в 50 мл диэтиловогоэфира. После 2 чперемешивания при КОМНЗТНОЙ ТЗМПВРЗТУре добавляют еще 0.4 г (50 ммоль) пиридина и нагревают 5 ч до температуры кипенияфлегмы. После охлаждения до комнатной. ттемпературы доба вляют 200 мл воды добавлением 140 мл насыщенного раствора гидрокарбоната натрия устанавливают значение рН раствора 7. После отделения фазы диэтилового эфира двакдыпромыва ют водой порциями по 100 мл. высушивают над сульфатом натрия, фильтруют и раство-ритель-испаряют. Оставшееся коричневое масло очищают с помощью колончатой хроматографии через силикагель (толуол/хлореформ/диэтиловыйвфир/петролейныйрения элюирующей смеси желтое маслоразбавляютсмесью диэтиловый эфир (петт релейный эфир) .т.кип. 0-7 ОС и ставят на холод для кристаллизацищжелтая кристал- . у эпическая пыль плавится при 77.579.5 С.(123 ммоль) высушенного возгонкой фтори 3476да калия и 0.3 г (1,13 ммоль) 18-краун-6 эфира нагревают в 50 мл ацетонитрила 40 ч до температуры кипения флегмы. После этого добавляют дополнительно 0.75 г (13 ммоль) фторида калия и нагревают 22 ч. для полного прохождения реакции еще раз добавляют 0,75 г (13 ммоль) высушенного возгонкой фторида калия и 0.1 г (038 ммоль) 18-краунб-эфира и дополнительно нагревают 24 ч до температуры кипения флегмы. После охлаждения до комнатной температуры суспензию смешивают с 150 мл диэтилового эфира. трижды промывают водой порциями по 20 мл. высушивают над сульфатом натрия. фильтруют и растворитель испаряют.Оставшееся коричневое МЗСЛО ОЧИЩЭЕТ Спомощью колончатой хроматографии через силикагель (толуолЛиюроформ/диэтиловый эфир/петролейный эфир т.кип. 5070 С. 5/3/1/1. После испарения элюирующей смеси желтое масло вносят в 10 мл петролейного эфира (т.кип. 5070 С) и помещают на холод для кристаллизации. Желтые кристаллы плавятся при 48-52 С.б) К суспензии 9.1 г (37.8 ммоль) 2-фениламино-4-гидроксиметил-б-циклопропилпи- римидина в 80 мл дихлорметана при перемешивании В течение 1 Ч ПО КЗПЛЯМ медленно добавляют 6.1 г (37.8 ммоль) диэтиламинотиотрифторида в 15 мл дихлорметана. После добавления 50 мл ледяной воды по каплям добавляют 50 мл 10-ного водного раствора гидрокарбоната натрия. По окончании выделения двуокиси углерода органическую фазу отделяют и водную фазу дважды экстрагируют дихлорметаном порциями по 20 мл. Соединенные растворы дихлорметана промывают водой (15 мл). высушивают над сульфатом натрия. фильт руют и испаряют растворитель. Оставшеесячерное масло очищают с помощью копончатой хроматографии через силикагель (толуол/хлороформ/диэтиловый эФир т.кип. 50-70 С. 5/3/1/1. Послеиспарения элюи рующей смеси желтое масло разбавляют 20мл петролейного эфира (т.пл. 5070 С) и помещают на холод для кристаллизации. Желтоватые кристаллы плавятся при 5052 С. Выход 4.9 г (20.1 ммоль. 53 от теории).комнатной температуре смешивают в 35 млэтанола с 15 мл концентрированной соляной кислоты. После 1 О-дневного стояния при комнатной температуре испаряют на роторном испарителе при температуре бани максимально 45 С. Остаток растворяют в 20 мл этанола. при этом очень быстро осаждается гидрохлорид реакционного продукта. При перемешивании добавляют 20 мл диэтилового зфира. выпавшие белые кристаллы отфильтровывают и промывают смесью атанола и диэтилового эфира и высушивают. В результате испарения фильтрата и перекристаллизации из смеси этанола и-диэтилового эфира (1 2) получают дополнительноеколичество гидрохлорида. Белые кристаллы плавятся при температуре выше 230 С. Вы- ход гидрохлорида 12.6 г (67.7 ммоль. 67,5 от теории).52.8 г (024 ммоль) гидрохлорида 2-гидрокси-д-метил-б-циклопропилпиримидина при перемешивании при комнатной температуре вносят в смесь 100 мл (1.1 ммоль) оксихлорида фосфора и 117 г (089 ммоль) диэтиланилина. при этом температура поднимается до 63 С. После нагревания в течение 2 ч до 110 С охлаждают до комнатной температуры и реакционную смесь при перемешивании переносят в смесь воды со льдом и метиленхлорида органическую Фазу отдаляют и промывают до нейтральной реакции насыщенным водным раствором гидрокарбоната натрия. После испарения растворителя получают 116.4 г масла. которое состоит из продукта реакции и диэтиланилина. Отделение диэтиланилина и очистку сырого реакционного продукта осуществляют с помощью колончатой хроматографии через силикагель(гексан/диэтилацетат 31). Через несколько дней закристаллизовавшееся бесцветное масло имеет показатель преломления под 1. 5419. Выход 35.7 г (011 ммоль. 87,5 от теории) т.пл. 3334 С.Раствор 5.5 г (50 ммопь) З-фторанилина и 9.3 г (55 ммопь) 2-хлор-4-метил-6-циклопропилпиримидина в 100 мл этанола при перемешивании добавлением 5 мл концентрированной соляной кислоты доводят до рН 1 и непосредственно после этогонагре вают 18 ч до температуры кипения флегмы.После охлаждения до комнатной температуры коричневую эмульсию доводят дод щелочной реакции добавлением 1 0 мл 30 ного аммиака. выливают .в 100 мл воды со яльдом и дваждыэкстрагируют диэтиловым эфиром порциями по 150 мл. Соединенныеэкстракты промывают 50 мл воды. высушивают над сульфатом натрия фильтруют ииспаряют растворитель. Оставшиеся желто БЗТНВ КОИСТЭПЛЫ ОЧИЩЗЮТ перекристалли зацией из смеси изопропиловый эфир(петролейный эфир) т.кип. 50-7 ОС. Белые. кристаллы плавятся при 87-899 С. Выход 8.3 г (34 ммольб 8 от теории).. 24.8 г (0.115 ммоль) гидрокарбоната 4 фторфенилгуанидина и 17.5 г (0.138 ммопь) у 1-циклопропил-1.3-бутандиона в 150 мл ме таноланагревают при перемешивании 24 чпри температуре кипения флегмы. причем образование двуокиси углерода через некоторое время явно уменьшается. Получен ный темно-коричневый прозрачный растворобрабатывают еще теплым активированным углем. фильтруют и фильтрат испаряютна роторном испарителе до отделения кри-сталлической массы и при перемешивании выливают в 500 мл воды Выпавшиекристаллы отфильтровывают. промывают небольшим количеством холодного этанола.явысушивают и перекристаллизовывают иэ смеси диизопропилового эфира и петролей ного эфира (50-70 С). Окрашенные в беже 5 вый цвет кристаллы плавятся при 89-91 С.62.2 г (03 ммопь) 95-ного гидрокарбоната фенилгуанидина помещают п 300 мл изопропанола и при перемешивании при внешней температуре 124 С нагревают до температуры кипения флегмы 78 С причем образуется суспензия, окрашенная в бежевый цвет. В течение 40 мин прикалывают 42.1 г (0.З ммопь) 1-(2-метилциклопропилЪЗ-бутандиона. при этом тотчас же начина- чется энергичное выделениегдиоксидауглерода. По окончании прикапывания реакциониую смесь нагревают 6 ч при переме У шивании при температуре кипения флегмы и после снижения наружной температурыконденсатора. После удаления. обогрева при внутренней температуре 60 С при пере-мешивании медленно добавляют 100 мл воды к коричневому раствору. который после добавления воды начинает медленно мут неть. После 12-часового перемешивания при комнатной температуре охлаждают в течение 1 ч до 5 С и в течение двух после- дующих часов до 3 С. выпавшую кашицувиз кристаллов отфильтровывают. промывают 40 мл холодной смеси (1 21) изопропанола и воды и высушивают белые кристаллы т.пл. 7374 С. Выход 51.4 г (О.215.ммоль. выход от теории 75.31,).л27 г (02 ммопь) фенилгуанидина в 200 д-мл диметилформамида при перемешивании .при комнатной температуре смешивают с 6 мл уксусной кислоты. После нагревания доохлаждения доукомнатной температуры ис паряют растворитель в вакууме и при пере- и темно-коричневуюмешивании А реакционную смесь выливают в 500 мл во ды. После установления рН 9 с помощью 0немного разбавленной щелочи (МаОН) дважды экстрагируют водную фазу диэтиловым эфиром порциями по 150 мл. соединенные экстракты промывают 200 мл водыи высушивают над сульфатом натрия. Фильтруют и эфир испаряют. Оставшееся масло
МПК / Метки
МПК: C07D 239/42, A01N 43/54
Метки: получения, производных, 2-анилинопиримидина, способ
Код ссылки
<a href="https://kz.patents.su/15-3476-sposob-polucheniya-proizvodnyh-2-anilinopirimidina.html" rel="bookmark" title="База патентов Казахстана">Способ получения производных 2-анилинопиримидина</a>