1-(2-Этоксиэтил)-4-этинил-4-оксипиперидин в качестве промежуточного соединения в синтезе гидрохлоридов 1-(2-этоксиэтил)-4-этинил-4-ацилоксипиперидинов, обладающих местноанестизирующей активностью
Номер патента: 3139
Опубликовано: 15.03.1996
Авторы: Шин Светлана Николаевна, Филимонова Лидия Алексеевна, Тараков Сатыбалды Амирбекович, Кондратенко Евгения Леонидовна, Ю Валентина Константиновна, Пралиев Калдыбай Джайловович, Исин Жумадил Искакович
Формула / Реферат
Изобретение касается гетероциклических соединений, в частности
1 - (2-этоксиэтил) -4-этинил-4-оксипиперидина, промежуточного соединения для синтеза гидрохлоридов 1-(2-этоксиэтил)-4этинил-4-ацилоксипиперидинов, обладающих местноанестезирующей активностью, что может быть использовано в медицине. Цель -создание нового промежуточного соединения для синтеза биологически активных веществ. Синтез нового соединения ведут реакцией 1-(2-этоксиэтил) -4-кетопиперидина с ацетиленом в присутствии едкого кали в жидком аммиаке. Выход 87%, т. пл. 81-82°С, брутто-ф-ла С14H19NO2. Синтезируемые на основе нового соединения вещества обладают местноанестезирующей активностью на уровне проксидола.
Текст
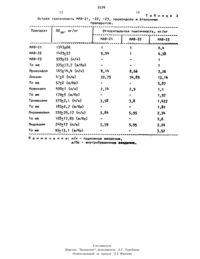
171,2 д г (1 моль) 1-(2-этоксиэтил)д-кетопиперидина в 300 мл эфира. Пропускают НСг-СН еще в течение д ч. Реакционную смесь оставляют в течение 12 ч, при этом происходит Часприбавляют 1500 мл воды, спИВТ 1 экстрагируют эфиром (2,0 Л). ИЗ эфирного экстракта выпадает осадок ацетипенового спирта 1, который отфильтровывают, промывают охлажденным эФиром сушат. маточный раствор спирта Е упаривают до 1/3 05 ЪеМЭ. выпавший осадок 1 отфильтровывают(0,235 ноль) уксусного ангидрида приливают 18 мл 10,25 моль) хлорис того ацетила. При этом смесь разогревается до до-Ц 5 с. Реакционную смесь оставляют при комнатной температуре в течение 2 ч. Выпавший осадок 11 отФильтровывают промывают ацетоном. маточный раствор упаривают досуха, остаток перекристаллизовывают из ацетона.20,0 г (01 моль) спирта 1 растворяют при нагревании в 130 мл (1 моль) пропионового ангидрида, затем приливают медленно 90 мл (1 моль) хлористого пролионила при этом смесь сильно разогревается. Реакционный раст 5 б,62 Н 8,0 Ц, вор выдерживают при 80-90 С в тече-.ние 7 ч. После охлаждения выпавший осадок отфильтровывают, промывают смесью ацетон - эфир (121), сушат. маточник упаривают досуха, остаток перекристаллизовывают из метилэтилкетона. Всего получают 26,3 (90,8 от теоретического) гидрохлорида 1-(2-этоксиэтил)-д-этинил-Ц-пропионилоксипиперидина с т.пл. 157-158 С, К 0,8.К 10,0 г (005 моль) ацетиленового спирта 1 в 100 мл сухого пиридина добавляют 21,1 г (17,3 мл, 015 моль)хлористого бензоилаупри этом наблю-ф дается разогревание смеси, раствор оставляют при комнатной температуре в течение 32 ч. Отгоняют пиридин остаток - темную массу, подкисляюте разбавленной соляной кислотой (11). Кислый раствор экстрагируют бензолом для удаления нейтральных продуктов,после чего раствор нейтрализуют поташом, основание бензоата извлекают бензолом, экстракт сушат сульфатом магния. К темно-коричневому бензольному раствору продукта добавляют 3 5 г активированного угля, смесь встря 58,12, н 8,25, ы ц,1 ь с 1 1 оь 9. в табл. 1, 3139кивают в течение 3 ч для поглощения углем смолистых продуктов. Отфильтровывают уголь, упаривают растворитель, остаток сушат в вакуум-эксикаторе, затем растворяют в 30 мл метилэтилкетона и подкисляют эфирным раствором НС 1 до рН 3-Ц, добавляют эфир до легкого помутнения. Выпав ший осадок отфильтровывают, промываютэфиром, перекристаллизовывают из смеси метилэтилкетон - этилацетат (123) и получаю 10,22 г (5966(от теоретического гидрохлорида 1- 2-этоксиэтил)-0-этинил-д-бензгилоксипиперидина с т. пл. 1738173 С К 085. 1 найдено 2 С 31 0 Н 7 я 5 Н д,21, С 1 10,00.Гидрохлориды -(2-этоксиэтил)-д-этинил-д-ацетоксипиперидипа (НАВ-21) 1- 2-этоксиэтил - -этинил -пропионилоксипиперидина (НАВ-22) и т-(2-этоксиэтил)-д-этинил-д-бензоилоксипиперидина (МАВ-23) испытаны на.местно-анестезирующую активность на каФедре Фармакологии Алма-Атинского государственного медицинского института.Местно-анестезирующую активность этих соединений изучали-по общепринятым методикам терминальная - по Ренье, инфильтрационная - по Больбрингу-Уэйду, проводниковая - по Искареву). Острую токсичность исследовали при подкожном (для МАВ-23) и при внутрнбрюшинном) введении на белых беспородных мышах обоего пола. массой 17-22 г. Анализ результатовработы проводили по показателям ин декс анестезии, ЭК 5, ЛЛ 5, длительность анестезии ч Активность и токсичность МАВ-21 22-23,сравнивали с аналогичнымипоказателями их структурного аналогалроксидола, и широко используемых местных анестетиков - дикаина, новокаина, тримекаина, лидокаина и пиромекаина.Данные по местноанестеэирующей активности всех веществ приведены по острой токсичности в табл. 2.Исследования показали, что НАВ-2 и -22 не обладают терминальной анес тезией, но проявляют активность при ИНФИЛЬТРаЦИонной и проводниковой видах анестезии. Анализ табл. 1 позволяет сделать вывод о том, что при инфильтрационной анестезии ИАВ-21 по активности сравним с эталонными препаратами, а МАВ-22 несколько превосходит их. Так, индекс анестезии в 0,5-ном растворе у МАВ-21 равен 19,5 У МдВ 22 357 у эталонных препаратов он колеблется в пределах 21-36. МАВ-21 дает в этой концентрации анестезию длительностью 5 мин,а МАВ - 22-28 мин. У сравниваемых препаратов она колеблется в пределах10-30 мин. По показателю экбд МАВ-21 несколько превосходит пиромекаин, но уступает остальным эталонным препаратам в 1,5-2 раза. НАВ-22 по ЭК 5 превосходит новокаин, тримекаин, пиромекаин и равенлидокаину. Структурный аналог предлагаемых препарато не обладает инфильтрационной анестезИей вСравнительная оценка активности при проводниковойанестезии показывает, что из двух препаратов МАВ-21 и НАВ-22 более активным является МАВ-22, превосходит НАВ-21 по всем показателям в 2-2,5 раза и сравним с эталонными препаратами. Так, в 2-ном растворе индекс анестезии у НАЗ-22 равен 385, у эталонных 310-598. длительность полной анестезии в этой концентрации у МАВ-22 равна 10 мин у пяти животных из девяти. Аналогичный показатель эталонных препаратов колеблется в пределах 10-30 мин для всекживотных. Экдо у НАВ-22 равен 1,202, у эталонных - 0,01-1,012. Проксидол несколько активнее МАВ-22.Анализ данных табл. 2 показывает,что оба препарата значительно менеетоксичны, чем сравниваемые вещества,св 3-30 раз при подкожном введении, что существенно увеличивает широту их фармакологического действия.МАВ-23, не обладая практически значимой терминальной анестезией(табл. 1), высоко активен при инфильтрационной и проводниковой анестезии. Так, при инфильтрационной анестезии индекс МАВ-23 в 0,5-ном растворе равен 33. вто время, как у новокаина, пиромекаина и дидокаи 3139 7на он колеблется в пределах 21-31. Только тримекаин в этой концентрации превосходит МАВ-23 (индекс равен 36). Длительность анестезии в этой концентрации равна 15 мин у НАВ-23,у эталонов - 10-30 мин. По показа-о телю экдд соединение МАВ-23 превосходит новокаин тримекаин и пиромекаин в 1,5-3 раза и равен лидокаиНУ. Проксидол не обладает активностью при инфильтрационной анестезии. о . При проводниковой анестезии НАВ 23 значительно превосходит все препараты по всем показателям. Так, есликонцентрации равен д 33 (722 от максимальной активности), то у сравниваемых препаратов аналогичная активиость появляется в концентрациях 12и выше. дпительностц аестеаии у изученногопрепарата в концентрации 0,12 равна 20 мн, у всех эталонов и прок-е сидела такая длительность появляется в концентрациях 0,53 и вше. по окааатеп эк КАБ-23 превосходит сравиваемне с ним впества в 206 раз при внутрибрюшинном еведенииВ 13 Раз при подкожном введении.Таким образом, МАВ 23 превосходит Проксидол и эталонные препараты по всем показателям инфильтрационной И проводниковой анестезии и обладает более низкой токсичностью, Ф О Р М У л а и 3 о б р е т е н и я1-(гчэтоксизтил)-дэтинилд-ок Сипиперидин Формулы НС 5 С ОН. 1 14в качестве промежуточного соединения в синтезе гидройлоридоа 1-(2-этоксиэтил)-д-этинил-д-ацилокси-п Пйперидинов общей Формулыпита д ига Два лад . ю.аш. ъмщ н жш.мм шш м.юн я о о ьо поьчо . ьц.ы . о. иы.о . о .ы ь. щ.о шы.ь ъ . .о.щ ъ о.ы ш.о т . М псэппосчппппчс асд.нп . . пягэгэпцнъя извини пинии полип 0. эв.ошхт . . М .оцьоо. сити н .юаьшо. ошжп к .кюцьохох п с ъ дщхюоьоотю квпозххцбводс .пшьооп шощдде цзногшмкп кшхмсюхххщон а
МПК / Метки
МПК: C07D 211/48
Метки: соединения, активностью, гидрохлоридов, 1-(2-этоксиэтил)-4-этинил-4-ацилоксипиперидинов, качестве, 1-(2-этоксиэтил)-4-этинил-4-оксипиперидин, обладающих, промежуточного, синтезе, местноанестизирующей
Код ссылки
<a href="https://kz.patents.su/8-3139-1-2-etoksietil-4-etinil-4-oksipiperidin-v-kachestve-promezhutochnogo-soedineniya-v-sinteze-gidrohloridov-1-2-etoksietil-4-etinil-4-aciloksipiperidinov-obladayushhih-mestnoanestizir.html" rel="bookmark" title="База патентов Казахстана">1-(2-Этоксиэтил)-4-этинил-4-оксипиперидин в качестве промежуточного соединения в синтезе гидрохлоридов 1-(2-этоксиэтил)-4-этинил-4-ацилоксипиперидинов, обладающих местноанестизирующей активностью</a>
Следующий патент: Электроперфоратор
Случайный патент: Композитная мука для выпечки хлеба