Иммуностимулирующее средство растительного происхождения
Номер патента: 24831
Опубликовано: 15.04.2014
Авторы: Зайцева Ирина Алексеевна, Алексюк Павел Геннадьевич, Коротецкий Илья Сергеевич, Богоявленский Андрей Павлинович, Березин Владимир Элеазарович
Формула / Реферат
Использование: в медицине, ветеринарии, а для повышения иммуногенности вакцин.
Задача изобретения является получение нового малотоксичного иммуностимулирующего средства для применения в медицинской и ветеринарной практике с целью повышения эффективности вакцинации.
Сущность изобретения:
Сущность изобретения заключается в получении сапонинсодержащего этанольного экстракта из корня растения Glycyrrhiza glabra L. с дальнейшим фракционированием сапонинсодержащего экстракта методом высокоэффективной жидкостной хроматографии (ВЭЖХ) для выделения очищенной сапонинсодержащей фракции с последующим лиофильным высушиванием. Полученное иммуностимулирующее средство обладает способностью эффективно стимулировать гуморальный, клеточный и протективный иммунитет против вирусных и паразитарных инфекций.
Положительный эффект:
Преимущества предлагаемого иммуностимулирующего средства растительного происхождения перед существующими заключаются в его низкой токсичности и высокой иммуностимулирующей активности при иммунизации в сочетании с различными антигенами вирусного и паразитарного происхождения, доступности сырья для получения препарата. Предлагаемое иммуностимулирующее средство, выделенное из растения Glycyrrhiza glabra L., позволяет расширить спектр препаратов для повышения эффективности и безопасности вакцинных препаратов и может быть использовано в качестве импортозамещающего средства в медицинской и ветеринарной практике.
Текст
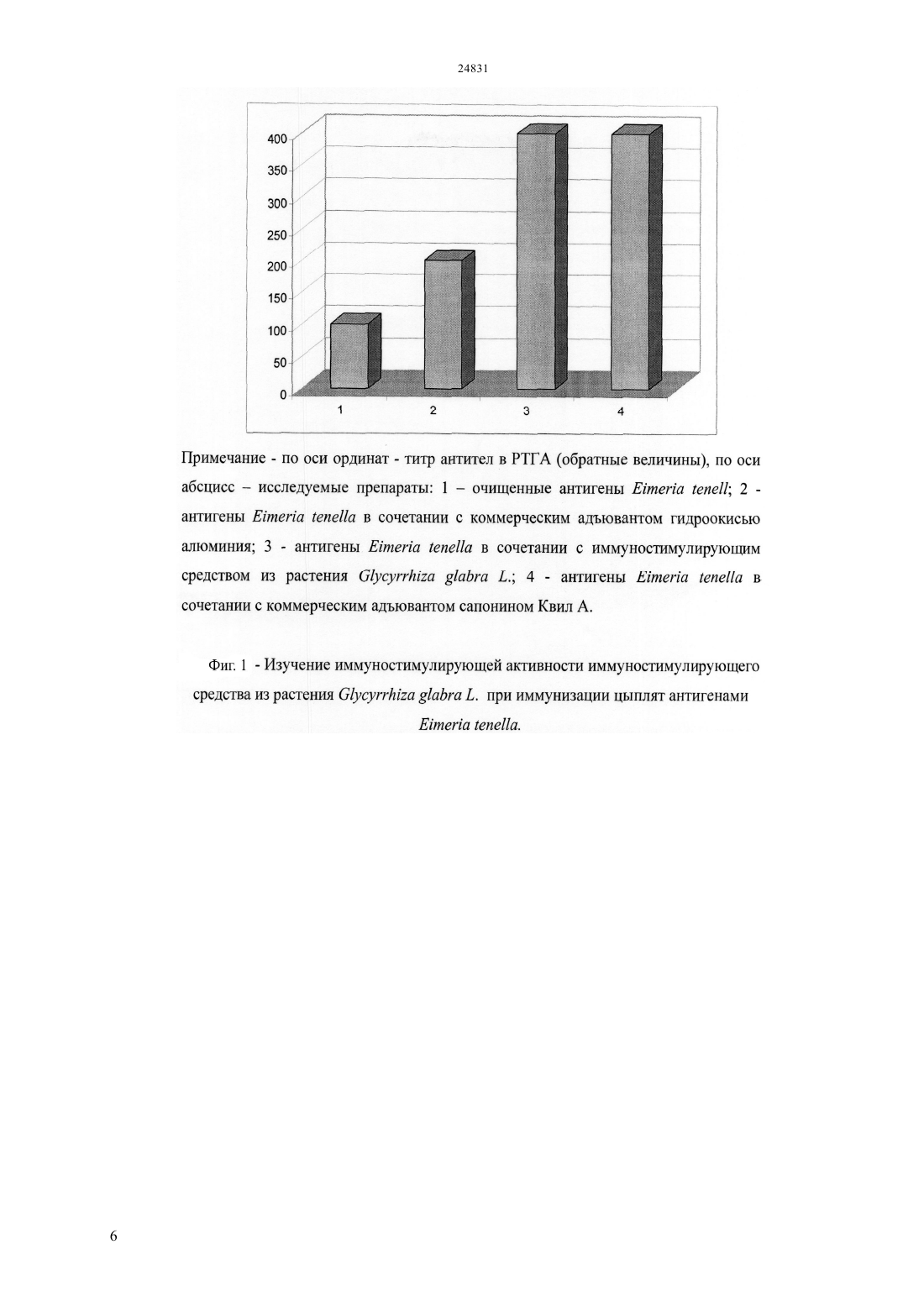
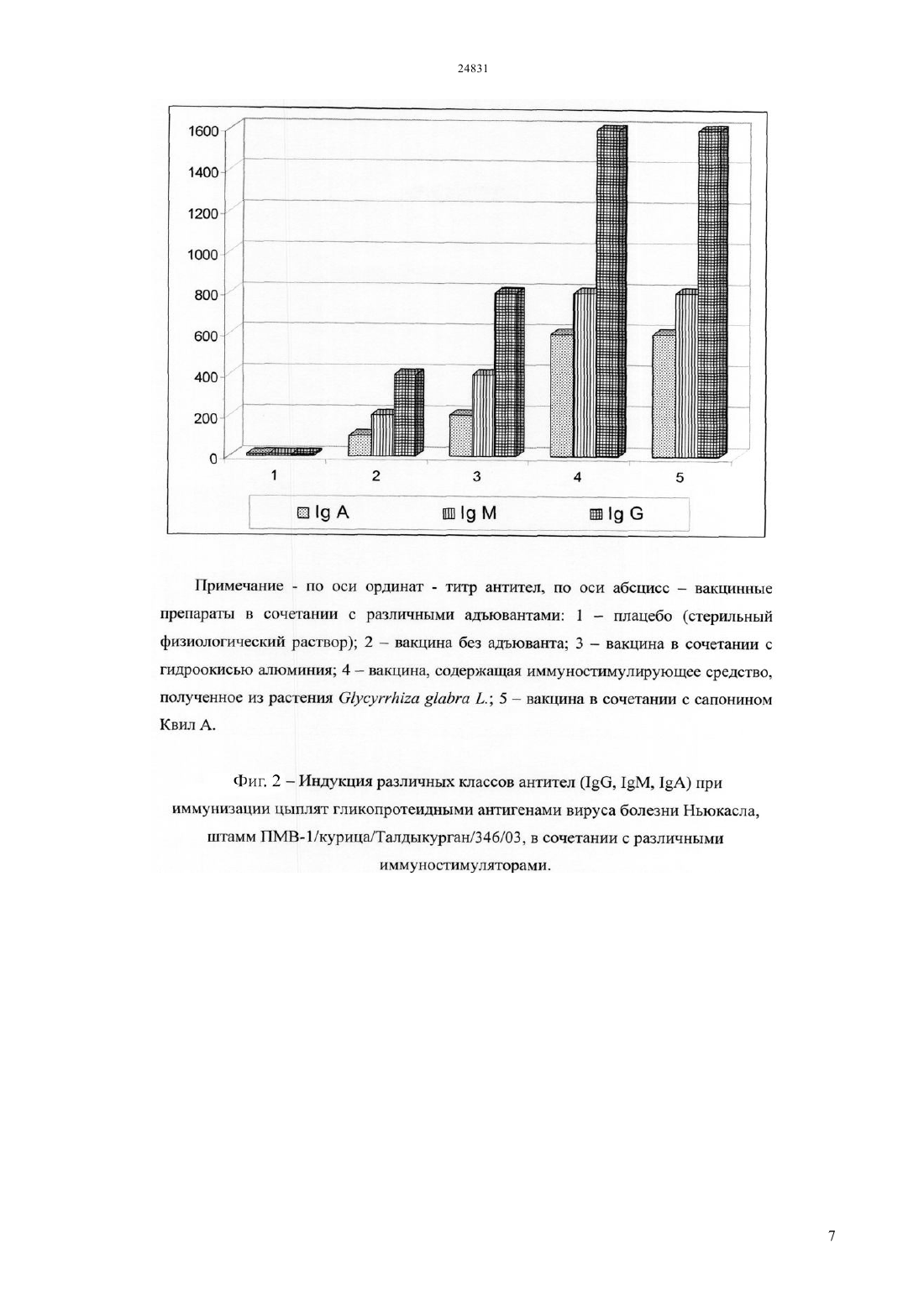
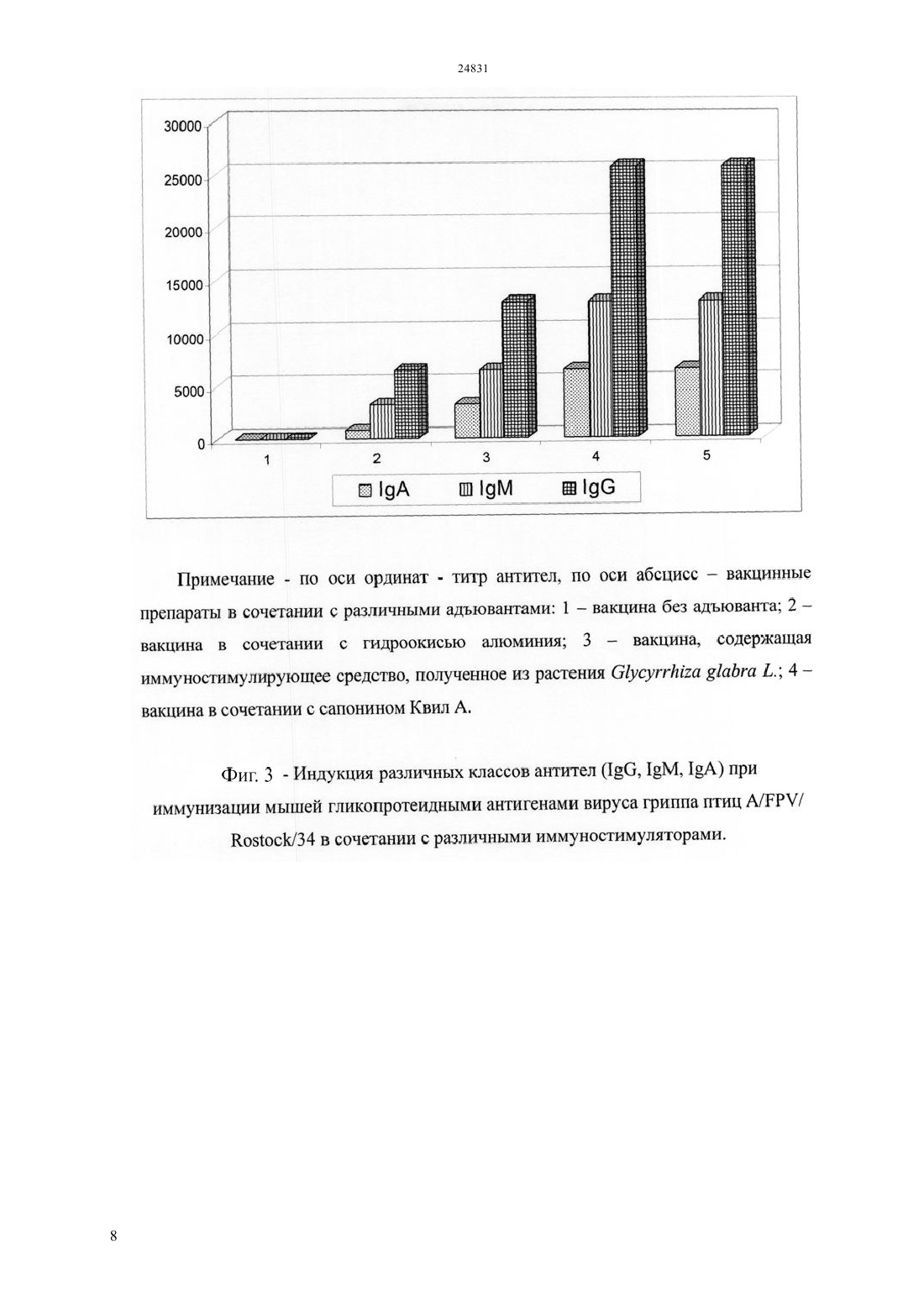
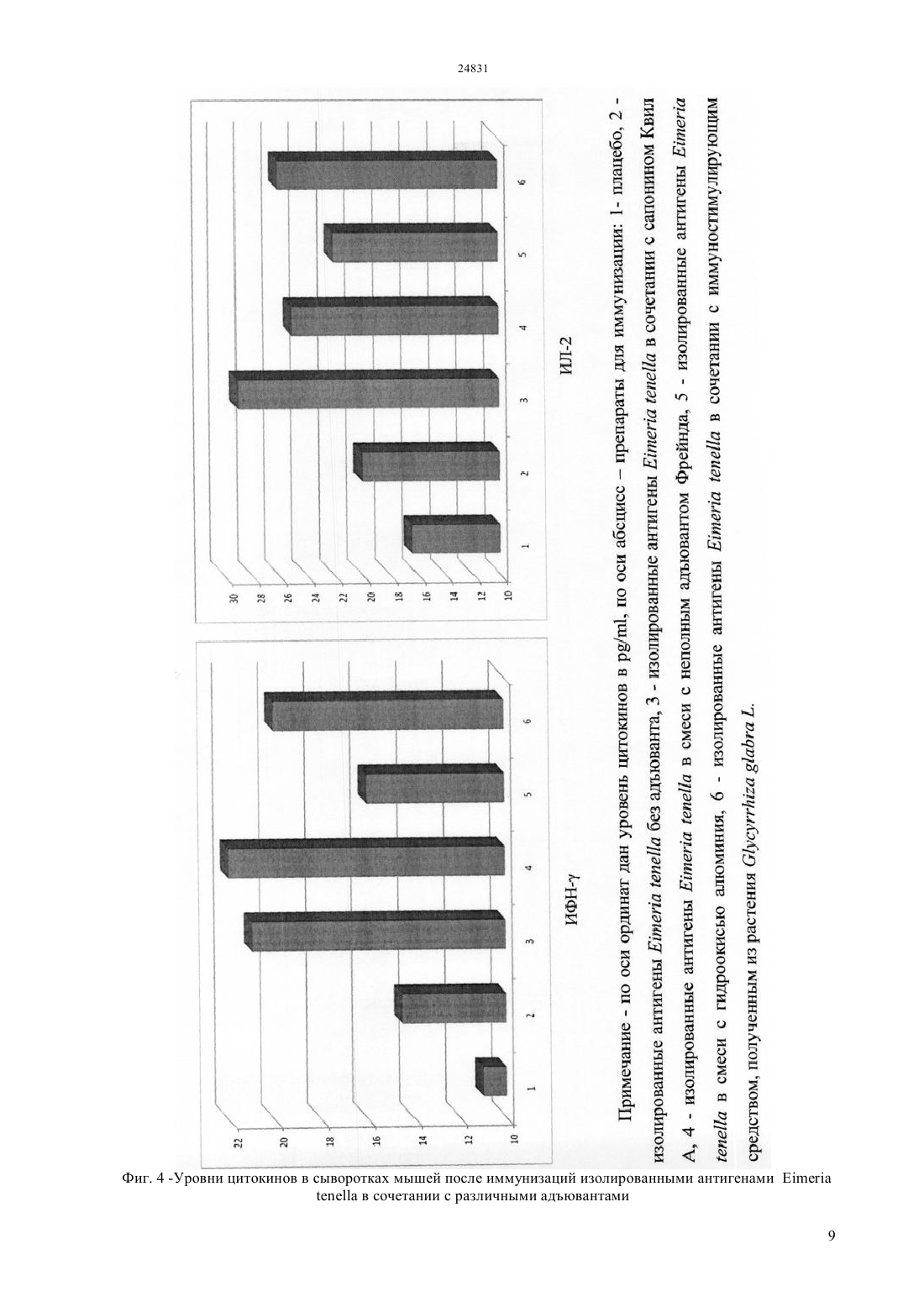
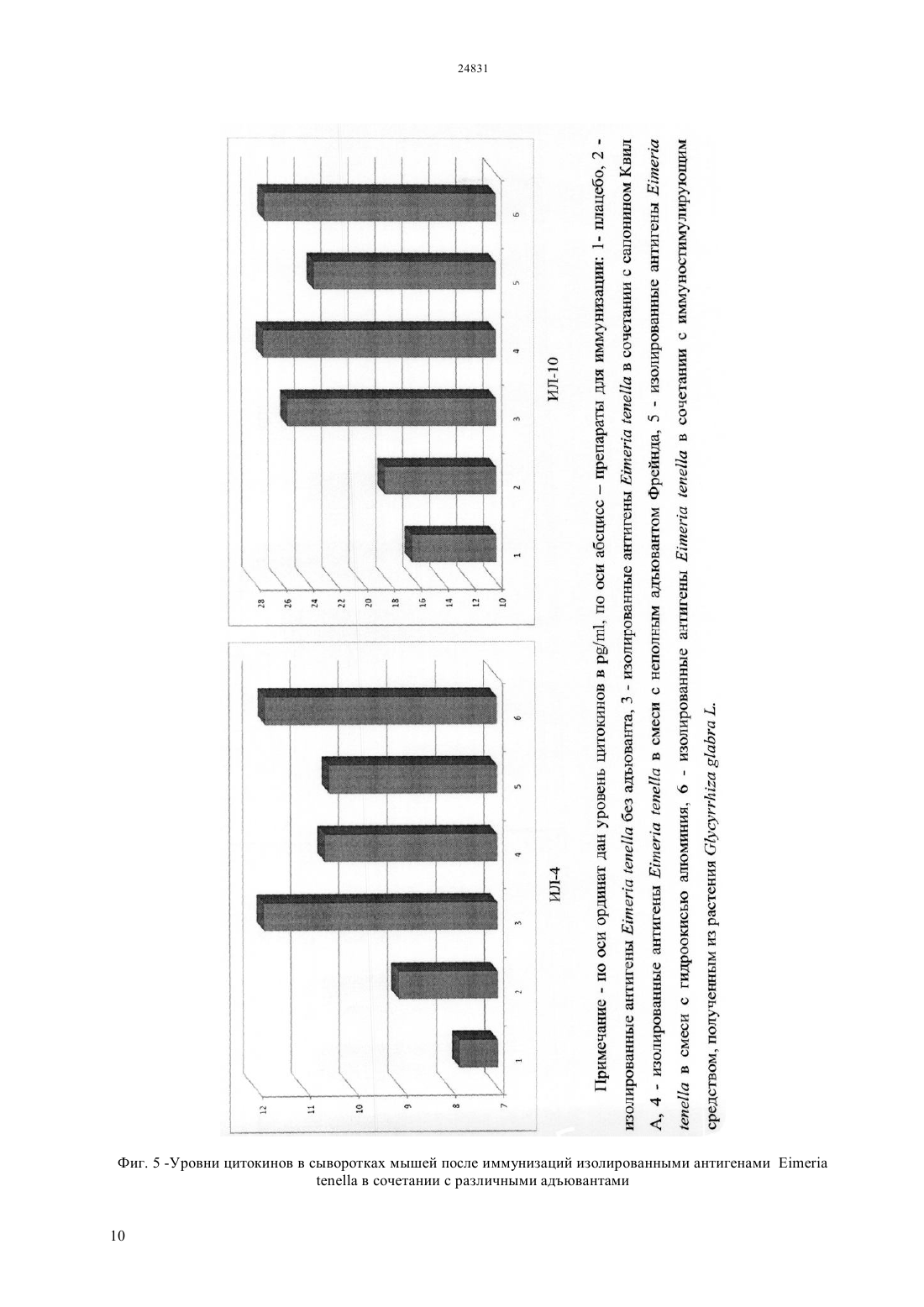
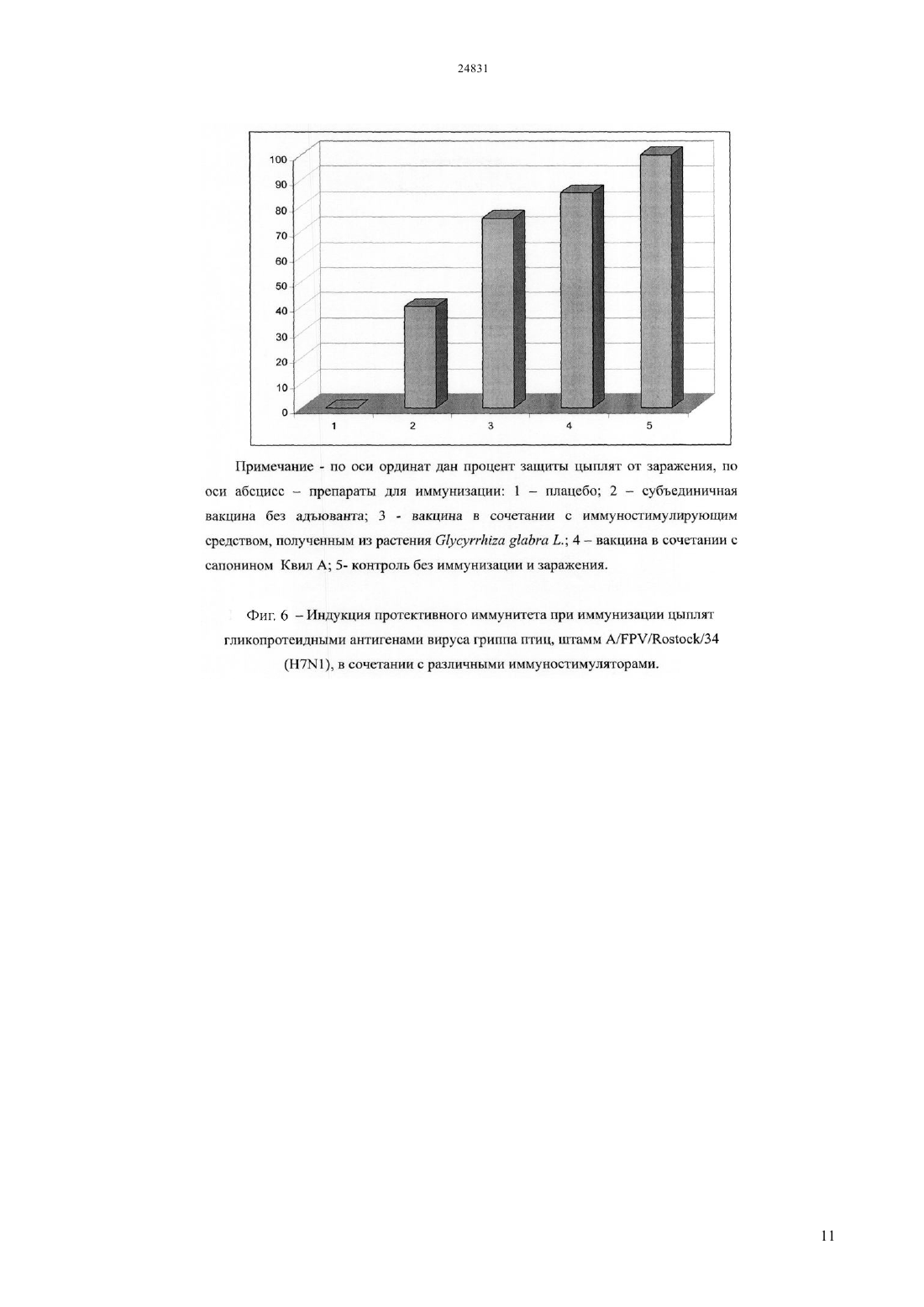
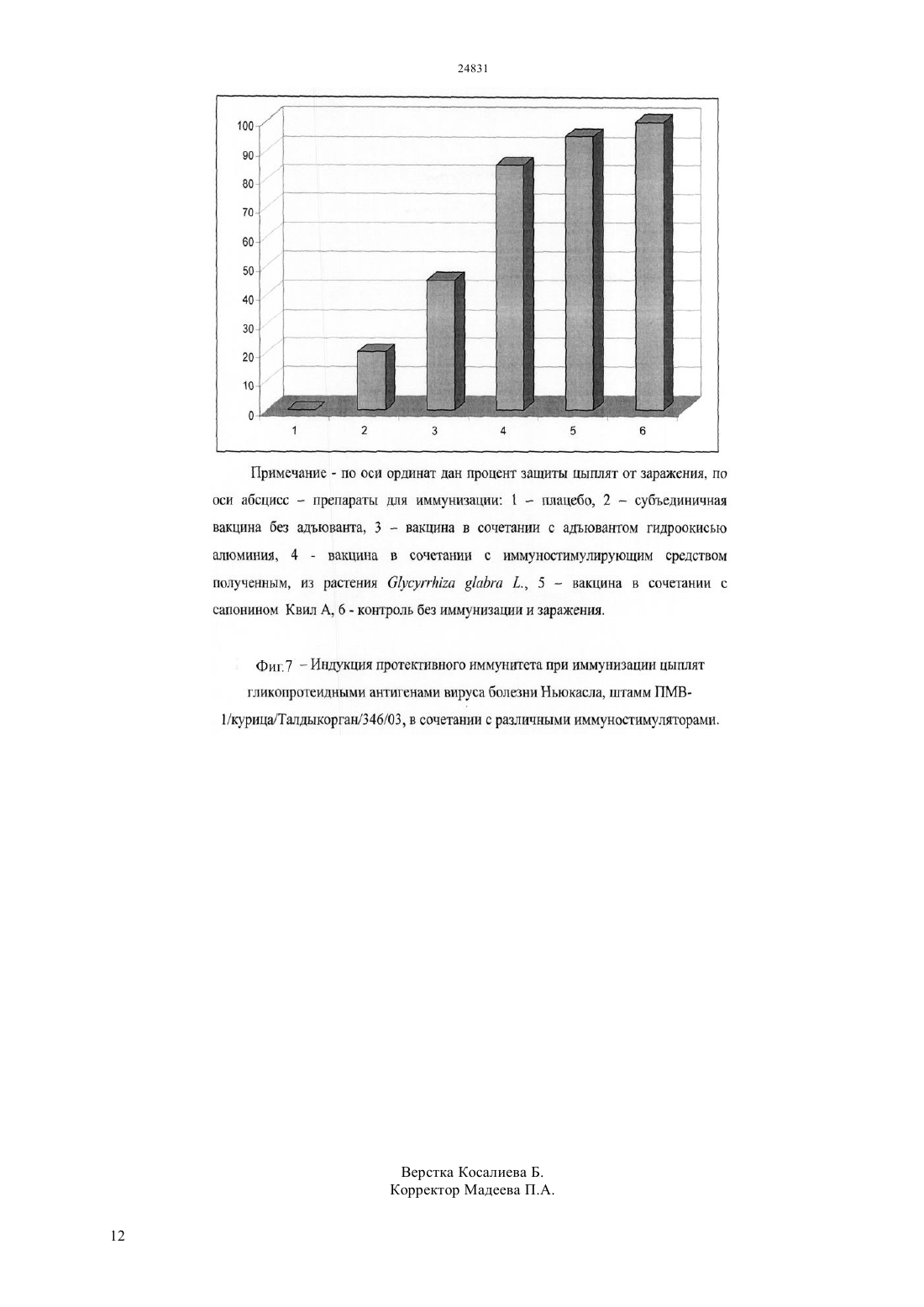
(51) 61 36/484 (2009.01) 61 37/04 (2009.01) КОМИТЕТ ПО ПРАВАМ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ МИНИСТЕРСТВА ЮСТИЦИИ РЕСПУБЛИКИ КАЗАХСТАН ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ИННОВАЦИОННОМУ ПАТЕНТУ фракционированием сапонинсодержащего экстракта методом высокоэффективной жидкостной хроматографии (ВЭЖХ) для выделения очищенной сапонинсодержащей фракции с последующим лиофильным высушиванием. Полученное иммуностимулирующее средство обладает способностью эффективно стимулировать гуморальный,клеточный и протективный иммунитет против вирусных и паразитарных инфекций. Положительный эффект Преимущества предлагаемого иммуностимулирующего средства растительного происхождения перед существующими заключаются в его низкой токсичности и высокой иммуностимулирующей активности при иммунизации в сочетании с различными антигенами вирусного и паразитарного происхождения,доступности сырья для получения препарата. Предлагаемое иммуностимулирующее средство,выделенное из растения.,позволяет расширить спектр препаратов для повышения эффективности и безопасности вакцинных препаратов и может быть использовано в качестве импортозамещающего средства в медицинской и ветеринарной практике.(72) Алексюк Павел Геннадьевич Березин Владимир Элеазарович Богоявленский Андрей Павлинович Зайцева Ирина Алексеевна Коротецкий Илья Сергеевич(73) Республиканское государственное предприятие на праве хозяйственного ведения Институт микробиологии и вирусологии Комитета науки Министерства образования и науки Республики Казахстан(54) ИММУНОСТИМУЛИРУЮЩЕЕ СРЕДСТВО РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ(57) Использование в медицине, ветеринарии, а для повышения иммуногенности вакцин. Задача изобретения является получение нового малотоксичного иммуностимулирующего средства для применения в медицинской и ветеринарной практике с целью повышения эффективности вакцинации. Сущность изобретения Сущность изобретения заключается в получении сапонинсодержащего этанольного экстракта из корня растения. с дальнейшим Изобретение относится к области медицины и ветеринарии,а именно к разработке иммуностимуляторов растительного происхождения. Известен адъювант сапонин Квил А, получаемый путм экстракции из коры южно-американского дерева( 4432969 211984, ,.). Недостатком данного препарата является относительно высокая токсичность и труднодоступность сырья в Республике Казахстан. Данный препарат является наиболее близким аналогом по отношению к заявленному изобретению. Известен иммуностимулирующий препарат Стимфорте представляющий собой комплекс низкомолекулярных природных соединений (патент 2003137519/15, заявка 6 октября 2005 г. Ильичев А.В., Бельков А.П., Мальдов Д.С,Асташкин Е.И. ЗАО Скай ЛТД). Недостатком данного препарата является неспособность стимулировать все звенья иммунного ответа. Известно иммуностимулирующее средство растительного происхождения, представляющее собой масло, выделенное из семян амаранта. Данный иммуностимулятор дает четко выраженный иммуностимулирующий эффект (патент 2000128729/14 заявка 17 ноября 2000 г.,Чернеховская Н.Е. Чернеховский Д.В. Черных С.Б. Данков ). Недостатком данного препарата является токсичность и высокий риск возникновения аллергических реакций. Известно иммуностимулирующее средство-. Данный адъювант состоит из полинуклеотидов стимулирующих синтез антигенспецифических антител (/2006/131023,142006, , ). Недостатком данного препарата является высокая сложность производства и неспособность стимулировать все звенья иммунного ответа. Целью изобретения является получение нового малотоксичного иммуностимулирующего препарата для применения в медицинской и ветеринарной практике с целью повышения эффективности вакцинопрофилактики. Для достижения поставленной цели был приготовлен иммуностимулирующий препарат в виде лиофильно высушенной сапонинсодержащей фракции, полученной из экстракта корня растения. Сущность изобретения заключается в получении сапонинсодержащего этанольного экстракта из корня растения. с дальнейшим фракционированием сапонинсодержащего экстракта методом высокоэффективной жидкостной хроматографии (ВЭЖХ) для выделения очищенной сапонинсодержащей фракции с последующим лиофильным высушиванием. Полученное иммуностимулирующее средство обладает способностью эффективно стимулировать гуморальный,клеточный и протективный иммунитет против вирусных и паразитарных инфекций. Преимущества предлагаемого 2 иммуностимулирующего средства растительного происхождения перед существующими заключаются в его низкой токсичности и высокой иммуностимулирующей активности при иммунизации в сочетании,с различными антигенами вирусного и паразитарного происхождения, доступности сырья для получения препарата. Предлагаемое иммуностимулирующее средство, выделенное из растения, позволяет расширить спектр препаратов для повышения эффективности и безопасности вакцинопрофилактики и может быть использовано в качестве импортозамещающего препарата в медицине и ветеринарии. Предлагаемое иммуностимулирующее средство представляет собой аморфный порошок горчичного цвета, без запаха. Порошок гигроскопичен,растворим в воде очищенной, 50 ацетонитриле,30 растворе кислоты уксусной и 10 растворе натрия гидроксида, мало растворим в эфире диэтиловом, практически нерастворим в бензоле и хлороформе. Подлинность препарата подтверждается с помощью 5 качественных реакций а) обработка раствором метилового красного в этаноле позволяет обнаружить в растительном экстракте наличие органических кислот (красное окрашивание) б) обработка 3,5-динитросалицилатом с последующим нагреванием при 105 С позволяет определить наличие восстанавливающих сахаров (черное окрашивание) и невосстанавливающих сахаров(серо-зеленое окрашивание) в) обработка 0,5-ным раствором йода в хлороформе позволяет обнаружить основания и липиды (коричневое окрашивание) г) обработка раствором аммиака позволяет обнаружить флавоноиды(желтокоричневое окрашивание) д) обработка 10 растворам О 3 в концентрированной серной кислотой (реакция Лафона) позволяет определить сапонины(кроваво-красное окрашивание). Сущность изобретения поясняется на следующих примерах. Пример 1. Для получения сапонинсодержащего иммуностимулирующего средства корень растения. измельчают до получения частиц диаметром 2-4 мм. Измельченный корень обрабатывают 2-3 раза 5-кратным объемом хлороформа при комнатной температуре в течение 1,5 часов. После удаления хлороформа растительную массу экстрагируют 3-кратным объемом 75-85 этанола в течение 18 часов при комнатной температуре. Полученный экстракт лиофильно высушивают и используют для фракционирования. Очищенные сапонины получают путем фракционирования методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Разделение проводят в градиенте ацетонитрила 0-80 в присутствии 0,1 трифлуороуксусной кислоты(ТФА) на колонкеС 18, 5, 21,2100 мм. На колонку наносят 500 мг экстракта, разведенного в 3 мл бидистиллированной воды. Контроль за хроматографическим процессом осуществляют спектрофотометрическим методом при длинах волн 254 нм и 353 нм. Отбирают фракцию с поглощением оптической плотности при 254 нм (зона поглощения сапонинов) и минимальным поглощением при 353 нм (зона поглощения флавоноидов). Полученный препарат лиофильно высушивают. Контроль содержания иммуностимулирующего средства проводят с помощью качественной химической реакции на сапонины (Реакция Лафона) и путем хроматографического анализа. При хроматографическом анализе в препарате выявляется основной пик при длине волны 254 нм,соответствующий сапонинам. Содержание сапонинов в конечном препарате составляет не менее 70 от сухой массы. Пример 2. Определение токсичности иммуностимулирующего средства, полученного из растения., проводят на модели куриных эмбрионов, мышей и 1-дневных цыплят. Доза препарата составляет 1000 мкг на животное,200 мкг на животное и 40 мкг на животное. Токсичность определяют с помощью подкожного или интраназального введения исследуемого материала мышам и цыплятам (токсичность на животных) или путем инокуляции препаратов в хорион-аллантоисную полость куриных эмбрионов(эмбриотоксичность). Токсичность полученного препарата сопоставляют с токсичностью коммерческого препарата, сапонина Квил А, производства компанииАВ. Швеция (таблица ). Результаты таблицы показывают, что заявленное иммуностимулирующее средство в отличие от коммерческого препарата острой токсичностью в указанном диапазоне концентраций не обладает. Пример 3. Активность индукции гуморального иммунного ответа определяют при иммунизации однодневных цыплят породы белый Леггорн антигенами мерозоитов и спорозоитовв сочетании с иммуностимулирующим средством,выделенным из растения. Антигеныв дозе 10 мкг/цыпленок смешивают с иммуностимулирующим средством в дозе 10 мкг/цыпленок. Цыплят иммунизируют однократно, подкожно. Для сравнения цыплят иммунизируют антигенамибез иммуностимулятора и этими же антигенами в сочетании с адъювантами гидроокись алюминия и Квил А, в тех же дозах. Через 2 недели после иммунизации производят забор крови у цыплят для определения уровня антител. Антитела определяют с помощью иммуноферментного анализа. Результаты испытаний приведены на рисунке 1. Показано, что иммунизация цыплят антигенами в сочетании с иммуностимулирующим средством, выделенным из растения. в 4 раза увеличивает титр антител в крови цыплят по сравнению с иммунизацией антигенами без иммуностимулятора и в 2 раза по сравнению с иммунизацией антигенами в сочетании с адъювантом гидроокисью алюминия. Уровень антител при иммунизации антигенами в сочетании с коммерческим адъювантом Квил А был сопостовим с уровнем антител, образуемым при иммунизации цыплят антигенами мерозоитов и спорозоитов в смеси с иммуностимулирующим средством, выделенным из корня. Пример 4. Активность гуморального иммунитета определяют при подкожной иммунизации 7 дневных цыплят породы белый Леггорн антигенами вируса болезни Ньюкасла(ВБН),штамм ПМВ 1/курица/Талдыкурган/346/03 в сочетании с иммуностимулирующим средством, полученным из растения. Изолированные гликопротеидные антигены ВБН в дозе 10 мкг/цыплнок смешивают с иммуностимулирующим средством, полученным из растения. в дозе 10 мкг/цыплнок. Для сравнения цыплят иммунизируют изолированными гликопротеидами ВБН в сочетании с коммерческими адъювантом гидроокисью алюминия и сапонином Квил А, а также изолированными гликопротеидами без адъюванта. Кровь забирают через 2 недели после однократной иммунизации, в сыворотках крови цыплят проводят определение уровня , , . Для выявления антител используют меченые пероксидазой хрена моноклональные антитела к определенным классам иммуноглобулинов. Результаты анализов приведены на рисунке 2. Показано, что иммунизация животных антигенами вируса болезни Ньюкасла в сочетании с иммуностимулирующим средством из растения. стимулирует образование антител классов , ,в 2 раза больше по сравнению с иммунизацией антигенами ВБН в сочетании с гидроокисью алюминия и в 4 раза больше по сравнению с иммунизацией антигенами ВБН без адъюванта. Также установлено, что титры различных классов иммуноглобулинов после иммунизации вакцинным препаратом,содержащим иммуностимулирующее средство из растения., сопоставимы с титрами антител при иммунизации вакциной, содержащей в качестве адъюванта сапонин Квил А. Необходимо отметить значительно меньшую токсичность заявляемого иммуностимулирующего средства из растения. по сравнению с коммерческим препаратом сапонина Квил А. Пример 5. Активность гуморального иммунитета определяют при иммунизации мышей гликопротеидными антигенамивируса гриппа птиц (ВГП), штамм ///34(71) в сочетании с иммуностимулирующим средством, полученным из растения. Мышей иммунизируют подкожно,иммунизацию проводят двукратно с интервалом в 3 недели. Мышам вводят 10 мкг антигена и 10 мкг 3 иммуностимулирующего средства. Иммуногенную активность вакцинного препарата, содержащего иммуностимулирующее средство из растения.,сравнивают с иммуногенностью вакцинных препаратов,содержащих коммерческий адъювант Квил А и адъювант гидроокись алюминия, а также с иммуногенностью очищенных антигенов без адъювантов. Кровь у мышей забирают через 7 суток после повторной иммунизации. В сыворотках крови методом ИФА определяют содержание вирусспецифических иммуноглобулинов классов, , . Результаты испытаний приведены на рисунке 3. Установлено, что двукратная иммунизация мышей изолированными гликопротеидными антигенами ВГП в сочетании с иммуностимулирующим средством, полученным из растения., индуцирует образование высоких титров антител классов , , , сопоставимых с титрами антител после иммунизации мышей вакциной, содержащей коммерческий адъювант сапонин Квил А, в 2 раза выше по сравнению с иммунизацией мышей антигенами ВГП в смеси с адъювантом гидроокисью алюминия и в 3 раза выше по сравнению с иммунизацией антигенами без иммуностимулятора. Пример 6. Изучение способности стимулировать синтез факторов клеточного иммунитета проводят при иммунизации белых мышей массой 18-20 г антигенамив сочетании с иммуностимулирующим средством, полученным из растения. Мышей иммунизируют подкожно, двукратно с интервалом в 3 недели, доза антигена и иммуностимулирующего средства составляет 10 мкг/мышь. Кровь у мышей собирают через 7 дней после бустер-иммунизации и проводят определение наличия цитокинов -, -2, -4, -10. Цитокины выявляют методом иммуноферментного анализа с использованием коммерческих тестсистем фирмы(США). Активность образования цитокинов при иммунизации антигенамив смеси с иммуностимулирующим средством, выделенным из растения., сравнивают с активностью стимуляции цитокинов при иммунизации очищенными антигенами без адъювантов, а также антигенами в смеси с сапонином Квил А, адъювантом гидроокисью алюминия, а также неполным адъювантом Фрейнда. Результаты исследований, приведнные на рисунках 4 и 5, показывают, что антигеныв сочетании с иммуностимулирующим средством, полученным из растения,. индуцируют образование практически равного уровня интерлейкинов Т - хелперов 1-го типа (ИФН-, ИЛ-2) и Т - хелперов 2-го типа (ИЛ-4,ИЛ-10). Активность индукции цитокинов предлагаемым иммуностимулирующим средством сопоставима с активностью стимуляции образования цитокинов под действием сапонина 4 Квил А и превосходит таковую при введении в состав вакцины адъюванта гидроокись алюминия и неполного адъюванта Фрейнда. Пример 7. Активность протективного иммунитета определяют после иммунизации цыплят вакциной против вируса гриппа птиц (ВГП), штамм///34(71),в условиях экспериментального заражения. Однодневных цыплят иммунизируют подкожно субъединичной вакциной, содержащей очищенные изолированные гликопротеидные антигены ВГП, штамм ///34 (71), и иммуностимулирующее средство, полученное из растения. Доза антигена и адъюванта составляет 10 мкг/животное. Через 14 дней после однократной иммунизации цыплят заражают вирусом ///34 (71) в дозе 100 ЛД 50 на цыплнка. Контрольные группы цыплят иммунизируют субъединичной гриппозной вакциной, содержащей адъювант сапонин Квил А, а также вакциной без адъювантов. Наблюдение за цыплятами проводят в течение 14 дней после заражения, учитывая число выживших и павших животных. Результаты оценки защитных свойств различных вакцинных препаратов представлены на рисунке 6. Показано, что иммунизация цыплят антигенами ВГП в сочетании с иммуностимулирующим средством из растения. индуцирует защиту от летального заражения вирусом гриппа птиц у 70 цыплят. Для сравнения,аналогичная иммунизация вакциной в сочетании с коммерческим адъювантом сапонином Квил А защищала от заражения около 80 цыплят, но при более высоком уровне токсичных реакций, а иммунизация вакциной без адъювантов индуцирует протективный иммунитет только у 40 цыплят. Пример 8. Активность протективного иммунитета определяют при иммунизации цыплят вакциной против вируса болезни Ньюкасла (ВБН), штамм ПМВ-1/курица/Талдыкорган/346/03, в условиях экспериментального заражения цыплят. Антигены ВБН в дозе 10 мкг/цыпленок смешивают с иммуностимулирующим средством,полученным из растения., в дозе 10 мкг/цыпленок. Цыплят иммунизируют однократно путем подкожного введения исследуемого препарата. Для сравнения цыплят иммунизируют антигенами ВБН в сочетании с коммерческим препаратом сапонина Квил А,адъювантом гидроокисью алюминия, а также антигенами без адъювантов. Через 2 недели после однократной иммунизации цыплят заражают вирусом ПМВ 1/курица/Талдыкорган/346/03 в дозе 105 ЭИД 50/цыпленок. Наблюдение за зараженными птицами проводят в течение 2 недель, учитывая количество павших и выживших цыплят. Результаты оценки защитных свойств различных вакцинных препаратов представлены на рисунке 7. Показано, что иммунизация цыплят субъединичной вакциной, содержащей антигены ВБН штамм ПМВ 1/курица/Талдыкорган/346/03 в смеси с иммуностимулирующим средством из растения. индуцирует защиту от летального заражения ВБН у 85 цыплят. Иммунизация цыплят вакциной, в сочетании с адъювантом Квил А защищала 95 цыплят, но при более высоком уровне токсичных реакций. Иммунизация субъединичной вакциной,включающей в качестве адъюванта гидроокись алюминия, защищала 45 цыплят от заражения, а вакцина без адъюванта - 20 цыплят. Таким образом,сапонинсодержащее иммуностимулирующее средство, полученное из растения., может быть эффективно использовано в качестве адъюванта для повышения иммуногенности и защитных свойств вакцинных препаратов, содержащих различные антигены паразитарного и вирусного происхождения, при меньшей токсичности данного иммуностимулирующего средства по сравнению с известным аналогом сапонином Квил А. ФОРМУЛА ИЗОБРЕТЕНИЯ Иммуностимулирующее средство растительного происхождения,обладающее способностью стимулировать гуморальный,клеточный и защитный иммунитет при иммунизации вирусными и паразитарными антигенами, отличающееся тем,что в качестве иммуностимулирующего средства используется лиофильно высушенная сапонинсодержащая фракция, полученная из растения. (солодка голая) путем спиртовой экстракции измельченного корня растения с последующим фракционированием экстракта методом высокоэффективной жидкостной хроматографии(ВЭЖХ) и лиофильным высушиванием сапонинсодержащей фракции, при содержании сапонинов в конечном продукте не менее 70 от сухой массы препарата. Фиг. 4 -Уровни цитокинов в сыворотках мышей после иммунизаций изолированными антигенамив сочетании с различными адъювантами 9 Фиг. 5 -Уровни цитокинов в сыворотках мышей после иммунизаций изолированными антигенамив сочетании с различными адъювантами
МПК / Метки
МПК: A61P 37/04, A61K 36/484
Метки: иммуностимулирующее, средство, происхождения, растительного
Код ссылки
<a href="https://kz.patents.su/12-24831-immunostimuliruyushhee-sredstvo-rastitelnogo-proishozhdeniya.html" rel="bookmark" title="База патентов Казахстана">Иммуностимулирующее средство растительного происхождения</a>
Предыдущий патент: Закваска «Казбиосил» для силосования растительных кормов (варианты)
Следующий патент: Способ получения единого бруцеллезного антигена
Случайный патент: Способ приготовления бетонной смеси