Способ борьбы с нежелательной растительностью
Формула / Реферат
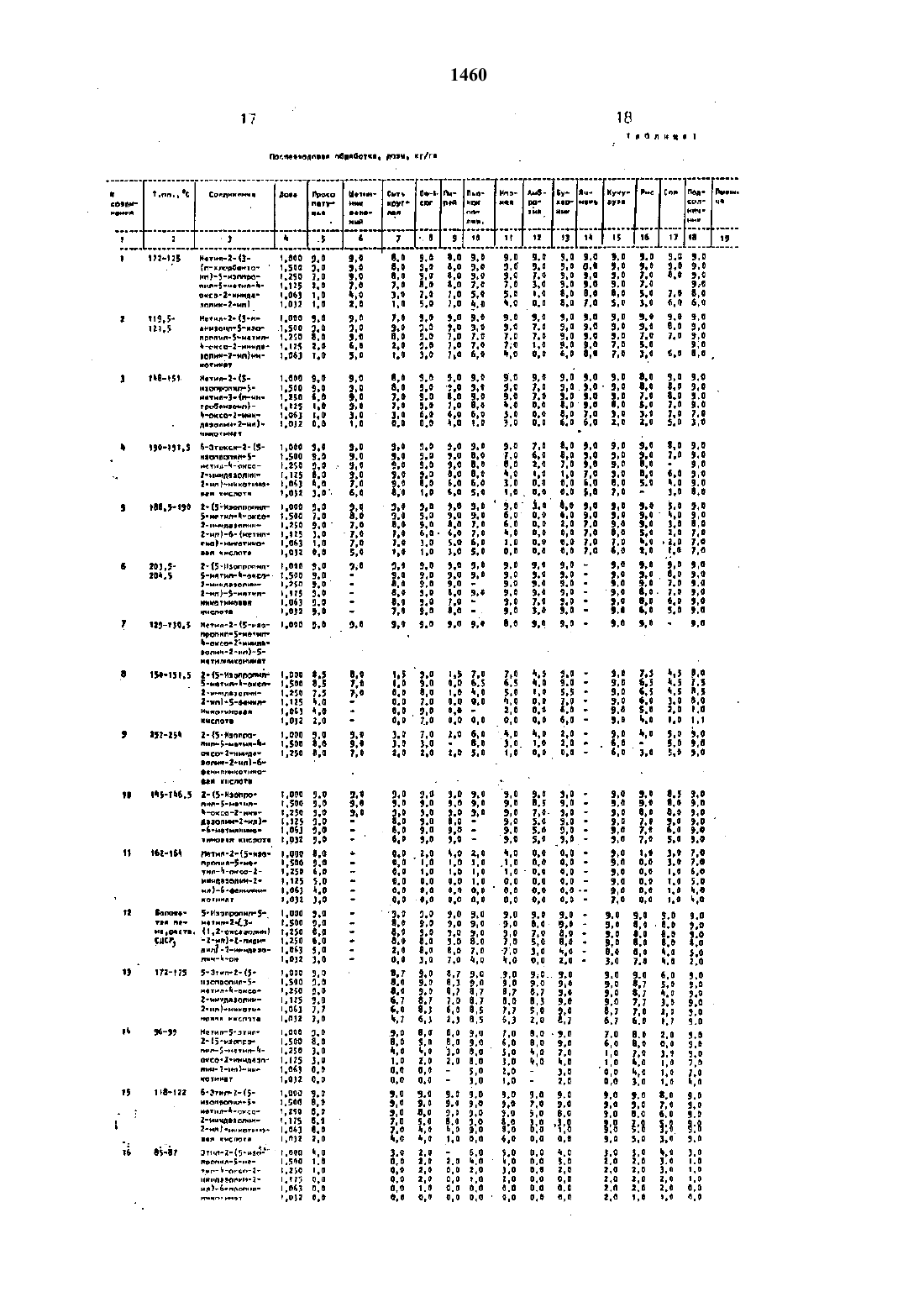
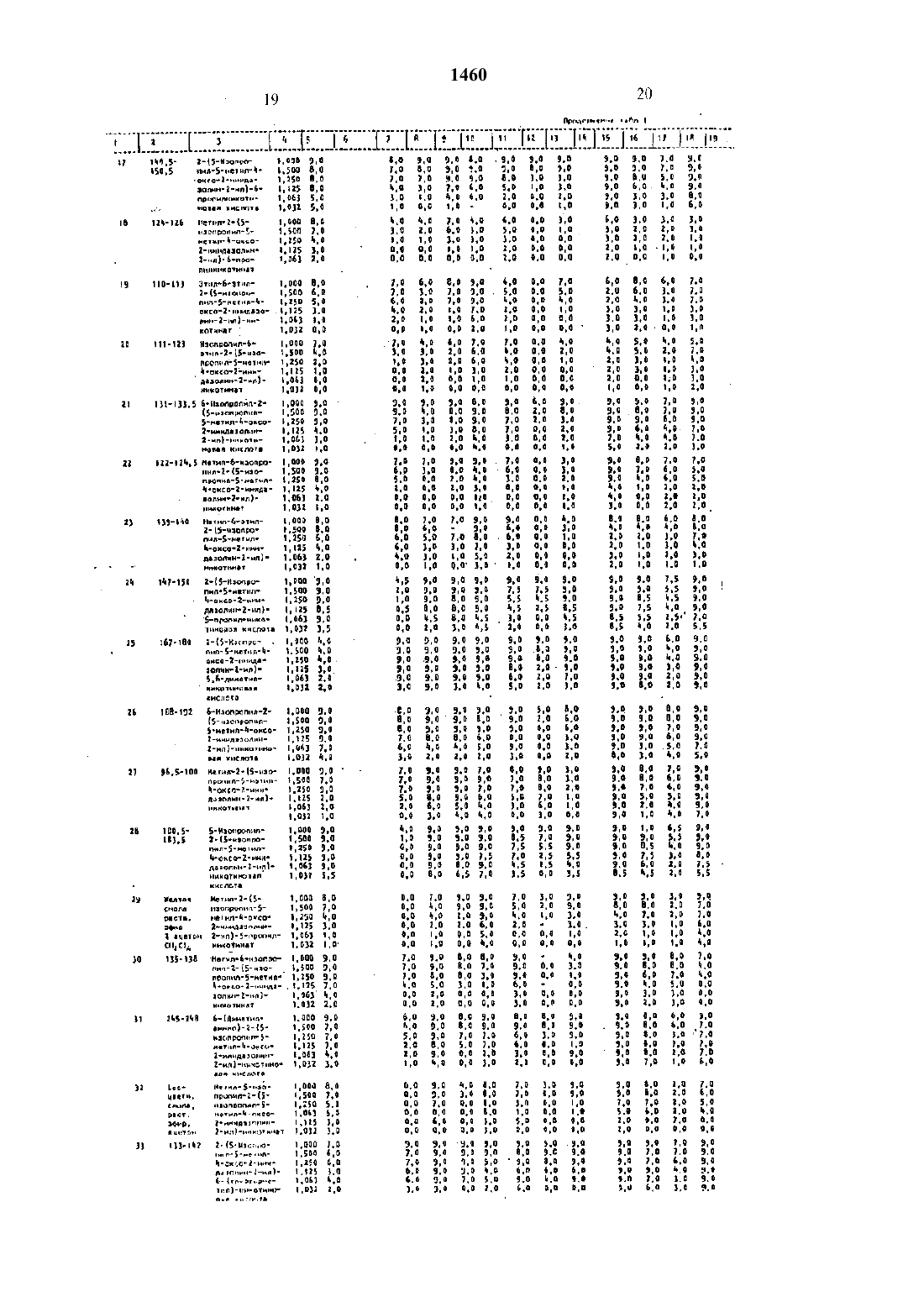
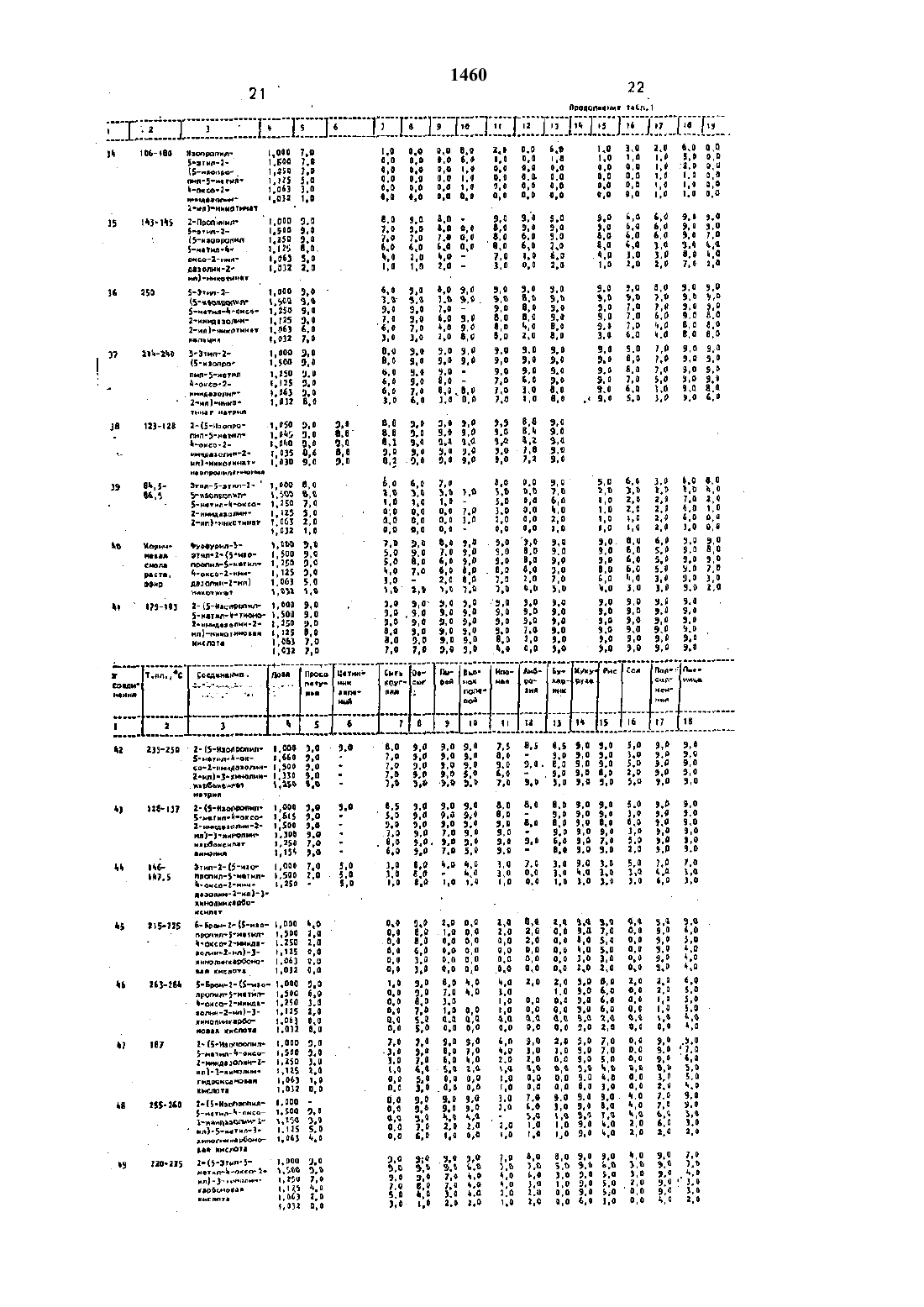
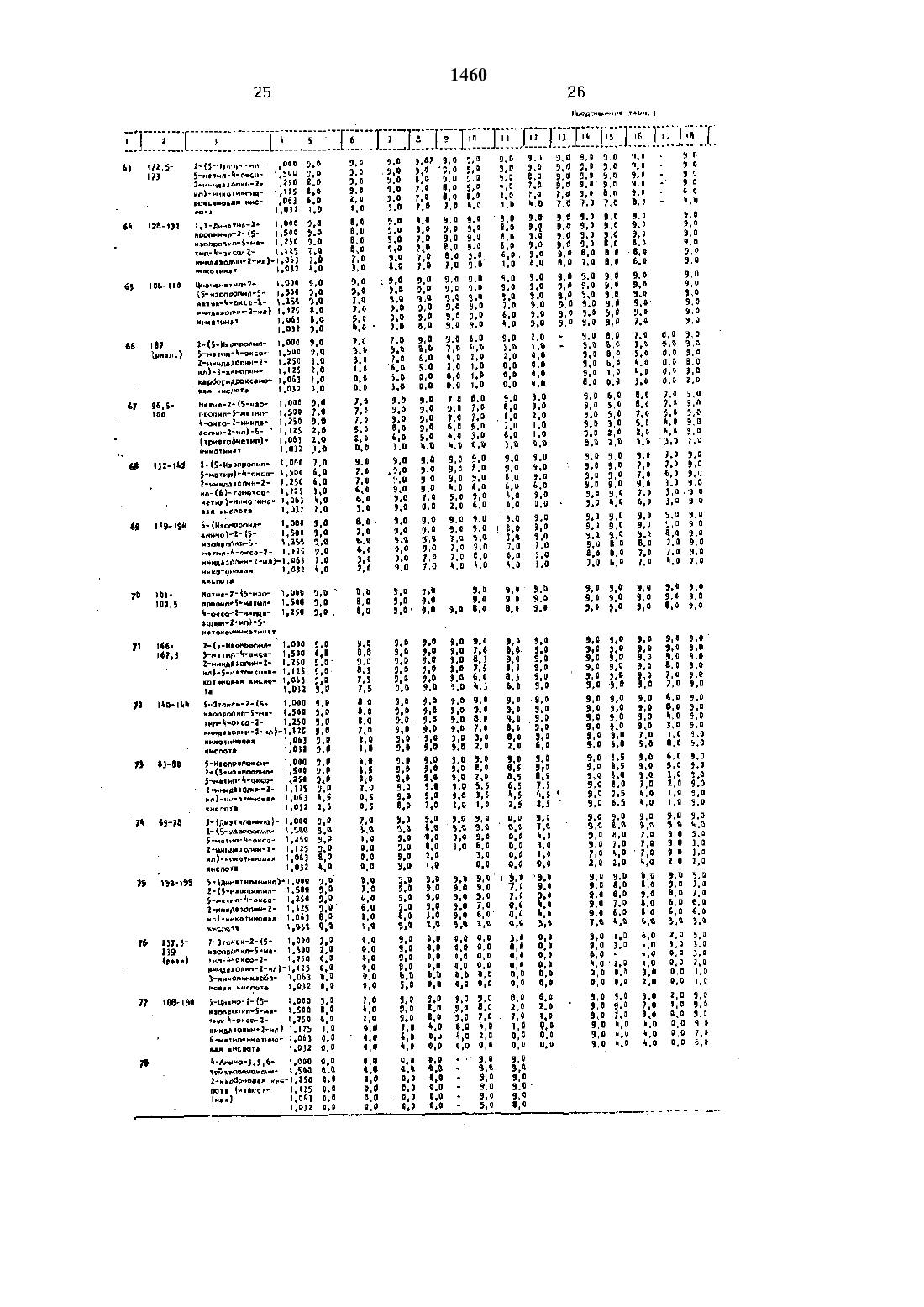
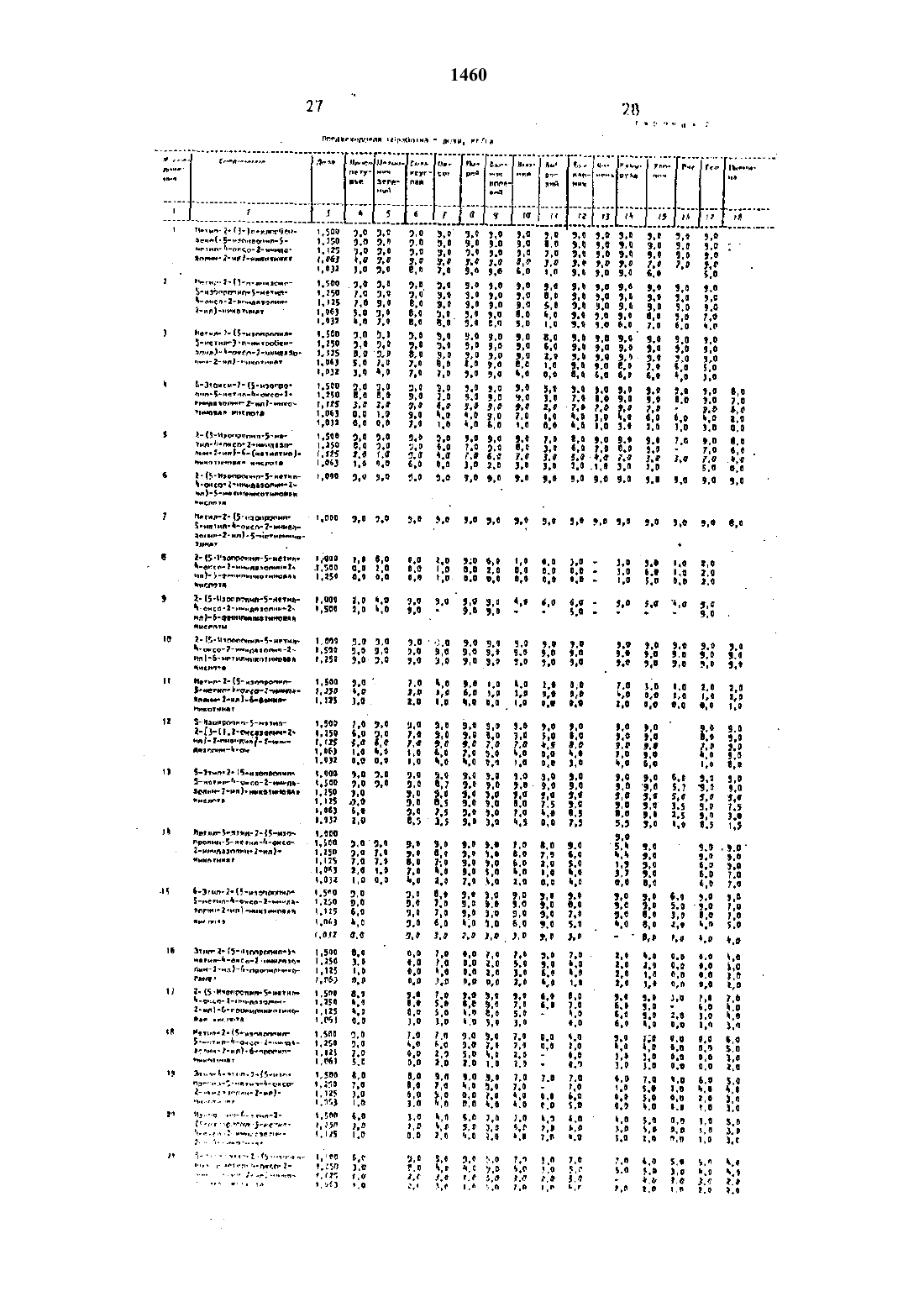
Использование: сельское хозяйство, химические способы защиты растений. Сущность изобретения: растения или почву, на которой произрастают растения, обрабатывают производным пиридина общей формулы (1), где R1 - метил; R2 - этил, изопропил: А - СООR3, СОNНОН, 1,3-оксазолинил-2; R3 - водород, C1-С3 - алкил, цианометил, 2-хлораллил, 2-пропинил, 1,1-диметил-2-пропинил, 2,2,2-трихлорэтил, фурфурил, катион, выбранный из группы натрий, кальций, иэопропиламмоний, диизопропиламмоний. таллоаммоний; В - водород, COR4, где R4 - метил, п-хлорфенил, п-нитрофенил, п-метоксифенил, при условии, что, когда В - COR4, А - СООR3, где R3 отличен от водорода или солеобразующего катиона, W - кислород, Z не является изопропиламиногруппой; W - кислород или сера; Y - водород, С1-С3 - алкил, С1-С3 - алкокси, диметиламино, диэтиламино, фенил, циано; Z - водород, C1-С3 - алкил, этокси, метилтио, трифторметил, изопропиламино, диметиламино, фенил; Y и Z совместно образуют группу -C(L) = С(М) - С(Q) = C(R), где L - водород, бром, метил; М - водород, хлор, бром, фтор; Q - водород.этокси; R - водород, хлор, метокси, при условии, что только один из радикалов L, М, Q или R может представлять собой заместитель, отличный от водорода, галогена или алкокси, и когда W - кислород и А-СООR3 при условии, что R3 не может быть ненасыщенным алкилом, Y не может быть диметиламино, диэтиламино, Z не может быть метилтио, диэтиламино, изопропиламино, в количестве 0,032-1,000 кг/га.
Текст
Указанная цель достигается путем обработки растений и почвы. на которой произрастают растения производным Где 11 т метилпьтридиъта обньей Формулы н тНа водород Ст-Са - алкил. цианометип, 2-хгюраллил. Ъпропинил, 1.1-диметил. 2-пропиттитт. 2.2.2-трихлорэтия фурфуридт. катион. выбранный из группы натрий, кальций. изопропиламмоний. диизопрогпиламмоний. таллоаммоний - ор В водород. (2084. где 524 метил. пхлорфенил. п-нитрофенил. п-метотссифеэгил при условии. что когда В т СОНАА предстаепяетсобой (100523. а котором На отличен от водорода или солеобразуаощего кантона И- кислород 2 не является изопропиламш ногруппой .У и 2 совместно образуют группу Си.) СМ) - С(О СЫЧ. где 1. - водород. бром. РЛЭТИЛПРИ УСЛОВИИ, ЧТО ТОЛЬКО ОДИН ИЗ РНДИКЗЛОВ, м. О или В может представлять собой заместитель. отличный от водорода. галогена или алкокси. и когда ш кислород и А СООН 3 при условии. что На не моэкет быть НЗПВСЫЩВННЫМ НЛКЪЧПОМ, У не МОНСЕТ БЫТЬ диметиламино. диэтиламътлто. 2 не может БЫТЬ МЕЗТИЛТРЬО. ДИМВТИЛБМИНО, ИЗОППОПИП амино. а количестве 0.032 - 1.000 кг/ге.Сложные эфиры 2-(2-имидазолитт-2 игопиридина формулы (1). в которой А СОШЪ, а Ка заместитель, отличный от водорода или сопеобразующего катиона. и Н 1. На. Г и 2 - описаны еыиле могут быть пол УЧЕНЫ ПО РВЗКЦИИ ИМИДЗЗОПИЮВОЛОПЛРИдиндиона с подходящим спьлртоьч. и соответстеупокцим алкипатом щелочного металла при 205 ОСВ этих реакцияд спирт может выполнять роль реагента и растворителя. В этой снту ацни егорищшй гдаьтеоръттелть не требуется.Однако при использовании для реакции дорогостоящего растворителя. я реакцноннуло смесь может быть добавлен менее дорогой вторичный растворитель. например диоксан. тетрагидрофуран или няней апротоягньъй растворитель. Кольъчество апротонного растворителя. добавляемого в реакционную смесь, может колебаться е широких пределах.Сложные ефирьп 22-иь 1 ицаэолин-2 ищпиридина могут быть преимущественно получены также из ацетамида диоксопнрролопиридина его циклизацией сильным основанием, таким как 1.5-диазабицикло(5..5.0)уъьдецч 5-ег 1 (ДБУ). в присутствии инертного органического раствортттепп. например ксилола или толуола, с получением сырого имидазопирротзопиридина формулы(Ш). Реакътиотпл-нупо смесь нагревают до 100 10 С и воду удаляют из реакционной смеси в ходе реакции с применением любых подходящих средств. птапрпичмер еодоотдеттитеп дядина-Старка. Затем к реакционной смеси добавляют минимум один эквивалент спирта. представленного трешь-лупой паон, где Е- член указанной группы. отличный от водорода или солеобразулощего каткюна, и полученную таким путем реакционную смесь нагревают до кипения с обратным колодиттьнътком при при 1 ООШ 1 БОС с получениемЕще один вариант относящийся к поп учению сложных эфиров 2-2-иьчьттдаэотлт-ттгищпиридина формулы 1 основан нациклизации сложного эфира карбамоп-тлацг-п-котиновой кислоты с пятинпористы м сросфором при повышенной теглпегдатуре. как правило при бО 100 С. Реакцию предпочтительно проводят в присутствии инертного органического растворителя. например толуола или бензол/ха. достигается хороший выход хлористооодородной солит-целевого сложного эфира формулы 1. хлористоводородную соль затем легко преобразуют в сложный зфиар срормупы 1 растворением соли присоединения кислоты а воде и нейт рапизацией полученного таким путем рас- теора основанием. например карбонатом натрия или калия.В еще одном варианте получения слезкных эфиров 2-2-имидезолин-2-нлнпттридтинов форт-пулы 1 согласно изобретению проводят циклизацию сложного эфира карбамоилътиконлновой кислоты с использованием смеси пятьтхлортчстого сросфщтгт и оксихпорътдта фосфора. Реакционную гтлесь переметншзают при комнатной температуре на протяжении е -8 ч. после чего РОСЬ удаляют а налаууьтез. Оставил-тиса остаток цис 5пергируют в органическом растворителе. например толуоле. Растворитель отгоняют и остаток диспергирутот в воде и нагревают до ВО-100 С. После охлаждения рН водной смеси доводят до 5-6 бикарбонатом натрия и продукт экстрагируют в метиленклорид с получением целевого сложного эфира 2-2 имидазолин--ищпиридина формулы 1.Сложный эфир З-(Е-имидаэолитч-Зилу-ларидина формулы 1. в которой А СООКз. до алкил С 1-С 3. алкенил Сз-Стг. Ъклорагпгтътл. Ъпропинил, 1.1-диметил-2 пропинил. а У, 2, Щ и К описаны выше. может быть преобразован в соответствующузо гидроксаминовуло кислоту по реакции с гидроксиламнном при повышенном давлении и тенлпературе от 25 до 125 С. Эта реакцнлдложет быть проведена в протонном растворителе. например низшем апканопа. или в апротонгтом растворителе, таком как тетрагидрофуран. диоксан и т.п.Производные М-замепцегнного имидзэогаинона формулы 1. где В СОКа ИБО Пт. Па. На. У и 2 описаны вывле. исключая случай. когда У и 2 являются алкиламино. гпдрокси или гглдрокси - низшеалкилом. могут быть получены по реакции соответственно замешанного 2-(2-иглидазолитт-2 ищпт-тридина избытком ацнлгалогенида. ацилангидрида или сульфонилгалогеъаида как тактооым или в растворителе. например пирндине или толуоле при повышенной температуре от 50 до 125 С.Сложные эфиры формулы 1. в которой В водород. Ш кислород. А 4300513, где На алкил Ст-Сз, т, На, У и 2 определены выше. могут быть получены по реакции соответствующей кислоты. т.е. когда А ССЮН. с полкодягцигт спиртом п присутстоихл каталитического количества сильной минеральной кислоты. такой как хлористоводородная кислота. сериал кислота и т.п при температуре от 50 до 10 ОС. Кислота формулы 1. описанная выше,в которой А - СЕЗОН. В водород. И кислород. а Я н. На. У и 2 определены выше. также легко преобразуется е соответствующии метилоый эфглр по реакции с диазометанпм при температуре от 0 до 25 С. Полученный таким путем ъчегиповый эфир может быть затем введен в реакцию с алкилатом щелочного металла. например алкилатом натрия или калия. для удобства показанным как На Ома, и подходящим спиртом. представленным структурой Н 3 ОН. где По т алкил Сг-Сз, в случае необходимости замощенный фурнлом. -хпораппидом.В еще одном варианте осуществления изобретения. соедипненил фпрмульт 1. в коТОВОГ А т СООЩ и На - водород. а Кт. 82. Уи 2 определены выше. могут быть полущ ны гидрогенолиэом бенэильного эфира имьбензиловый эфир формулы (КУ) растворяюили диспергируют в органическом раство рителе. например низшем-спирте. простои эфире. таком как диоксан. тетрагидрофура и т.п толуоле или ксилоле. Катализатор предпочтительно палладий на угле добав ляют к смеси и смесь нагреают до 2 О 25 С нагретую смесь затем обрабатывают газообразным водородом с получением целевой кислоты. .В альтернативе. кислоты формулы 1. в которой А - СООН. могут быть получены обработкой водного раствора сложного эфира формулы 1 сильным основанием. На практике сложный эфир формулы 1 обычно обрабатывают одним эквивалентом основания в водном растворе и смесь нагревают до 205 ОС. Смесь затем охлаждают и доводят до рН 654.5. предпочтительно рН 7. добавлением сильной минеральной кислоты. Подобнал обработка дает целевую кислоту. Кислоты формулы т, в которой А СООН. В водород. И а кислород. а У. 2. Щ и 22 указаны выше. могут бытнполучены по реакции соответственно замешанного имидазолиноъча с алкиллитием предпочтительно в присутствии инертного растворителя. такого как тетрагидрофуран. в атмосфере азота при температуре от 370 до -80 С. Полученную таким путем смесь затем обрабатывают гексаметилфосфорамидом и двуокисью углерода. предпочтительно. винертном растворителе. например тетра гидрофуране. с получением целевого продукта. Соединения формулы 1. в которых А СООЩ и Е представляет собой солеобразующий катион. такой как Щелочной металл. щелочноземельньпй металл аммоний или алифатический аммоний. а 81122. У и 2 спи саны выше. могут быть получены растворением --ИмидазопиНЦ-ищпчдридигтонойкислоты формулы 1 в продходящем раство рителе с последующей обработкой раствора кислоты одним эквивалентом солеобрааующего катиона. Для получения соединений. в которых солеобраэующим катионом являетсянеоргзническал соль, например. натрий. кальций. кислота формулы 1 может быть растворено или диспергирована в воде или низигем спирте или их смесях. Один эквивалент солеобразупоъцего катиона обычно в внде гидроокиси карбоната. бикарбоната и т.п но предпочтительно в виде гидроокиси.ст-тетвиоавот с раствором кислоты формулы 1. По протестным нескольких глинут. соединение формулы 1. о которой На т неорганический солеобрааутоип-ти катион. как правило вьшадает в осадок и может бьттъ выделено из сътеси либо крильтраттией. либоааоотротнгои дистилл птицей с тлспольаоваттъч ем органического растворителя, например диоксона. .Для поттученил соединения Формулы 1. в которой А т СООЩ. и 83 аммоний или органический аммоний, кислоту формулы П рлстоорлтот или диспергирутот в органическом растворителе. например диоксан. тетрагидрофуран и т.п и смесь обрабатывают одним эквивалентом аммиака или амина ИЛИ ГЩЦПППКПС 11 ТЗТПЭЭПКИЛНАМЕПНДП.На практике спустя несколько минут соль аммония или органического аммония вьтнадтатэт л осатдок и может быть выделена ЛЮБЫМ ИЭВВСТПЫМ МЕТОДОМ. д-ЪЭЧРИМВР гриньтргтпатттттвгл или негтргтфугирооадн-чем. Кроме того. реакциозтнал сгиесъ меняет быть концентрттроватта, остающийся растворитеттоуделен гексансм. а остаток затем высуШОН ДИЕТ ПНДЭЛСНИЯ аГ-ЛАЕЛПЛСПОГ ИЛИ орг-ллаичесттгэлгльлоътиеаой соли формулы 1.Многие на производных 22 тимидазолитт-2 члл)-хинолтлна согласно изобретению могут бьтть полтученьт по тлетодъткатл. описанным выше ллл 242 имидазолътг-т-2-ътл-пътрилиноонк соединении Цторьчулъп 1. Например. слоэкные эфиры 2-(2-тлнтътдозо лин-З-т-ппкиттолнгтклрботговои кислоты фор мулы, где Пз заместт-чтелъ. отличный от водорода или солеобразуъоидего катиона. а Пт. Пэз, 1 М. О. и П описаны еыцте. тлогут быть получлгн-т обработкой диона подходящим стартом и алкилатотл щелочного металла при теглнературе от 20 до 5 ОС. В этих рва кЦИПК. КЕМ Н П ЕНЗНОИЧНЬ 1 Х ПЕЗКЦППХ полученил пиридина) гттормултьт 1. спирт выполняет функцию как реагента. так и растворители. Как таковой вторичный растооритель не гребуетсл. но о случае необходимости он может использоваться. При испольаопат-аии вторичного растворители пргзттпочгитетаьно употребление апротонного растворителя. такого как тетрагидрофуран или диоксин.Сполсные этгн-тры 2-(2-итьттлдазолинк 2 плиттолин-каттботтовои кислоты также могут быть получены из ацетамъчда далоксътпирролохтвттолитта. где Пт, Пи. Д. М. О и П описан ы пыше. их циклизациейт сильным основанием. например 1.5-дп 1 а 3 еб 111.н 4 кпо 5. 4.0)гндегл-5-еттлм (ДВУ) в присутствии инерТНПГО ППГПННЧЕЕСПСОТО ППЦТПППИЧИЕЛЯ. НЭППМмер ксилол или толуол. г гнолучепзтагдт сьцэого имиттааогчирролпхиттопинжтитотта. Реакцион 1460ную смесь нагрепают до ШОЧБОС и полу ОТЛЛЛИЮТ ОТ ЗОЗКЦЕФОЕФРЕОЙ СМПСИ С ПОИМЕННнием водоотделителя дивна-Старка. Затем к реакционнои- смеси добаолятот миникчум один эквивалент спирта НзОН. где Н с вьтше ОПИСЭННЫЙ ЗЗМЕСТЬБТСПЫ НО С ИСКЛЮЧЕНИЕМ водорода и солеобразутощих катионов. и таким путем полученную смесь нагревают до кипения с обратным холодильником при 10 О 150 С с получентлем сложного эфира.Сложные эфиры 2-(2-имида 3 ппитн 4 ищхинолиъткарбоътовои кислоты могут быть также получены цикпизациетй сложного эфира карбамоилхинолинкарбоновой кислоты с помоьцыо ллтихпорь-лстого фосфора при повъштепсиои теьтпературе от 60 до 100 С. Реакцию обычно проводят в присутствии инертного органического растворителя. например толуола или бензола. с получением хлористооодородной соли сложного эфира 2-2 имидааольтнй-итнхинолинкарбоноаой кислоты. Обработка полученной таким обрек зом гантоидооодороднои соли основанием. напрътмер карбонатом натрия или калии. дает тогда сложный эфир 2-(2-имидазолиът-2 таль-напелинкарбгяттовой кислоты.также циклизацией сложных эфиров карба-глоилзинолинкарбоновои ктислоты. циклизации сложного эфира карбамоилхтлъаолтчнкарботлопои кислоты обеслечиаа ется его реагироеанъчем со смесью плтхлористого фосфора и оксихлорида фосфора. Реакционную смесь перемешила ют несколько часов при температуре от 15 до 35 С и РОСГз затем отгоняют а вакууме. Остаток от этой обработки диспергируют е органическом растворителе. ттаоример толуолецзатем растворитель отделяют от результирующей смеси и остаток циспергьъ рутот а воде. нагреваемой до 80 1 О 0 С. После окттаждеьтъля рН водной смеси доводлт до 5-15 добавлением бикарбоната натрия или калия и продукт экстрагирулот в метиленхлортлд с получением сложного эфира 2-(2-иьтьтдааолин-2-ипхинолтлгкарбоиовой кислоты.Хинотлновьпй эфир. в котором Р соответствует приведенным определениям. но с исключен-писем водорода или солеобразую щих катионов. а 17-11. На. . М. О и Н описанывыше. легко преобразуют в соответствующую соль присоединения кислоты по реакцим указанного сложного эфира с минимум одним эквивалентом сильной кислоты. Исполььзуп сильные минеральные кислоты. таь кие как хлористоволороднае кислота.ЛПТЗ. ХОТЯ МОГУТ ППИМВНТЬСН ГНКЖВ И Орга 9пьшеские кислоты На практике оказалось. что реакция протекает наиболее удовлетворительно в присутствии инертного органического растворителя. например эфира. хлороформа. метнленхлорида или их смесей. Сернокнслотньте соли получают как правило по данной методике. но с заменой упомянутых растворителей нтлзтиим алифатическим спиртом.Получение производных 2-(2-имидааолин-Ъижнкиттоттитаа. в которой А - СООН, В водород, И кислород. а Нт, На. 1., М. О и Я имеют приведенные выше определения при условии. что 1., М. С и Н не являются галоген-сом. может быть осуществлено гидрогенолизом бенэилового эфира 2(2-имидаэо лин-2-илкьтнолинкарбот-товой кислоты. Реакция предполагает диспергирование бензилового эфира в органическом растворителе и обработку полученной таким путем реакционной смеси газообразным водородом в присутствии катализатора. такого как палладий или платина на угле-носителе,Гидрогенолиз обычно проводят при температуре от 20 до 50 С.Получение производных 2-2-имидазолин--илрсинотнтна формулы. в которых А СООКа. На - солеобразующий катион. В водород. И - кислород. а Вт, Нз. Е. М, О и Е определены выше. может быть осуществлено растворением кислоты в подходящем растворителе и обработкой полученной твкимлутем смеси минимум одним эквивалентом солеобразутощего катиоъта. Реакция по существу идентична описанной для получения пиридинов формулы 1, в которой А СООНз. а На ч солеобразутощий катион, Следует иметь также в виду. что имидаэолинилкинолинкарбоновые кислоты и их сложные эфиры. представленные формулой Н. в которой В Н. могут быть таутомерными. . Следует также иметь в виду, что когда Н и П представляют собой разные заместители на производных 2-(2-имидазолин-2 илпинолина и имидааопирролохинолиндионах углерод. к которому присоединены Щ и Нг. является асимметрическим центром и продукты а также их промежуточные продукты) существуют р о- и Р-формак, а также сп-формах. тК 20 мл сухого метанола. в котором реагирует 10 г гидрида натрия добавляют 2 г сглеси имидазопиррологзиттътддиное. После перемешивания. продолжаэотътетосч в течение 16 ч. добавляют 0.03 г гтдннотт уксуснойкислотьа для нейтрализации оснопанъттт,раствор кот-щентрьттзуъгзт под вакуумом и остаток хроматографирутот из раствора в эфире на силикагеле. Соединение, вьтходтятттее с более вьзсохкой скоростью (целевой эфир),получают в нескольких фракциях. объединлпот, концентрируют и кристаллнзукэт из ацетонитритта, получал при этом тамидазольтнилникотттттат. имеющий т.пл. 121123 С. Аналитически чистый образец. полученный перекристаллизацией смеси из хлористого метилена с гексаном. имеет т.пл. 12 т 122 С.Смесь 25 г амида и 1 мл ЪЕ-диазабицъткло-(54,О)ундец.-5-ена ШЕЮ в 500 мл ксилола кипятят с обратным холодильником в течение 1 головушкой воды Дина-Старка. Смесь несколько охлаждают, ловушку воды удаляют. добавляют 100 мл безводного метанола и смесь кипятят с обратным холодильником в течение 1 ч. Затем под вакуумом удаляют растворители, продукт выделяют хроматографически так. как описано выцте. и получают 13.65 г продукта. имеющего т.пл. 120-122 С и идентичного продукту. полученному в пригмере 1.Смесь 13.65 г никотината и 9.69 г пятикпористого цтосфора а 110 мл сухого толуола нагревают при перемешивании при 80 С. Через 1.5 ч вязкую смесь охлаждают, фильтруют. твердое соединение промывают зфъъром и сушат. Это хлористоводородная соль целевого продукта.Эту соль растворяют в 60 мл воды раствор нейтрализуют бикарбонатом натрия,результирующий осадок удаляют фильтрованием, промывают водойусушат на воздуке и получают продукт, идег-ттичньтй продукту. полученному по примеру т, Методика В.Смесь 5 г никотината, и 7.1 г плтихлористого фосфора в 40 мл окстаклорттда фосфора перемешивают при комнатной температуре в течение ночи. Йксихтлорид фосфора удаляют под вакуумом. остаток суспендьтруяот в 110 мл толуола и снова концентрирутот. Эту операцию повторяют. К остатку добавляют 40 мл воды, смесь нагревают и кипятят с обратным холодильником в течение 1 ч. После охлаждения смесь экстрагируют клортлстьтм МВТНПВНО-Ъ ЗКСТРЗКТ СУШЭТ. ЕСОНЕДЕЭНТПЪЦПУЮТ и получают 1.05 г цеттового продукта. рН водной фазы. сставитейся после экстракции хлористым метнленоттт. донгтдлг до 5 6 рас
МПК / Метки
МПК: A01N 43/50
Метки: способ, растительностью, борьбы, нежелательной
Код ссылки
<a href="https://kz.patents.su/18-1460-sposob-borby-s-nezhelatelnojj-rastitelnostyu.html" rel="bookmark" title="База патентов Казахстана">Способ борьбы с нежелательной растительностью</a>
Предыдущий патент: Гербицидная композиция
Следующий патент: Способ производства зернового хлеба
Случайный патент: Катионит на основе сополимера глицидилметакрилата и лимонной кислоты