Полиморфные формы рифаксимина и способы их получения
Номер патента: 19433
Опубликовано: 15.09.2010
Авторы: РИГИ, Паоло, ВИСКОМИ, Джузеппе С., БРАГА, Дарио, КАННАТА, Винченцо, РОСИНИ, Гоффредо, КОНФОРТИНИ, Донателла, КАМПАНА, Мануэла
Формула / Реферат
Объектом изобретения являются кристалл-лические полиморфные формы рифаксимина (INN), названные рифаксимин α и рифаксимин β, и низкокристаллическая форма, названная рифак-симин γ, полезные в изготовлении лекарств, содержащих рифаксимин, для перорального и местного применения и полученные посредством способа кристаллизации, при котором осуществ-ляют растворение сырьевого рифаксимина в горячем этиловом спирте и вызывают кристал-лизацию продукта путем добавления воды при определенной температуре и в течение опреде-ленного промежутка времени, после чего осуществ-ляют сушку в контролируемых условиях до тех пор, пока в конечном продукте не будет достигнуто определенное содержание воды.
Текст
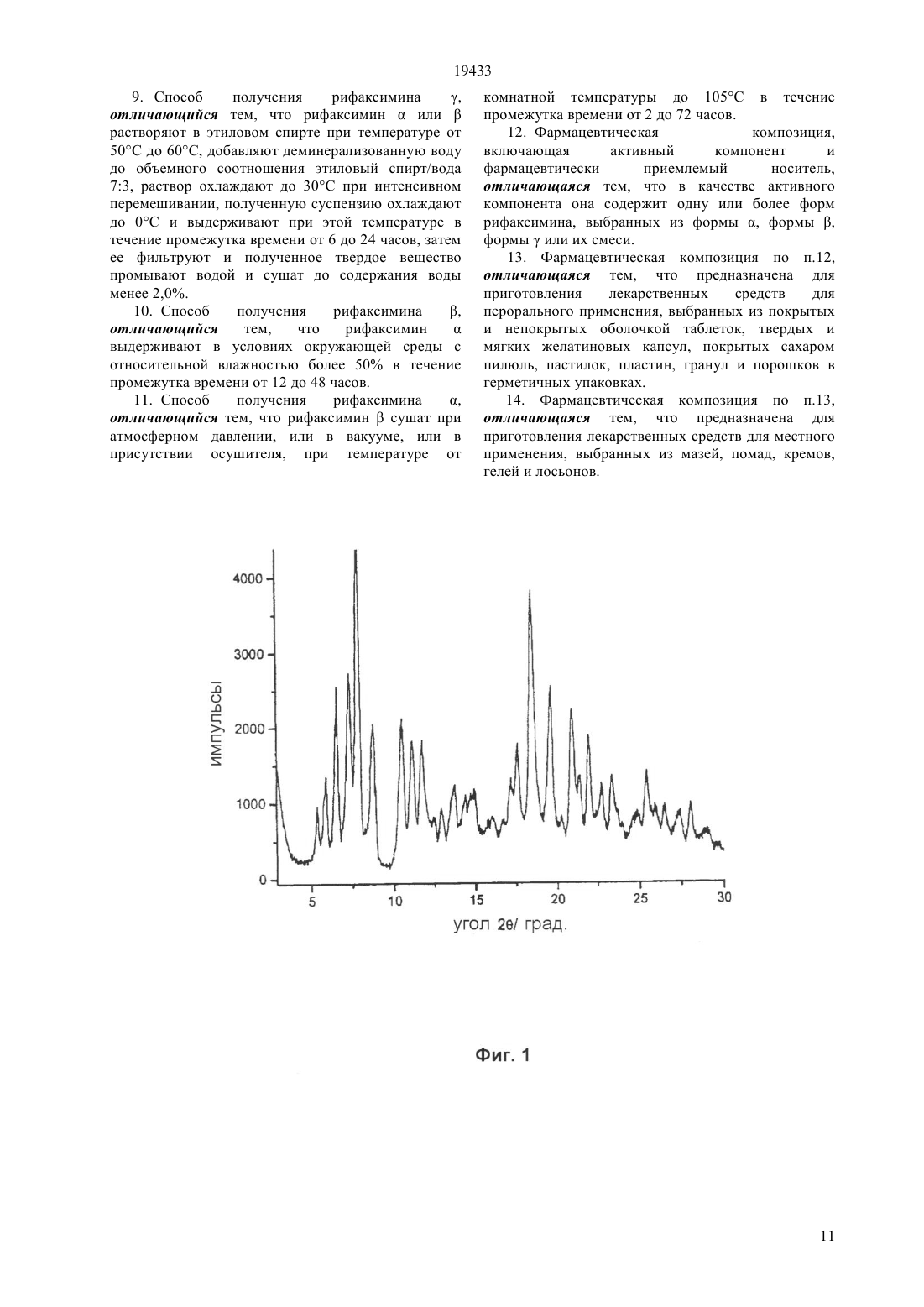
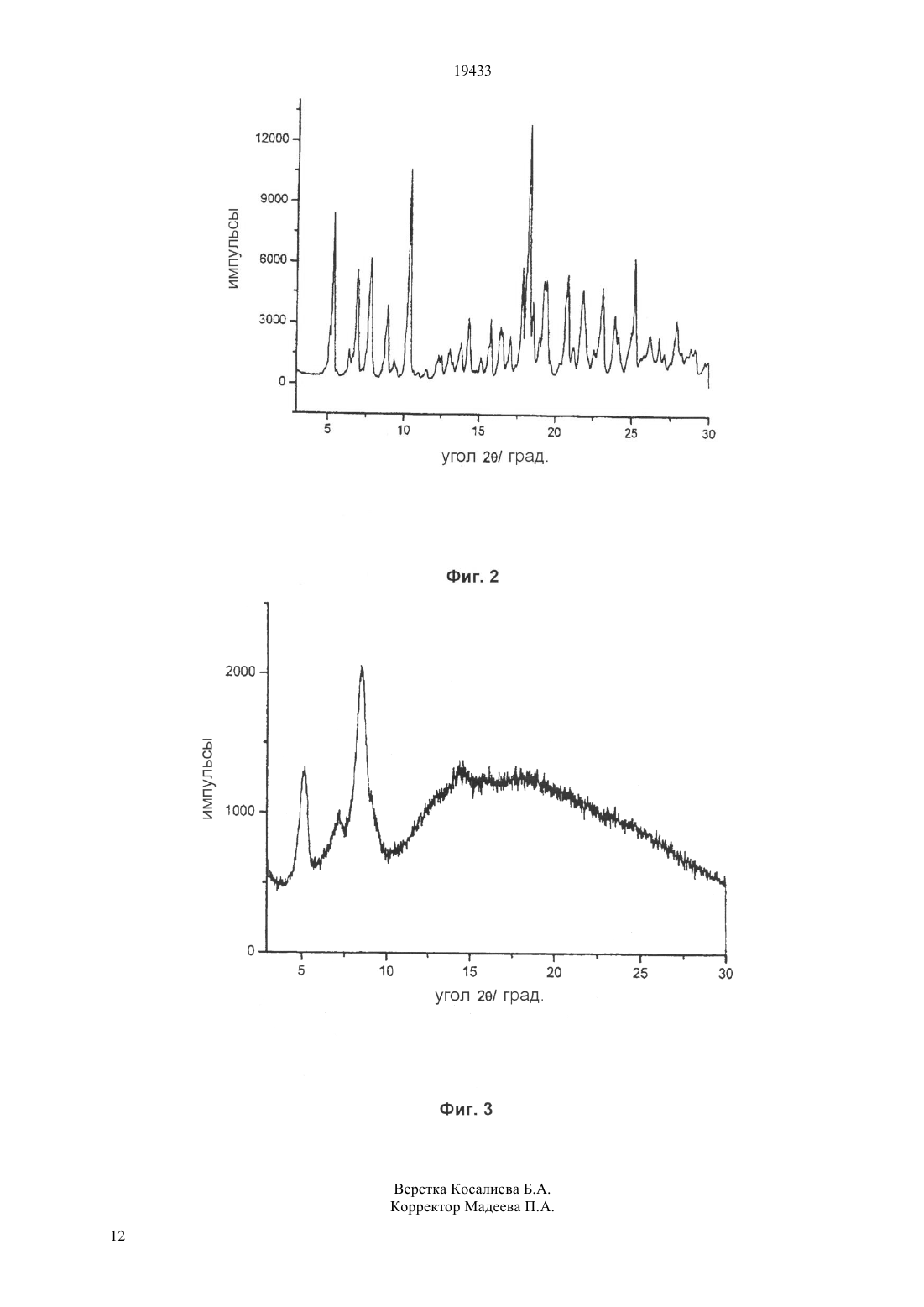
(51) 61 31/395 (2009.01), 61 31/4353 (2009.01), 61 31/00 (2009.01),07 498/22 (2009.01) КОМИТЕТ ПО ПРАВАМ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ МИНИСТЕРСТВА ЮСТИЦИИ РЕСПУБЛИКИ КАЗАХСТАН(54) ПОЛИМОРФНЫЕ ФОРМЫ РИФАКСИМИНА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ(57) Объектом изобретения являются кристаллические полиморфные формы рифаксимина , названные рифаксимини рифаксимин , и низкокристаллическая форма,названная рифаксимин , полезные в изготовлении лекарств,содержащих рифаксимин,для перорального и местного применения и полученные посредством способа кристаллизации, при котором осуществляют растворение сырьевого рифаксимина в горячем этиловом спирте и вызывают кристаллизацию продукта путем добавления воды при определенной температуре и в течение определенного промежутка времени, после чего осуществляют сушку в контролируемых условиях до тех пор, пока в конечном продукте не будет достигнуто определенное содержание воды.(74) Тагбергенова Алма Таишевна Тагбергенова Модангуль Маруповна Касабекова Найля Ертисовна 19433 Настоящее изобретение относится к полиморфным формам рифаксимина ,ик способам их получения и их применению в изготовлении лекарственных препаратов для перорального и местного применения. Рифаксимин(международное непатентованное название) см., ., 8304) представляет собой антибиотик,относящийся к классу рифамицина, а именно пиридо-имидазо-рифамицин, который описан и заявлен в итальянском патенте 1154655, тогда как в ЕР 0161534 описан и заявлен способ его получения из рифамицина О (,., 8301). В обоих этих патентах в общем виде описана очистка рифаксимина путем кристаллизации в подходящих растворителях или системах растворителей, и в нескольких примерах кратко показано, что полученный продукт можно кристаллизовать из смеси этиловый спирт/вода (73) и сушить как при атмосферном давлении, так и в вакууме. Не приведено никакой информации,касающейся экспериментальных условий кристаллизации и сушки, а также каких-либо отличительных кристаллографических характеристик полученного продукта. Наличие различных полиморфов не было установлено, и, следовательно, экспериментальные условия, описанные в обоих патентах, были разработаны с целью получения гомогенного продукта, обладающего подходящей с химической точки зрения чистотой,без учета кристаллографических характеристик самого продукта. В настоящее время неожиданно обнаружено, что существуют несколько полиморфных форм рифаксимина,образование которых зависит от растворителя,а также от временных и температурных условий,при которых осуществляются как кристаллизация, так и сушка. Ниже в настоящей заявке эти полиморфные формы будут называться рифаксимин(фиг. 1) и рифаксимин(фиг. 2) на основе их соответствующих характерных дифрактограмм, в то время как низкокристаллическая форма с высоким содержанием аморфного компонента идентифицирована как рифаксимин(фиг. 3). Полиморфные формы рифаксимина охарактеризованы методом дифракции рентгеновских лучей на порошке. Идентификация и характеристика этих полиморфных форм и, как принято в настоящее время, определение экспериментальных условий их получения очень важны для соединения,обладающего фармакологической активностью,которое, как рифаксимин, поставляется на рынок в качестве медицинского препарата для применения как у людей, так и у животных. Действительно,известно, что полиморфизм соединения, которое может быть использовано в качестве действующего начала, содержащегося в медицинском препарате,может влиять на фармакотоксикологические свойства этого лекарственного средства. Разные 2 полиморфные формы действующего начала,вводимого в качестве лекарственного средства в форме для перорального или местного применения,могут менять многие его свойства, такие как биодоступность, растворимость, стабильность, цвет,прессуемость, текучесть и обрабатываемость с последующим изменением профилей токсикологической безопасности, клинической эффективности и эффективности получения. Все вышесказанное подтверждается тем фактом,что органы, регулирующие разрешения на допуск лекарственных средств на рынок, требуют, чтобы способы получения действующих начал были стандартизованы и контролировались таким образом, чтобы обеспечивать однородные и стабильные результаты в отношении полиморфизма партий продукта (//96, 2003 //367/96 -Дата вступления в силу май 2000 года). Необходимость в вышеуказанной стандартизации дополнительно усилилась в области рифамициновых антибиотиков благодаря(4), 403-408, (2000), которые установили, что различные партии продукта рифампицина ,изготовленные разными производителями,отличаются друг от друга, так как демонстрируют разные полиморфные характеристики, и, как следствие,проявляют различные профили растворения наряду с последующим изменением соответствующих фармакологических свойств. При слежении за процессами кристаллизации и сушки, описанными в общем виде в 1154655 и ЕР 0161534, было обнаружено, что в некоторых экспериментальных условиях получается низкокристаллическая форма рифаксимина, тогда как в других экспериментальных условиях получаются другие кристаллические полиморфные формы рифаксимина. Кроме того, было обнаружено,что некоторые параметры, которые не были описаны в вышеупомянутых патентах, например условия хранения и относительная влажность окружающей среды, оказывают неожиданное влияние на форму полиморфа. Полиморфные формы рифаксимина, являющиеся объектом настоящей заявки, никогда ранее не были обнаружены,и их существование не предполагалось, так как обычно предполагалось, что какой бы не был выбран способ в пределах диапазона описанных условий, независимо от условий, используемых для кристаллизации, сушки и хранения всегда получается единственный гомогенный продукт. В настоящее время было обнаружено, что образование -, - и -форм зависит от присутствия воды в кристаллизационном растворителе, от температуры, при которой продукт кристаллизуется,и от количества воды, присутствующей в продукте в конце стадии сушки. 19433 Форма , формаи формарифаксимина были синтезированы и являются предметом данного изобретения. Кроме того, было обнаружено, что присутствие воды в рифаксимине в твердом состоянии является обратимым, так что со временем может происходить поглощение и/или передача воды при наличии подходящих условий окружающей среды следовательно, рифаксимин подвержен превращению из одной формы в другую, оставаясь в то же время в твердом состоянии, не требуя снова растворения и перекристаллизации. Например, когда полиморфпоглощает гидратную воду до содержания более 4,5, он превращается в полиморф , который в свою очередь превращается в полиморфпри сушке до содержания воды менее 4,5. Эти результаты очень важны, поскольку они определяют условия некоторых стадий промышленного получения, которые ранее не считали критическими для определения полиморфизма продукта,например стадии промывки кристаллического продукта, условия хранения конечного продукта, или характеристики контейнера, в котором хранится продукт. Рифаксимин проявляет широкую антибактериальную активность в желудочнокишечном тракте в отношении локализованных в нем бактерий, включая анаэробные штаммы,вызывающих инфекционную диарею. Сообщалось,что рифаксимин из-за своих химических и физических характеристик характеризуется незначительной системной абсорбцией (.,., 14 (2), 51-56, (1994. Теперь авторы изобретения обнаружили, что уровень системной абсорбции рифаксимина может быть изменен, и это составляет часть настоящего изобретения,путем введения определенных полиморфных форм рифаксимина, а именно рифаксимина , рифаксиминаи рифаксимина . Возможно получить разницу в абсорбции почти в 600 раз, в интервале от 0,001 до 1 м кг/мл. Очевидная разница в биодоступности является важной,поскольку она может отличать фармакологическое и токсикологическое поведение трех полиморфов рифаксимина ,и . Действительно, рифаксимини рифаксиминнезначительно абсорбируются при пероральном применении, в то время как рифаксиминдемонстрирует умеренную абсорбцию. Рифаксиминыи , которые практически не абсорбируются, могут оказывать только местное действие, включая случай желудочно-кишечного тракта, имея в качестве преимущества очень низкую токсичность. С другой стороны, рифаксимин , который умеренно абсорбируется, может найти преимущественное применение в отношении системных микроорганизмов,способных скрываться и частично избегать действия местных антибиотиков. Что касается возможных побочных эффектов,связанных с терапевтическим применением рифаксимина, особенно существенной является индукция у бактерий резистентности к антибиотикам. Вообще говоря, в терапевтической практике применения антибиотиков, резистентность бактерий к тем же или другим антибиотикам может возникать, когда появляются резистентные штаммы. В случае рифаксимина этот аспект является особенно важным, так как рифаксимин принадлежит семейству рифамицина, один член которого,рифампицин, широко используется в лечении туберкулеза. В настоящее время короткий курс лечения туберкулеза представляет собой комбинированную терапию с привлечением четырех активных фармацевтических ингредиентов рифампицина,изониазида,этамбутола и пиразинамида, причем рифампицин играет главную роль. Следовательно,любое лекарственное средство, которое угрожает эффективности терапии путем отбора по резистентности к рифампицину,является неблагоприятным. (1.,. . , 11 (2), 153157, (2002. В принципе, принимая во внимание структурное сходство между рифаксимином и рифампицином,применение рифаксимина может индуцировать отбор резистентных штаммов М.и перекрестной резистентности к рифампицину. Чтобы избежать такого негативного влияния, важно контролировать количество системно абсорбируемого рифаксимина. С этой точки зрения важной является разница между системной абсорбцией -, - и -форм рифаксимина, так как показано, что при концентрациях рифаксимина ниже ингибирующих,например в интервале от 0,1 до 1 мкг/мл, возможен отбор резистентных штаммов (1.,,,- . , 46(4), 253266, (2000. Указанное выше ясно показывает важное значение полиморфных форм рифаксимина по настоящему изобретению и различных способов получения по изобретению для изготовления отдельных чистых форм, обладающих разными фармакологическим свойствами. Вышесказанное ясно подтверждает важность настоящего изобретения, которое обеспечило знание того, что существуют вышеуказанные полиморфные формы рифаксимина и различные способы промышленного получения отдельных чистых форм, обладающих разными фармакологическими свойствами. Вышеуказанные -, - и -формы можно преимущественно использовать в виде чистых и гомогенных продуктов в изготовлении медицинских препаратов, содержащих рифаксимин. Как уже говорилось, способ получения рифаксимина из рифамицина О, описанный и 3 19433 заявленный в ЕР 0161534, несовершенен с точки зрения очистки и идентификации полученного продукта также он имеет некоторые ограничения с точки зрения синтеза, например, из-за очень длительного времени реакции, составляющего от 16 до 72 часов, которое плохо применимо в промышленном применении и, кроме того, из-за того что он не обеспечиваетвосстановление окисленного рифаксимина,который может образовываться в реакционной смеси. Таким образом, еще один объект настоящего изобретения представляет собой улучшенный способ промышленного получения -, - и -форм рифаксимина, заявленных здесь в качестве продуктов и используемых в качестве определенных и гомогенных действующих начал в изготовлении лекарственных препаратов, содержащих такое действующее начало. Настоящее изобретение относится к форме ,формеи формеантибиотика, известного как рифаксимин , к способам их получения и к их применению в изготовлении лекарственных препаратов для перорального или местного применения. Способ по настоящему изобретению включает реакцию одного молярного эквивалента рифамицина О с избытком 2-амино-4-метилпиридина,предпочтительно от 2,0 до 3,5 молярных эквивалентов, в смеси растворителей, состоящей из воды и этилового спирта, в объемных соотношениях от 11 до 21, в течение промежутка времени от 2 до 8 часов, при температуре от 40 С до 60 С. По окончании реакции, реакционную массу охлаждают до комнатной температуры и к ней добавляют раствор аскорбиновой кислоты в смеси воды,этилового спирта и водной концентрированной соляной кислоты при интенсивном перемешивании с целью восстановления небольшого количества окисленного рифаксимина, образующегося в процессе реакции. Наконец, рН доводят до приблизительно 2,0 путем последующего добавления концентрированного водного раствора соляной кислоты, чтобы лучше удалить избыток 2 амино-4-метилпиридина, используемого в данной реакции. Суспензию фильтруют, и полученное твердое вещество промывают той же самой смесью растворителей вода/этиловый спирт, используемой в данной реакции. Такой полуобработанный продукт назван сырьевой рифаксимин. Сырьевой рифаксимин непосредственно может быть подвергнут последующей стадии очистки. Альтернативно,если ожидается,что полуобработанный продукт будет храниться в течение длительного времени, то сырьевой рифаксимин можно высушить в вакууме при температуре менее 65 С в течение промежутка времени от 6 до 24 часов. Такой полуобработанный продукт назван высушенный сырьевой рифаксимин. Полученный сырьевой рифаксимин и/или высушенный сырьевой рифаксимин очищают путем растворения в этиловом спирте при температуре от 45 С до 65 С с последующей кристаллизацией 4 путем добавления воды, предпочтительно в массовом количестве от 15 до 70 от массового количества этилового спирта, используемого для растворения, и выдерживания полученной суспензии при температуре от 50 С до 0 С при перемешивании в течение промежутка времени от 4 до 36 часов. Суспензию фильтруют, и полученное твердое вещество промывают водой и сушат в вакууме или при нормальном давлении, возможно в присутствии осушителя, при температуре от комнатной температуры до 105 С, в течение промежутка времени от 2 до 72 часов. Получение -, - и -форм зависит от условий,выбранных для кристаллизации. В частности, было доказано, что критическими являются состав смеси растворителей, используемой для кристаллизации,температура, при которой реакционную смесь выдерживают после кристаллизации, и промежуток времени, в течение которого данная температура поддерживается. Точнее, рифаксиминполучают, когда раствор доводят до температуры от 28 С до 32 С для того,чтобы началось осаждение, и полученную суспензию затем охлаждают до 0 С и выдерживают при этой температуре в течение промежутка времени от 6 до 24 часов. Суспензию фильтруют, твердое вещество промывают деминерализованной водой и сушат до содержания воды от 1,0 до 2,0. Рифаксиминыиполучают, когда температуру сначала доводят до значения от 28 С до 32 С для того, чтобы началась кристаллизация, затем суспензию доводят до температуры от 40 С до 50 С,и выдерживают при этом значении в течение промежутка времени от 6 до 24 часов, затем суспензию быстро охлаждают до 0 С в течение промежутка времени от 15 минут до одного часа,потом фильтруют, твердое вещество промывают водой и затем сушат. Стадия сушки играет важную роль в получении- и -полиморфных форм рифаксимина, и ее следует контролировать путем использования подходящего метода определения содержания воды,такого как метод Карла Фишера, для того чтобы контролировать количество воды, оставшейся в продукте после сушки. Рифаксиминили рифаксиминполучают путем сушки до разного конечного содержания воды, а именно до содержания более или менее 4,5, они не зависят от экспериментальных условий давления и температуры, при которых достигаются эти критические значения процентного содержания воды. Фактически эти две полиморфные формы с более высоким или более низким содержанием воды могут быть получены путем сушки в вакууме или при атмосферном давлении, при комнатной температуре или при высоких температурах,возможно в присутствии осушителей, при условии что сушка продолжается в течение промежутка времени, необходимого для того, чтобы достичь содержания воды, характерного для каждой полиморфной формы. 19433 Полиморфную формуполучают в том случае,когда сушку выкристаллизованного и промытого водой продукта останавливают при содержании воды более 4,5 при измерении методом Карла Фишера, предпочтительно при содержании воды от 5,0 до 6,0, в то время как полиморфную формуполучают, когда сушка продолжается до тех пор,пока не будет достигнута величина содержания воды менее 4,5, предпочтительно от 2,0 до 3,0. Как форма , так и формыирифаксимина гигроскопичны, они обратимо абсорбируют воду при наличии подходящих условий давления и влажности в окружающей среде, и они подвержены превращению из одной формы в другую. Когда полиморфную формувыдерживают в условиях относительной влажности более 50 в течение промежутка времени от 12 до 48 часов, она превращается в полиморфную форму , которая в свою очередь превращается в полиморфную формупри сушке до содержания воды менее 4,5,предпочтительно от 2,0 до 3,0. Еще один тип превращения происходит между формойи формамиив зависимости от температур, поддерживаемых на стадии осаждения рифаксимина. В частности, формапревращается в формыилипри хранении суспензии формырифаксимина в смеси растворителей этиловый спирт/вода 73 (об./об.) при температуре от 38 С до 50 С при интенсивном перемешивании в течение длительного промежутка времени, предпочтительно составляющего от 6 до 36 часов. После фильтрации и промывки деминерализованной водой, сушки до содержания воды более 4,5, предпочтительно от 5,0 до 6,0,получают полиморфную форму , в то время как при продолжении сушки до содержания воды менее 4,5, предпочтительно от 2,0 до 3,0, получают форму . Рифаксиминыиможно в свою очередь превращать в рифаксиминпутем растворения в этиловом спирте и обработки полученного раствора в соответствии с тем, как было описано ранее для получения формы . Эти превращения из одной формы в другую очень важны для настоящего изобретения,поскольку они могут представлять альтернативный способ получения формы, желательной для изготовления медицинских препаратов. Следовательно, важными составляющими данного изобретения являются способ, позволяющий превращать рифаксиминв рифаксиминилипригодным для промышленности путем, способ,позволяющий превращать рифаксиминилив рифаксиминпригодным для промышленности путем,способ,позволяющий превращать рифаксиминв рифаксимин , или наоборот рифаксиминв рифаксимин , пригодным для промышленности путем. Способ,относящийся к превращению рифаксиминав рифаксиминили рифаксиминвключает суспендирование рифаксиминав смеси растворителей, состоящей из этилового спирта/воды в объемном соотношении 73, нагревание суспензии до температуры от 38 С до 50 С и выдерживание ее при этой температуре при интенсивном перемешивании в течение промежутка времени от 6 до 36 часов. Суспензию затем фильтруют, твердое вещество промывают водой и сушат полиморфную формуполучают, когда сушку осуществляют до содержания воды от 5,0 до 6,0 при измерении методом Карла Фишера, в то время как полиморфную формуполучают, когда сушку продолжают до содержания воды от 2,0 до 3,0. Способ получения формыиз рифаксиминаиливключает растворение - или -формы в этиловом спирте при перемешивании при температуре от 50 С до 60 С, добавление деминерализованной воды до объемного соотношения этиловый спирт/вода 73, охлаждение раствора до 30 С при интенсивном перемешивании, охлаждение осадка до 0 С, и выдерживание суспензии при перемешивании при 0 С в течение промежутка времени от 6 до 24 часов. Суспензию затем фильтруют, твердое вещество промывают водой и сушат до содержания воды менее 2,0, получая,таким образом, рифаксимин . Способ превращения формыв формусостоит в выдерживании порошка рифаксиминав условиях окружающей среды с относительной влажностью более 50 в течение промежутка времени, необходимого для получения содержания воды в порошке более 4,5, это время, как правило,составляет от 12 до 48 часов. Способ превращения формыв формусостоит в сушке порошка рифаксиминав вакууме или в условиях нормального давления, возможно в присутствии осушителя, при температуре в интервале от комнатной температуры до 105 С, в течение промежутка времени от 2 до 72 часов, для достижения содержания воды в порошке менее 4,5, предпочтительно от 2,0 до 3,0. Из приведенного выше обсуждения понятно, что в процессе хранения продукта следует особенно позаботится о том, чтобы условия окружающей среды не влияли на содержания воды в продукте,путем хранения продукта в условиях окружающей среды с контролируемой влажностью или в закрытых контейнерах, которые не допускают существенного обмена водой с внешней окружающей средой.-Полиморф рифаксимина характеризуется содержанием воды ниже 4,5, предпочтительно от 2,0 до 3,0, и дифрактограммой рентгеновских лучей на порошке (показанной на фиг. 1), которая демонстрирует пики при величинах углов дифракции 2 6,6 7,4 7,9 8,8 10,5 11,1 11,8 12,9 17,6 18,5 19,7 21,0 21,4 22,1. Полиморф рифаксимина характеризуется содержанием воды более 4,5, предпочтительно от 5,0 до 6,0, и дифрактограммой рентгеновских лучей на порошке (показанной на фиг. 2), которая демонстрирует пики при величинах углов дифракции 2 5,4 6,4 7,0 7,8 9,0 10,4 13,1 14,4 17,1 17,9 18,3 20,9. 5-Полиморф рифаксимина характеризуется гораздо более скудной дифрактограммой рентгеновских лучей на порошке из-за низкой кристалличности значительные пики наблюдаются при величинах углов дифракции 2 5,0 7,1 8,4,как показано на фиг. 3. Дифрактограммы были получены с использованием приборас геометрией Брэгга-Брентано (-) и следующими условиями работы Рентгеновская трубка Медная Используемое излучение К (1), К (2) Напряжение и сила тока генератора 40 кВ, 40 мА. Монохроматор Графитовый Размер шага 0,02 Время шага 1,25 секунд Начальная и конечная угловая величина 2 3,030,0. Оценку содержания воды в анализируемых образцах всегда осуществляли методом Карла Фишера. Рифаксимин , рифаксимини рифаксиминтакже значительно отличаются друг от друга по биодоступности и характеристическому растворению. Исследование биодоступности трех полиморфов проводили на собаках породы бигль, при этом им перорально давали дозу 100 мг/кг одного из полиморфов, собирали образцы крови из яремной вены каждого животного перед каждым приемом дозы и через 1, 2, 4, 6, 8 и 24 часа после каждого приема дозы переносили эти образцы в пробирки,содержащие гепарин,и отделяли плазму центрифугированием. Плазму анализировали на рифаксимин достоверным методом -/ (жидкостная хроматография-масс-спектрометрия/массспектрометрия) и наблюдали максимальную концентрацию в плазме (Сах), рассчитываливремя достижения (Сах), и площадь под кривой зависимости концентрации от времени . Экспериментальные данные, приведенные в следующей ниже таблице 1, ясно показывают, что рифаксимини рифаксиминабсорбируются незначительно, в то время как рифаксиминабсорбируется со значением (Сах 0,668 мкг/мл),попадающим в интервал от 0,1 до 1 мкг/мл. Таблица 1 Фармакокинетические параметры полиморфных форм рифаксимина после однократного перорального введения собакам в количестве 100 мг/кг посредством капсул. Испытания характеристического растворения проводили с каждым из трех полиморфов в соответствии с методом, описанном в монографии 1087 на страницах 2512-2513(Фармакопеи США) 27, и ясно показали значительные различия между рифаксимином , рифаксиминоми рифаксимином . Образец каждого из полиморфов рифаксимина помещали в матрицу и прессовали силой 5 тонн посредством штампа гидравлического пресса с получением прессованной таблетки. Держатель матрицы, содержащей прессованную таблетку, затем устанавливали на лабораторное перемешивающие устройство, погружали в среду для растворения и вращали при помощи перемешивающего устройства. Испытание, проводимое в среде для растворения,приготовленной из водного фосфатного буфера рН 7,4 и лаурилсульфата натрия, при температуре 370,5 С продемонстрировало значительные различия между скоростями характеристического растворения, демонстрируемыми тремя полиморфами. Рифаксиминпродемонстрировал распадаемость прессованной таблетки в пределах 10 минут,так что было невозможно рассчитать значение его характеристического растворения, в то время как 6 характеристическое растворение рифаксиминабыло приблизительно в десять раз больше, чем у рифаксимина,в соответствии с его биодоступностью, которая более чем в 100 раз выше чем у рифаксимина . Приведенные выше результаты экспериментов дополнительно указывают на различия,существующие между этими тремя полиморфами. Формы ,имогут быть преимущественно использованы в изготовлении медицинских препаратов, обладающих антибиотической активностью и содержащих рифаксимин, как для перорального, так и для местного применения. Медицинские препараты для перорального применения содержат рифаксиминили , иливместе с обычными эксципиентами, например разбавителями, такими как маннит, лактоза и сорбит связывающими агентами, такими как крахмалы, желатины, сахара,производные целлюлозы, природные смолы и поливинилпирролидон смазывающими агентами,такими как тальк, стеараты, гидрированные растительные масла, полиэтиленгликоль и коллоидный диоксид кремния разрыхлителями, такими как крахмалы, целлюлозы, альгинаты, смолы и сшитые полимеры красителями, корригентами и подсластителями. 19433 Настоящее изобретение относится ко всем твердым препаратам, которые можно вводить пероральным путем, например к таблеткам,покрытым и непокрытым оболочкой, мягким и твердым желатиновым капсулам,пилюлям,покрытым сахаром, пастилкам, пластинам, гранулам и порошкам в герметично закрытых упаковках. Медицинские препараты для местного применения содержат рифаксимин , или , иливместе с обычными эксципиентами, такими как белый вазелин, белый воск, ланолин и его производные, стеариловый спирт, пропиленгликоль,лаурилсульфат натрия, простые эфиры жирных полиоксиэтиленовых спиртов, сложные эфиры жирных полиоксиэтиленовых кислот, сорбитанмоностеарат, глицерилмоностеарат, пропиленгликоля моностеарат, полиэтиленгликоли, метилцеллюлоза,гидроксиметилпропилцеллюлоза, натрий-карбоксиметилцеллюлоза, коллоидный силикат алюминия и магния, альгинат натрия. Настоящее изобретение относится ко всем препаратам для местного применения, например мазям, помадам, кремам, гелям и лосьонам. Данное изобретение ниже проиллюстрировано некоторыми примерами. Эти примеры не следует рассматривать в качестве ограничивающих данное изобретение, действительно очевидно, что формы , имогут быть получены путем подходящего объединения упомянутых выше условий кристаллизации и сушки. Пример 1 Получение сырьевого рифаксимина и высушенного сырьевого рифаксимина В трехгорлую колбу,оборудованную механической мешалкой, термометром и обратным холодильником, последовательно при комнатной температуре загружают 120 мл деминерализованной воды, 96 мл этилового спирта, 63,5 г рифамицина О и 27,2 г 2-амино-4-метилпиридина. После загрузки массу нагревают при 473 С и оставляют перемешиваться при этой температуре в течение 5 часов, затем охлаждают до 203 С, и в течение 30 минут добавляют отдельно приготовленную смесь,состоящую из 9 мл деминерализованной воды, 12,6 мл этилового спирта, 1,68 г аскорбиновой кислоты и 9,28 г водной концентрированной соляной кислоты. По окончании добавления массу оставляют перемешиваться в течение 30 минут при внутренней температуре 203 С и затем, поддерживая указанную температуру, по каплям добавляют 7,72 г концентрированной соляной кислоты до получения рН 2,0. По окончании добавления массу оставляют перемешиваться в течение 30 минут, поддерживая внутреннюю температуру 20 С, затем осадок отфильтровывают и промывают смесью из 32 мл деминерализованной воды и 25 мл этилового спирта. Полученный сырьевой рифаксимин(89,2 г) сушат в вакууме при комнатной температуре в течение 12 часов, получая 64,4 г высушенного сырьевого рифаксимина,демонстрирующего содержание воды, равное 5,6, и дифрактограмму,соответствующую полиморфной форме . Продукт дополнительно сушат в вакууме до постоянной массы с получением 62,2 г высушенного сырьевого рифаксимина, имеющего содержание воды, равное 2,2, дифрактограмма которого соответствует полиморфной форме . Продукт является гигроскопичным, и полученная полиморфная форма является обратимой полиморфная формаабсорбирует воду из атмосферы в зависимости от относительной влажности и времени экспозиции. Когда содержание воды, абсорбированной полиморфной формой ,становится больше 4,5, полиморфная формапревращается в полиморфную форму . Она, в свою очередь, теряет часть воды при сушке, превращаясь в полиморфную форму , когда достигается содержание воды от 2,0 до 3,0. Пример 2 Получение рифаксимина 163 мл этилового спирта и 62,2 г высушенного сырьевого рифаксимина загружают при комнатной температуре в трехгорлую колбу, оборудованную механической мешалкой, термометром и обратным холодильником. Суспензию нагревают при 573 С при перемешивании до полного растворения твердого вещества, и при этой температуре за 30 минут добавляют 70 мл деминерализованной воды. После окончания добавления температуру доводят до 30 С в течение 40 минут, и выдерживают при этом значении до завершения кристаллизации, затем температуру дополнительно снижают до 0 С в течение 2 часов и выдерживают при этом значении в течение 6 часов. Суспензию затем фильтруют, и твердое вещество промывают 180 г деминерализованной воды и сушат в вакууме при комнатной температуре до постоянной массы, получая таким образом 52,7 г чистого рифаксиминас содержанием воды 1,5. Формахарактеризуется дифрактограммой рентгеновских лучей на порошке,демонстрирующей значительные пики при величинах углов дифракции 2 5,0 7,1 8,4. Пример 3 Получение рифаксимина 62,2 грамма высушенного сырьевого рифаксимина и 163 мл этилового спирта загружают при комнатной температуре в трехгорлую колбу,оборудованную механической мешалкой,термометром и обратным холодильником. Суспензию нагревают при 573 С до полного растворения твердого вещества, и затем при этой температуре в течение 30 минут добавляют 70 мл деминерализованной воды. После окончания добавления температуру доводят до 30 С в течение 40 минут, и выдерживают при этом значении до обильной кристаллизации. Температуру суспензии затем доводят до приблизительно 40 С и выдерживают при этой температуре в течение 20 часов при перемешивании затем температуру снижают до 0 С в течение 30 минут и суспензию немедленно фильтруют. Твердое вещество промывают 180 мл деминерализованной воды и сушат в вакууме при комнатной температуре до постоянной массы, получая, таким образом, 51,9 г 7 19433 формы рифаксимина с содержанием воды, равным 2,5,и рентгеновскую порошковую дифрактограмму, демонстрирующую пики при величинах углов дифракции 2 6,6 7,4 7,9 8,8 10,5 11,1 11,8 12,9 17,6 18,5 19,7 21,0 21,4 22,1. Пример 4 Получение рифаксимина 89,2 грамма сырьевого рифаксимина и 170 мл этилового спирта загружают при комнатной температуре в трехгорлую колбу, оборудованную механической мешалкой, термометром и обратным холодильником, затем суспензию нагревают при 573 С до полного растворения твердого вещества. Температуру доводят до 50 С и при этой температуре в течение 30 минут добавляют 51,7 мл деминерализованной воды. После окончания добавления температуру доводят до 30 С в течение одного часа, и суспензию выдерживают при этой температуре на 30 минут, получая обильную кристаллизацию. Температуру суспензии доводят до 40 С и оставляют перемешиваться при этой температуре в течение 20 часов, а затем температуру снижают до 0 С в течение 30 минут, после чего суспензию немедленно фильтруют. Твердое вещество промывают 240 мл деминерализованной воды и сушат в вакууме при 65 С до постоянной массы, получая 46,7 г рифаксиминас содержанием воды, равным 2,5. Пример 5 Получение рифаксиминаПример 3 повторяют, но увеличивают до 50 С температуру, при которой выдерживают суспензию,и уменьшают до 7 часов время, в течение которого суспензию выдерживают при этой температуре. Продукт соответствует продукту Примера 3. Пример 6 Получение рифаксиминаКристаллизацию высушенного сырьевого рифаксимина осуществляют в соответствии со способом, описанным в Примере 3. Сушку в вакууме при комнатной температуре контролируют с использованием метода Карла Фишера и останавливают, когда содержание воды достигает 5,0 получают 52,6 г рифаксимина,характеризующегося дифрактограммой рентгеновских лучей на порошке, демонстрирующей пики при величинах углов 2 5,4 6,4 7,0 7,8 9,0 10,4 13,1 14,4 17,1 17,9 18,3 20,9. Пример 7 Получение рифаксиминаиз рифаксимина 5 грамм рифаксиминасуспендируют в смеси,состоящей из 13 мл этилового спирта и 5,6 мл воды,и суспензию нагревают при 40 С в течение 24 часов при перемешивании в 50 мл колбе, оборудованной обратным холодильником,термометром и механической мешалкой. Суспензию затем фильтруют, и твердое вещество промывают водой,затем сушат в вакууме при комнатной температуре до постоянной массы. Получают 4 грамма рифаксимина, демонстрирующего дифрактограмму рентгеновских лучей на порошке, соответствующую 8 дифрактограмме полиморфной формы , и содержание воды 2,6. Пример 8 Получение рифаксиминаиз рифаксимина 15 грамм -формы рифаксимина и 52,4 мл этилового спирта загружают трехгорлую колбу на 250 мл, оборудованную обратным холодильником,термометром и механической мешалкой суспензию нагревают при перемешивании при температуре 50 С до полного растворения твердого вещества. В прозрачный раствор в течение 30 минут при перемешивании добавляют 22,5 мл воды,охлаждают до 30 С и выдерживают при этой температуре в течение 30 минут. Образующуюся суспензию охлаждают до 0 С при интенсивном перемешивании и выдерживают при этой температуре в течение 6 часов. После этого часть суспензии отбирают, фильтруют, промывают деминерализованной водой и сушат в вакууме при 30 С до постоянной массы. Полученный продукт, 3,7 г, демонстрирует дифрактограмму, соответствующую дифрактограмме формы , и содержание воды 1,7. Оставшуюся часть суспензии выдерживают при 0 С в течение еще 18 часов при интенсивном перемешивании и затем фильтруют, промывают деминерализованной водой и сушат при 30 С в вакууме до постоянной массы. Получают 9 грамм продукта, который демонстрирует дифрактограмму,соответствующую дифрактограмме формы , и содержание воды, равное 1,6. Пример 9 Получение рифаксиминаиз рифаксимина 5 грамм рифаксиминас содержанием воды 5,0 сушат в вакууме при 30 С в течение 8 часов,получая 4,85 г рифаксиминас содержанием воды 2,3. Пример 10 Получение рифаксиминаиз рифаксимина 5 грамм рифаксиминас содержанием воды 2,5 выдерживают в течение 40 часов в атмосфере с относительной влажностью 56, созданной с помощью насыщенного водного раствора тетрагидрата нитрата кальция. По окончании этого времени получают 5,17 грамм рифаксиминас содержанием воды 5,9. Пример 11 Биодоступность при пероральном введении собакам Двенадцать чистокровных собак породы бигль в возрасте 12 недель и с массой от 5,0 до 7,5 кг делили на три группы по четыре особи. Первую из этих трех групп обрабатывали рифаксимином , вторую - рифаксимином , и третью - рифаксиминомв соответствии со следующей методикой. Каждая собака получала перорально 100 мг/кг одной из полиморфных форм рифаксимина в желатиновых капсулах, и из яремной вены каждого животного отбирали образцы крови объемом 2 мл перед каждым введением и через 1, 2, 4, 6, 8 и 24 часа после введения. Каждый образец переносили в гепаринизированную пробирку и 19433 центрифугировали плазму делили на две аликвоты по 500 мкл и замораживали при -20 С. Рифаксимин, содержащийся в плазме, оценивали посредством достоверного метода -/ и в соответствии со стандартным некомпартаментальным анализом рассчитывали следующие параметры Сахмаксимальную концентрацию рифаксимина, наблюдаемую в плазме Тахвремя достижения Сахплощадь под кривой зависимости концентрации от времени, рассчитанную по линейной формуле трапеций. Результаты, приведенные в таблице 1, ясно показывают, что рифаксиминабсорбируется значительно, более чем в 102 раз, в сравнении с рифаксиминоми рифаксимином , которые практически не абсорбируются. Пример 12 Испытание на характеристическое растворение Образец массой 100 мг каждого полиморфа рифаксимина подвергали испытанию на характеристическое растворение, проводимому как описано в монографии 1087 на страницах 2512-2513(Фармакопеи США) 27. 100 мг полиморфа рифаксимина помещали в матрицу и прессовали в течение 1 минуты под давлением 5 тонн посредством штампа в гидравлическом прессе. В матрице образовывалась компактная таблетка,у которой одна сторона с определенной площадью на дне матрицы оставалась незащищенной, так что от 50 до 75 прессованной таблетки могло раствориться в подходящей для растворения среде. Держатель,удерживающий матрицу,устанавливали на лабораторное перемешивающие устройство, погружали в стеклянный сосуд,содержащий среду для растворения и вращали со скоростью 100 об/мин при помощи перемешивающего устройства,поддерживая температуру среды для растворения 370,5 С. Среда для растворения, содержащаяся в стеклянном сосуде, состояла из 1000 мл 0,1 М водного фосфатного буфера, рН 7,4, содержащего 4,5 г лаурилсульфата натрия, и ее поддерживали при 370,5 С на всем протяжении испытания. Образцы раствора объемом 2 мл отбирали через 15, 30, 45 и 60 минут от начала процедуры растворения и количество растворенного рифаксимина анализировали посредством ВЭЖХ. Образец,содержащий рифаксимин,систематически демонстрировал распадаемость прессованной таблетки в пределах 10 минут, и это явление также наблюдалось при более низких концентрациях (0,1 и 0,3) лаурилсульфата натрия и даже в отсутствие указанного поверхностно-активного вещества,так что невозможно было рассчитать значение его характеристического растворения. Характеристическое растворение рифаксиминакаждый раз было приблизительно в десять раз больше, чем для рифаксимина , как это можно заключить из экспериментальных результатов,представленных в следующей таблице 2. Таблица 2(мг/мин/см 2) ФОРМУЛА ИЗОБРЕТЕНИЯ 1.Полиморф рифаксимина,характеризующийся содержанием воды менее 4,5,предпочтительно составляющим от 2,0 до 3,0, и дифрактограммой рентгеновских лучей на порошке,демонстрирующей пики при величинах углов дифракции 2 6,6, 7,4, 7,9, 8,8, 10,5, 11,1, 11,8,12,9, 17,6, 18,5, 19,7, 21,0, 21,4 22,1. 2.Полиморф рифаксимина,характеризующийся содержанием воды более 4,5,предпочтительно составляющим от 5,0 до 6,0, и дифрактограммой рентгеновских лучей на порошке,демонстрирующей пики при величинах углов дифракции 2 5,4, 6,4, 7,0, 7,8, 9,0, 10,4, 13,1,14,4, 17,1, 17,9, 18,3, 20,9. Растворенный рифаксимин (мг/см 2) полиморфполиморф 0,28 2,46 0,50 4,52 0,72 6,44 0,94 9,04 0,0147 0,1444 3.Полиморф рифаксимина,характеризующийся содержанием воды,составляющим от 1,0 до 2,0, и дифрактограммой рентгеновских лучей на порошке,демонстрирующей в основном аморфный профиль и несколько значительных пиков при величинах углов дифракции 2 5,0, 7,1, 8,4. 4. Способ получения рифаксимина,включающий взаимодействие молярного эквивалента рифамицина О с избытком 2-амино-4 метилпиридина, предпочтительно от 2,0 до 3,5 молярных эквивалентов, в смеси растворителей,состоящей из воды и этилового спирта в объемном соотношении от 11 до 21, в течение промежутка времени от 2 до 8 часов при температуре от 40 С до 60 С обработку реакционной смеси при комнатной 9 19433 температуре раствором аскорбиновой кислоты в смеси воды, этилового спирта и концентрированной водной соляной кислоты, затем доведение концентрированным водным раствором соляной кислоты до рН 2,0, фильтрование суспензии,промывание полученного твердого вещества той же смесью растворителей вода/этиловый спирт,которую использовали в предыдущей реакции,очистку полученного сырьевого рифаксимина путем растворения в этиловом спирте при температуре от 45 С до 65 С осаждение путем добавления воды,предпочтительно в количестве от 15 до 70 по массе от массового количества этилового спирта,использованного для растворения снижение температуры до значения между 28 С и 32 С для того,чтобы началась кристаллизация,выдерживание полученной в результате суспензии при температуре от 40 С до 50 С при перемешивании в течение промежутка времени от 6 до 24 часов, охлаждение до 0 С в течение промежутка времени от 15 минут до одного часа,затем фильтрование суспензии, промывание водой и сушку полученного в результате твердого вещества в вакууме или в условиях нормального давления,возможно в присутствии осушителя,при температуре от комнатной температуры до 105 С в течение промежутка времени от 2 до 72 часов до содержания воды менее 4,5, предпочтительно от 2,0 до 3,0. 5. Способ получения рифаксимина,включающий взаимодействие молярного эквивалента рифамицина О с избытком 2-амино-4 метилпиридина, предпочтительно от 2,0 до 3,5 молярных эквивалентов, в смеси растворителей,состоящей из воды и этилового спирта в объемном соотношении от 11 до 21, в течение промежутка времени от 2 до 8 часов при температуре от 40 С до 60 С обработку реакционной смеси при комнатной температуре раствором аскорбиновой кислоты в смеси воды, этилового спирта и концентрированной водной соляной кислоты, затем доведение концентрированным водным раствором соляной кислоты до рН 2,0, фильтрование суспензии,промывание полученного твердого вещества той же смесью растворителей вода/этиловый спирт,которую использовали в предыдущей реакции,очистку полученного сырьевого рифаксимина путем растворения в этиловом спирте при температуре от 45 С до 65 С осаждение путем добавления воды,предпочтительно в количестве от 15 до 70 по массе от массового количества этилового спирта,использованного для растворения снижение температуры до значения между 28 С и 32 С для того,чтобы началась кристаллизация,выдерживание полученной в результате суспензии при температуре от 40 С до 50 С при перемешивании в течение промежутка времени от 6 до 24 часов, охлаждение до 0 С в течение промежутка времени от 15 минут до одного часа,затем фильтрование суспензии, промывание водой и сушку полученного в результате твердого вещества в вакууме или в условиях нормального давления,возможно в присутствии осушителя,при 10 температуре от комнатной температуры до 105 С в течение промежутка времени от 2 до 72 часов до содержания воды более 4,5, предпочтительно от 5,0 до 6,0. 6. Способ получения рифаксимина,включающий взаимодействие молярного эквивалента рифамицина О с избытком 2-амино-4 метилпиридина, предпочтительно от 2,0 до 3,5 молярных эквивалентов, в смеси растворителей,состоящей из воды и этилового спирта в объемном соотношении от 11 до 21, в течение промежутка времени от 2 до 8 часов при температуре от 40 С до 60 С обработку реакционной смеси при комнатной температуре раствором аскорбиновой кислоты в смеси воды, этилового спирта и концентрированной водной соляной кислоты, затем доведение концентрированным водным раствором соляной кислоты до рН 2,0, фильтрование суспензии,промывание полученного твердого вещества той же смесью растворителей вода/этиловый спирт,которую использовали в предыдущей реакции,очистку полученного сырьевого рифаксимина путем растворения в этиловом спирте при температуре от 45 С до 65 С осаждение путем добавления воды,предпочтительно в количестве от 15 до 70 по массе от массового количества этилового спирта,использованного для растворения снижение температуры до значения между 28 С и 32 С для того,чтобы началась кристаллизация,выдерживание полученной в результате суспензии при температуре от 40 С до 50 С при перемешивании в течение промежутка времени от 6 до 24 часов, охлаждение до 0 С в течение промежутка времени от 15 минут до одного часа,затем фильтрование суспензии, промывание водой и сушку полученного в результате твердого вещества в вакууме или в условиях нормального давления,возможно в присутствии осушителя,при температуре от комнатной температуры до 105 С в течение промежутка времени от 2 до 72 часов до содержания воды от 1,0 до 2,0. 7. Способ получения рифаксимина суспендируют в смеси растворителей, состоящей из этилового спирта/воды, взятых в объемном соотношении 73, суспензию нагревают до температуры от 38 С до 50 С и выдерживают при этой температуре при перемешивании в течение промежутка времени от 6 до 36 часов, суспензию фильтруют,полученное твердое вещество промывают водой и сушат до содержания воды менее 4,5, предпочтительно от 2,0 до 3,0. 8. Способ получения рифаксимина суспендируют в смеси растворителей, состоящей из этилового спирта/воды в объемном соотношении 73, суспензию нагревают до температуры от 38 С до 50 С и выдерживают при этой температуре при перемешивании в течение промежутка времени от 6 до 36 часов, суспензию фильтруют, полученное твердое вещество промывают водой и сушат до содержания воды более 4,5, предпочтительно от 5,0 до 6,0.,отличающийся тем, что рифаксиминилирастворяют в этиловом спирте при температуре от 50 С до 60 С, добавляют деминерализованную воду до объемного соотношения этиловый спирт/вода 73, раствор охлаждают до 30 С при интенсивном перемешивании, полученную суспензию охлаждают до 0 С и выдерживают при этой температуре в течение промежутка времени от 6 до 24 часов, затем ее фильтруют и полученное твердое вещество промывают водой и сушат до содержания воды менее 2,0. 10. Способ получения рифаксимина выдерживают в условиях окружающей среды с относительной влажностью более 50 в течение промежутка времени от 12 до 48 часов. 11. Способ получения рифаксимина,отличающийся тем, что рифаксиминсушат при атмосферном давлении, или в вакууме, или в присутствии осушителя, при температуре от комнатной температуры до 105 С в течение промежутка времени от 2 до 72 часов. 12. Фармацевтическая композиция,включающая активный компонент и фармацевтически приемлемый носитель,отличающаяся тем, что в качестве активного компонента она содержит одну или более форм рифаксимина, выбранных из формы , формы ,формыили их смеси. 13. Фармацевтическая композиция по п.12,отличающаяся тем, что предназначена для приготовления лекарственных средств для перорального применения, выбранных из покрытых и непокрытых оболочкой таблеток, твердых и мягких желатиновых капсул, покрытых сахаром пилюль, пастилок, пластин, гранул и порошков в герметичных упаковках. 14. Фармацевтическая композиция по п.13,отличающаяся тем, что предназначена для приготовления лекарственных средств для местного применения, выбранных из мазей, помад, кремов,гелей и лосьонов.
МПК / Метки
МПК: A61K 31/4353, A61K 31/395, C07D 498/22, A61P 31/00
Метки: полиморфные, способы, получения, формы, рифаксимина
Код ссылки
<a href="https://kz.patents.su/12-19433-polimorfnye-formy-rifaksimina-i-sposoby-ih-polucheniya.html" rel="bookmark" title="База патентов Казахстана">Полиморфные формы рифаксимина и способы их получения</a>
Предыдущий патент: Способ размещения серы в виде жидких, при комнатной температуре, соединений
Следующий патент: Способ переработки свинецсодержащих материалов
Случайный патент: Способ комбинированной герниопластики больших вентральных грыж