Способ получения амидов ароматических карбоновых кислот
Формула / Реферат
Сущность изобретения: продукт-амиды ароматических кислот формулы 2R2-4R3+5R1+С6Н2-М-С6Н4-4R1. где R1 - галоген, OR5, R2 - H, низший алкил, R3 и R4 вместе алкилен С3-С5 с неразветвленной цепью, R5 - H, ацетил, морфолино-низш.алкил, М-CONH, NHCO. Реагент 1: 2R2-4R3-5R4-С6Н2А. Реагент 2: 4R1C6H4B. где А -карбоксил или реакционноспособное его производное и В-аминогруппа или А-аминогруппа и В-карбоксил или реакционноспособное его производное.
Текст
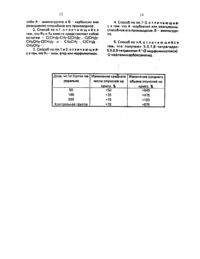
где либо А - карбоксил или реакционноспособное его производное и В т аминогруппа. либо А аминогруппа и В - карбоксил или реакционноспособътое его производное. Н 11- остаток 521. в котором наличествуюшая. возможно. аминогруппа защищена аминозаниитной группой. после чего отщепляют напичествующую. возможно. аминозащитную группу. Реакцию взаимодействия соединения с соединением Н можно осуществить известными методами ацилирования аминов. Предпочтительно подвергают взаимодействию соединение формулы 11. где А группа галогенангидрида карбоновой кислоты. например. -СОС 1. с соединением Ш. где В -МН 2. с получением соединения 1, где М СОМН-. или амин формулы с галогенангидридом карбоновой кислоты формулы Н с получением соединения 1. где М - -М--СО.Реакцию ацилирования целесообразно осуществить в присутствии основания, на 1558В качестве аминозащитньлк групп можно использовать обычно применяемые амигруппы. такие как фталоильная. бензилоксикарбонильная или трет-бутсксикарбонильная. Отщепление этих групп осуществляют с помощью обычно применяемых средств. Так. фталоилънуто труппу можно отщепить обработкой гидразином. бензилоксикарбонилвную - каталиТИЧВСКНМ гидрированием. а трегбутоксикарбонипьную - обработкой кислотами. например. разбавленной соляной или трифторуксусной кислотой.Соединения П и Ш, используемые в качестве исходных соединений формулы . если ОНИ не ИЗВВСТНЫ ИЛИ НЕ ОПИСЗНЫ НИЖЕ. можно тоже получить аналогично извест НЫМ ИЛИ НИЖЕОПИСЭННЫМ МВТОДЗМ.Соединения Представляют собой фармакодинамически ценные соединения. Их можно использовать для местной и системной терапии доброкачественных и злокачественных новообразований. предзлокачественных поражений. а также для системной и местной профилактики названных поражений.Кроме того. они пригодны для местной и системной терапии акне. псориаза и других дерматозов. сопровождаемых усилен НЫМ ИЛИ патологическим ОВОГОВВНИВМ. а также воспалительными аллергических дерматологических поражений и вышеупомянутой кожи пожилого возраста. Соединения 1 можно использовать и для лечения заболеваний слизистой оболочки. связанных С ВОСПЗЛИТВЛЬНЫМИ ИЛИ дегене 4ративными МВТЗПЛЭСТИЧВСКИМИ ИЗМЕНЕНИЯми. Противоопухолевое действие соединений формулы 1 можно испытать по нижеописанной методике. Крысам-самкам штамма ЗргаоиеОатеу выдерживают в контролируемых температурных и световых условиях со свободным доступом к питьевой воде и корму. в возрасте 50 дней каждой крысе с помощью желудочного зонда вводят 12 мг 7.1 Э-диметил-бенз(а)антрацена. После пе риода времени ок. 4 месяцев. за который вкаждой крысе выросли в среднем 3.6 4 злокачественные опухоли молочной железы, начинается лечение крыс. испытуемое вещество в виде 25-ного высушенного распылением препарата добавляют к обычному корму раз в неделю измеряются следутощие параметры вес тела крыс. среднее количество и средний объем опухолей на Е 2 х 302. где В больший и о меньший диаметр опухолевого эллипсоида.Данные. полученные по данной методике с соединением по примеру 3 при продолжительности опыта 10 недель. приведены в табл. .Соединения можно использовать идля лечения воспалительных, аллергических. ревматических и иммунологических заболеваний различных органов. Примерами подобных заболеваний могут служить ревматоидный полиартрит. Зропоуъапгтз апсуюроетйса. остеоартритидьт. артрнтиды и артрозы экземы. атонический дерматит,Нтпттйз анеготса. Азтлта ЬголЫаЕе автомамунньте заболевания. например. шриз егутпептатозиз. синдром Рейтера.Предлагаемые средства можно вводить энтрально. парентерально или местно. Пригодными для энтерального введения являются средства в виде таблеток. капсул.крысу. Объем исчисляется по формуледраже. сиропов. взвесей. растворов исуп позиториев. а для парентерального введения средства в виде растворов для инфуэий или инъекций.Дозировка вводимых препаратов определяется способом и путем введения, а также личными потребностями пациента. При оральном введении предлагаемых соединений суточная доза для взрослого составляет примерно 01-100 мг/кг, предпочтительно 05-50 мг/кг.Препараты вводятся либо одной либо несколькими дозами. предпочтительнуюформу введения представляют собой капсулы с содержанием ок. 5-500 мг действующего начала. .Препараты могут содержать инертные или же фармакодинамически активные добавки, Таблетки или гранулы могут. содержать. например. целый ряд связующих. наполнителей, носителей или разбейтелей. Жидкие препараты могут иметься. например. в виде стерильного. смешиваемого с водой раствора. Капсулы могут содержать наряду с действующим началом также наполнитель и загуститель. Далее. препараты могут содержать ароматизирующие вещества. вещества. которые обычно применяются в качестве консервантов. стабилизаторов. увлажнителей и эмульгаторов. далее. соли для изменения осмотического давления. буферы и другие добавки.Упомянутые выше носители и разбавители могут состоять из органических или неорганических веществ, таких как вода. желатина, молочный сахар, крахмал. стеарат магния. тальк. аравийская камедь. полиалкипенглътколи и т.п. Единственным условием для использования всех вспомогательных веществ в получении препаратов является их нетоксичность.Для местного применения действующие начала целесообразно использовать в виде мазей. тинктур, кремов. растворов. лосьонов, аэрозолей. взвесей и т.п. Предпочтение отдается мазям. кремам и растворам. Предназначенные для местного применения препараты приготовляют смешением предлагаемых продуктов в качестве действующего начала с нетоксичнымимнертными, пригодными для местного применения и обычно применяемыми для этих целей твердыми или жидкими носителями. Целесообразными для местного применения являются растворы концентрацией ок. 0.1-5.предпочтительно 0.34. и мази или кремы концентрацией ок. 0.16. предпочтительно ок. 0.3-2.При необходимости в препараты могут быть добавлены противоокислители. наг.ример. токоферол. М-метил- чокоферамин. а также трет-бутил-оксианизол или треп-бутил-окситолуол.П р и м е-р 1. К 2 г 5. В. 7, ЕЗ-тетрагидро 5.5.В.8.-тетраметил-2 ч-тафталин-карбоновой кислоты добавляли 15 мл тионилхлорида. после чего полученную смесь нагревали с обратным холодильником в течение одного часа. После отгонки избыточного тионилхлорьтда растворяли остаток в 10 мл ТГФ. Полученный раствор с перемешиванием по каплям добавляли краствору 1 г н-фтор-анилина в 20 мл пиридина. После перемешивания а течение 30 мин при комнатной температуре реакционную смесь выливали в ледяную воду. после чего экстрагировали этилацетатом. Затем промывали органическую фазу 2-н, соляной кислотой и водой. высушивали и выпаривали.П р и м е п . Получали 1.7 г кГ-фтор 5.Б.7.8-тетрагидро-5.5.ЗАЗ-тетраметил-З-н афталин-карбоксанилида в виде бесцветных кристаллов. т.пл. 16 З 165 С из смеси этилацетата и гексане).Пр и м е р 3. Аналогично примеру 1 52.5 г 5.6.7.В-тетрагидро-5.Б.В.В-тетраме тил-Е-нафталинкарбоновой кислоты реакцией взаимодействия с 200- мл тионилхлорида переводили в хлоридангидрид кислоты. который растворяли в 200 мл ТГФ. Полученный раствор по каплям добавляли в раствор 48.8 г 42-4-аминофенокси)тзтилморфолина в 400 мл пиридина. слегка охлаждая массу так. чтобы ее температура не превышала 30 С. После перемешивания массы в течение 1 ч при комнатной температуре въальтвали ее на ледяную оду и экстрагировали этилацетатом. Органическую фазу промывали ледяной 2-н. соляной кислотой, высушивали и выпаривали. Кристаллический сырой продукт очищали фильтрацией через колонку из силикагеля(элюенты смесьтексана и этилацетата 14. затем этилацетат, затем смесь этилацетата и этанола 11) и перекристаллизовьтвали из смеси гексана и этилацетата. Получали 52 г 5.6.7,8-терагидра-Б.5.8.В-тетраметил 4-2 морфолиноэтоксиН-нафталин-карбоксани лида в виде белых кристаллов. тлл 134136 С.Используемый в качестве исходного вещества 4-2-(4-аминофенокси)этилморфолин получали следующим образом19 г гидрида натрия (БОЭЬ-ной взвеси в минеральном- масле промывали два раза абс. пентаном. высушивали и взвешивали в130 мл димметилформамида, К полученной взвеси с охлаждением льдом по каплям добавляли раствор 42.5 н д-аминофенола в 250 мл диметилформамида. после чего перемешивали еще 1 ч при 0 С. Затем по каплям добавляли раствор 100 г д-Ъхлорзтити-морфолина в 250 мл диметилформамида. После нагревания массы в течение 1 ч до 70 С ее выливали наледяную водуи экстрагировали этилацетатом. органическую фазу промывали водой, высушивали и выпаривали. Полученное в результате темнокоричневов масло очищали фильтрацией через колонку из силикагеля злюент -4 этилацетат) и после сушки в высоком вакууме получали 66 г 4-2 ГП р и м е р 4. Аналогично примеру 1 из 2 г 5.6.7.В-тетрагидра-БЕЗ.В.В-тетраметил-2 нафталинкарбоновой кислоты и 0.95 г 4 аминофенола после перекристаллизации из смеси гексана и этилацетата получали 2.1 гП р и м е р 5. Аналогично примеру 1 из 4 г 1.1 Зд-тетраметил-Б-инданкарбоновой кислоты и 2 г д-фторанилина после перекристаллиза ции из смеси ге кса на и этилацетата получали 2.1 г 4-фтор-1 ЪЗЗ-тетраметил-Бинданкарбосканилида, т.пл. 155158 С.П р и м е р б. Аналогично примеру 2 реакция взаимодействия 5.7 г 1.1.3.3-тетраметил-Б-инданкарбоновой- кислоты с 5.8 г 4-2-(4-аминофенокси)этилморфолина поСЛЕ ПЕВЕКПИСТЭППИЗЗЦИИ ИЗ СМЕСИ ГВКСЗНЭ И этилацетата давала 5.2 г 1.1.3.3-тетра-метип-д-(2-морФолино-зтоксЩ-Б-инданкарбоП р и м е р 7. Аналогично примеру 1 из 4 г 1.1.3.3-тетраметил-Б-инданкарбоновой кислоты и 1.9 г д-аминофенола после перекристаллизации из смеси гексана и атилацетата получапи 2.3 г 4-окси-1.1.3 Зчетраметил-Б-инданкарбоксанилида. т.пл. т 96197 С.П р и м е р 8. 5.9 г 5.6.7.В-тетрагидро 5.5.В.8 тетраметил-2-нафтипамина растворяли в 50 мл пиридина и при комнатной температуре добавляли гт-фторбензоилклорид. полученный из- 4 г д-фторбенэольнойкислоты и 15 мл тионипкпорида в ТГФ. После перемешивания в течение 2 ч при комнатной температуре реакционную смесь выливали в ледяную воду и после подкисления З-н. соляной кислотой экстрагировали этилацетатом. Масло. полученное в результате высушивания и выпаривания органической фазы. перекристаллиаовывали изП р и м е р 9. 6.1 г р-(Ъморфолиноэтокстаобензоинои кислоты заливали 100 мл тионилхлорид-а и е течение одного часа нагревали с обратным холодильником. Остаток. полученный в результате упаривания избыточного тионилхлорида взвешивали в 100 мл ТГФ и по каплям добавляли его к раствору 4.9 н 5.67 В-тетрагидро-5.5.8.8 тетраметил-2-нафтиламина в 150 мл пиридина. Послеперемешивания в течение 20 ч при комнатной температуре полученную ре 1558акционную смесь выливали а ледяную воду и экстрагировали этилацетатом. После многократного промывания органической Фазы водой. высушивания сульфатом натрия и уваривания растворителя получали кристаллический сырой продукт. который подвергали дальнейшей очистке путем фильтрации сприменением силикагелевой колонки (элтоент сначала смесь гексана и этил-ацетата (1 1. а затем этилацетат) и кристаллизации из смеси гексана и этилацетата. В результате получали 8.6 г р-(2-морфолиноэтоксиюг-Е 6.7.В-тетрагид ро-5.5 ДВ.В-тетраметил-2-нафтищбензасмид а, т.пл. 130-132 С.используемую в качестве исходного продукта р-(2-морфолино-этоксюбензоиную кислоту получали следующим образом 10 г метилового эфира д-окси-бензобтной кислоты и 20.5 г 4-2-хлорэтилморфопина) растворяли в 100 мл диметилформамида и после добавления 38 г карбоната калия нагревали до 100 С в течение 1 ч. Полученную реакционную массу выливали в ледяную воду. экстрагировали этилацетатом. высушивали и выпариеали. маслянистый коричневатый остаток омыляли гидроокисью калия в смеси воды и этанола и после подкисления и перекристаллизации из смеси гексана и этилацетата давал 7.3 н р-2-морфолинозтоксигбензоинои кислоты в виде бежевых кристаллов. т.пл. 112114 с. . П р и м е р 10, Аналогично примеру 8 из 1 г 5.5.8 В-тетраметил-2-нафтиламина и 1 г В-ацетоксибензоилхлорида после перекриСТЗЛЛИЗЭЦИИ ИЗ СМЕСИ ГВКСЭНЭ И ЭТИЛЭЦВТПЭ гтолучали 1.5 г- р-(5.6,7.8-тетрагидроЪ 5.5.8.В-тетраметил-2-нафтил)карбамо илфенилацетата. т.пл. 18 б 18 ВС.В результате гидролиза этого соединения с помощью смеси гидроокиси калия. воды и этанола и перекристаллизации из смеси гексана и этилацетата получали 1.1 г р-окси-М-(5.6.7-8 тетрагидро-5.5.8 В-тетраП р и м е р 11, Аналогично примеру-В из 6.5 г 1.1.3 Зтетраметил-Б-инданамина и 4 г д-фторбензоилклорида после перекристаллизации из смеси гексана и этилацетата получали 5.5 н р-фтор-Ьд-П .1 .3.3-тетраметилЗ-инданигобензамида. т.пл. 167-169 С.П р и м е р 12. Аналогично примеру 9 из 4 н р-(Ъморфопиноэтоксщ-бензоиной кислоты и 3.1 г 1.1 Зд-тетраметил-Б-инданамина и после перекристаллизации из смеси гексане и этилацетата получали 4.6 г р-(2 морфолинозтоксЩ-Ы-П.1.3.3-тетраметил-5П р и м е р 13. Аналогично примеру 8 из 2 г 1.1 ЗДЗ-тетраметил-Б-инданамина и 2.2 н р-ацетоксибензоилхлорида после перекристаллизации из смеси гексана и этилацетата получали 2.7 г р-(1 .1.3.3-тетраметил-5-инданоиюкарбамоищфенилацетата. т.пл. 19619 вс. - -В результате гидролиза этого соединения получали 2.2 г р-окси-М-(1.1.3.3-тетраметил-З-инданищбензамида. т.пл. 1 В 5-187 С.П р и м е р 14. К 1.77 г 6.7 В.9-тетрагидро-7,Г-диметил-БН-бенаоциклогептен-З-ка рбоновои кислоты добавляли 1,17 мл З 0 С 12 и нагревали с обратным холодильником а течение 45 мин. Затем под пониженным давлением удаляли-избыточный реагент и сырой хлорангидрид кислоты Быстро высушивали в высоком вакууме. Потом его растворяли в 20 мл абс. пиридина и в атмосфере аргона при 0 С по каплям добавляли к раствору 0.97 г д-аминофенола е 16 мл абс. пиридина. Затем смеси давали прореагировать в течение еще 20 мин при комнатной температуре. после чего ее выливали в смесь льда и конц. соляной кислоты. Затем экстрагировали этилацетатом. промывали 1-н. соляной кислотой. 10-ным раствором соды и насыщенным раствором хлористого натрия. после чего высушивали сульфатом натрия. кипятили с активным углем и фильтровали. Полученный фильтрат концентрировали под пониженным давлением до начала кристаллизации продукта. в результате чего попучали 1.98 г д-окси-анилида 6.7.В.9-тетрагтгдро-7 Ъдиметил-БН-бензоциклогептен-Зг-карбоновои кислоты в виде коричневатых кристаллов, т.пл. 175-176 С.Исходный продукт получали следующим образом .К 16.3 г Са(ОС)2 в 60 мл Н 20 добавляли смесь 11.4 г К 2 С 03 и 3.40 г КОН. после чего полученную смесь растворяли в 30 мл воды. В течение 15 мин массу сильно перемешивали и потом фильтровали. К полученному фильтрату. содержащему гипохлорит калия. добавляли 6.49 г б.7.8.9-тетрагидро-7.7-диметил-БН-бензоциклогептен-2-илметилке тона и медленно нагревали. При 70 С начиналась сильно Экзотермическая реакция. вследствие чего температура поднималась до 100 С. После охлаждения реакционной смеси ее осторожно подкисляли 50 мл З-н. соляной кислоты и отфильтровывали выпавшую кислоту. После промывки водой и высушивания в высоком вакууме получали 5.48 г 67.8.9-тетрагидро-7.Ъдиметил-БН-бензоциклогептен-2-карбоновои кислоты в виде белых кристаллов. т.пл. 1 ББ 1 ПС.из 4-аминофенола и 6.7.8.9-тетрагидро-9.9 диметил-БН-бензоциклогептен-Ъкарбоно вой кислоты получали д-окси-анилид 6.7.8.9 тетрагидро-З.Э-диметил-БН-Бензоциклогеп твид-карбоновой кислоты в виде белых кристаллов. т.пл. 14714 ВС. Исходное соединение можно получить следующим образомИэ,4.00 г 2-6 ром-6.78.9-тетрагидр 0-99 дИМетил-бН-бензоциклотептена ЕРА 20315071) и 456 мг магниевои стружки в атмосфере аргона в-20 мл абс. ТГФ получают соединение Гриньяра. После металлизации при 10 С в массу вводят сильный поток СО 2. Массу гидролиэуют разбавленной соляной кислотой. экстрагируют диэтиловым эфиром и промывают небольшим количеством воды. Затем очищают кислоту экстрагированием 1-н. МаОН. подкислением соляной кислотой до значении рН 1 и повторной экстракцией диэтиловым эфиром. После промывки водой. высушивания сульфатом натрия и выпаривания получают 2.64 г 6.7.8.9-тетрагидро-9 В-диметил-БР бензоциклогептен-2-карбоноаой кислоты оИсходный материал можно синтезировать иа этилбензола. ангидрида З.3-диметилглутаровой кислоты и ацетилхлорида (см. Е Р-А 2-О 315 О 71).можно получить следующие соединения анилид 6.8.9-тетрагидро 4-окси-Б.5 диметил-БЩ-бенэоциклогегттен-З-карбоно вой кислоты р-фтор-М-бдВВ-тетрагидрод/.9.9-три метил-БН-бе изо-цикленептен--ищбензам ътд
МПК / Метки
Метки: карбоновых, ароматических, получения, способ, кислот, амидов
Код ссылки
<a href="https://kz.patents.su/7-1558-sposob-polucheniya-amidov-aromaticheskih-karbonovyh-kislot.html" rel="bookmark" title="База патентов Казахстана">Способ получения амидов ароматических карбоновых кислот</a>