Способ получения редких металлов
Номер патента: 26691
Опубликовано: 15.02.2013
Авторы: УЦУНОМИЯ, Казухиро, ФУДЗИТА, Рейко, НАКАМУРА, Хитоси, ОМОРИ, Такаси, КАНАМУРА, Сохеи, МИЗУГУТИ, Кодзи, НОМУРА, Сундзи
Текст
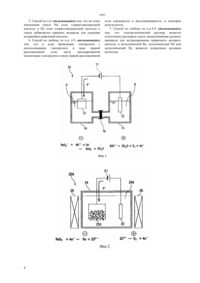
(51) 25 3/34 (2006.01) 22 3/44 (2006.01) 22 59/00 (2006.01) КОМИТЕТ ПО ПРАВАМ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ МИНИСТЕРСТВА ЮСТИЦИИ РЕСПУБЛИКИ КАЗАХСТАН(54) СПОСОБ ПОЛУЧЕНИЯ РЕДКИХ МЕТАЛЛОВ(57) В соответствии с одним воплощением способ получения редких металлов включает в себя этапы электролиза электролитического раствора для экстрагирования оксидана катоде извлечения оксидаи электролиза оксидав электролите из расплавленной соли для экстрагирования металлического извлечения остаточного раствора, содержащегообработки остаточного раствора, содержащего , для получения оксидаэлектролиза оксидав электролите из расплавленной соли для экстрагирования металлическогоизвлечения остаточного раствора, содержащего , обработки остаточного раствора, содержащего , для получения оксида, и электролиза оксидав электролите из расплавленной соли для экстрагирования металлического .(74) Русакова Нина Васильевна Жукова Галина Алексеевна Ляджин Владимир Алексеевич Область техники, к которой относится изобретение Описанные здесь воплощения, в общем относятся к способу получения редких металлов и в частности относятся к способу получения рения, неодимияи диспрозияв растворе. Известный уровень техники Ренийявляется особо редким металлом среди редких металлов и используется для армирования материалов,например,для авиационных турбин. В качестве общепринятого процесса для получения металлического рения известен процесс,в котором из руды получают аммониевый перренат рения (АПР), как промежуточный продукт, который восстанавливают в потоке водорода при приблизительно 150 С для получения металлического рения. Более того обычно редкоземельные металлы,например, неодимийи диспрозий ,используемые как сырьевой материал для магнитов,трудно разделяются на отдельные металлы, так как эти элементы имеют сходные химические свойства. В качестве общепринятого процесса для разделения этих металлическихиизвестен процесс, в котором руда растворяется серной кислотой и тому подобным затем такие примеси как щелочные металлы и металлы платиновой группы отделяются и удаляются способом осаждения щавелевой кислотой и редкоземельные металлы отделяются один от другого и восстанавливаются фтористым кальцием. В качестве альтернативного процесса для разделения этих редкоземельных металлов известен процесс, в котором редкоземельные металлы отделяются один от другого и извлекаются путем испарения оксидов редкоземельных металлов в расплавленной соли (см. например, Патентный документ 1 (Японская выложенная патентная заявка 2005-201765. К сожалению в общепринятых процессах расход кислот, щелочей, органических растворителей и ионообменных смол дает большое количество вторичных отходов, в результате чего получают этот АПР, как промежуточный продукт в производстве металлического рения. Другой проблемой является малая скорость восстановления оксидов редкоземельных металлов,таких каки , и трудное воспроизведение используемого восстанавливающего агента, что снова приводит к получению большого количества вторичных отходов. С другой стороны, не было сообщений о способе независимого разделения металлического рения и редкоземельных металлов, таких как металлическийи металлическийи извлечения этих металлов посредством целого ряда этапов. Сущность изобретения Настоящее изобретение было сделано с учетом таких обстоятельств. Целью настоящего изобретения является обеспечение способа получения редких металлов, посредством которого редкие металлы могут быть разделены и извлечены 2 посредством ряда этапов и может быть уменьшено количество вторичных отходов. Способ получения редких металлов в соответствии с настоящим изобретением включает в себя этапы электролиза электролитического раствора, содержащего, по меньшей мере,элементарный , для экстрагирования оксидана катоде извлечения оксидаи электролиза оксидав электролите из первой расплавленной соли для экстрагирования металлическогона катоде. В соответствии со способом получения редких металлов по настоящему изобретению, посредством ряда этапов, редкие металлы, как вторичные целевые металлы, могут быть разделены и извлечены из остаточного раствора после выщелачивания рудного минерала для экстрагирования первичного целевого металла. Это обеспечивает способ получения редких металлов,посредством которого число этапов снижается и количество образующихся вторичных отходов уменьшается. Краткое описание чертежей Фиг.1 является схематическим изображением,показывающим воплощение электролитической ванны с раствором, которая является компонентом системы для получения редких металлов в соответствии с настоящим изобретением. Фиг.2 является схематичным изображением,показывающим воплощение электролитической ванны с первой расплавленной солью, которая является компонентом системы для получения редких металлов в соответствии с настоящим изобретением. Фиг.3 является схематичным изображением,показывающим воплощение электролитической ванны со второй расплавленной солью, которая является компонентом системы для получения редких металлов в соответствии с настоящим изобретением. Фиг.4 является изображением блок-схемы технологических операций, показывающей первое воплощение процесса для получения редких металлов в соответствии с настоящим изобретением и Фиг.5 является изображением блок-схемы технологических операций, показывающей второе воплощение процесса для получения редких металлов в соответствии с настоящим изобретением. Подробное описание(Первое воплощение) Ниже на основе приведенных изображений будут описаны воплощения в соответствии с настоящим изобретением. Система для получения редких металлов в соответствии с первым воплощением настоящего изобретения включает в себя электролитическую ванну 10 с раствором (Фиг.1) и электролитическую ванну 20 с первой расплавленной солью (Фиг.2) . Система для получения редких металлов,имеющая такую конфигурацию, отделяет и извлекает оксидиз электролитического раствора Р, в котором растворены ионы, содержащие элементарный , и ионы, содержащие другие металлические элементы. Кроме того в случае,когда другими металлическими элементами являются элементарныйи элементарный ,относящиеся к редкоземельным металлам, система для получения независимо разделяет и извлекает металлическийи металлический . Как показано на Фиг.1, электролитическая ванна 10 с раствором включает в себя катод 12,соединенный с отрицательным полюсом источника питания 11 постоянного тока, и анод 13,соединенный с положительным полюсом источника питания 11 постоянного тока катодную камеру 14,вмещающую электролитический раствор Р, в который погружен катод 12 анодную камеру 15,вмещающую буферный раствор , в который погружен анод 13, и диафрагму 16, расположенную на границе раздела между катодной камерой 14 и анодной камерой 15. В электролитической ванне 10 с раствором,имеющей такую конфигурацию, оксидосаждается на катоде 12 и экстрагируется электролизом электролитического раствора Р, в котором растворены ионы оксида . Раствор, используемый в качестве этого электролитического раствора Р,является остаточным раствором, полученным при мокром рафинировании с целью получения первичного целевого металла, например, такого как уран, медь и молибден, но не только их. Раствор, содержащий элементарный и элементарный , может быть использован должным образом. В качестве буферного раствораиспользуется такой же кислый раствор как и электролитический раствор Р,но который не содержит вышеупомянутых металлических элементов. Этот буферный раствор отделяют от электролитического раствора Р посредством диафрагмы 16 так, чтобы буферный растворне мог смешиваться с электролитическим раствором Р,а ионы могли свободно проходить через диафрагму. Когда между катодом 12 и анодом 13 прикладывается напряжение для проведения электролиза, то ионы оксида , растворяющиеся в электролитическом растворе Р, восстанавливаются до оксидатак, чтобы он осаждался на катоде 12. Затем катод 12, имеющий осажденный на нем оксид, вынимается из электролитической ванны 10 с раствором и обжигается на воздухе приблизительно при температуре от 100 до 300 С для удаления влаги. Таким образом получают порошковый оксид. Материалом для катода 12 должен быть металлический материал, имеющий большое водородное перенапряжение для того, чтобы подавить реакцию образования водорода, которая конкурирует с реакцией осаждения оксида . Материалом для катода 12 предпочтительно иметь один из таких как кадмий, ртуть, таллий,индий, олово, свинец, висмут, графит, медь, тантал,ниобий, бериллий, алюминий, серебро, железо,молибден, никель, гладкая платина, вольфрам и золото, или их сплавы. В случае использования тантала для катода 12,полученный результат исследования показывает,что степень извлечения оксидадостигает 70. С другой стороны, степень извлечения в случае использования пластины в качестве обычного катодного материала составляет от 13 до 16. Это сравнение показывает, что степень извлечения в случае применения тантала повышается не менее чем в 4 раза, чем в случае использования платины. Здесь реакция на катодном электроде 12 и реакция на анодном электроде 13 соответственно представлены следующими формулами (1) и (2). Известно, что элементарныйимеет валентность от -1 до 7. Поэтому оксидимеет разные формы, такие как О 2, О 3, 2 О 7, 2 О 3,и действительная химическая реакция на электроде является сложной. Катод О 4-4 Н 3 е-О 22 Н 2 О (1) Анод 4 ОН-2 Н 2 ОО 24 е(2) После окончания реакций (1) и (2) на электродах электролитический раствор Р остается в электролитической ванне 10 в качестве остаточного раствора, содержащего элементарныйи элементарный . Затем будет описан способ независимого разделения и извлечения элементарныхииз остаточного раствора, содержащегои , как оксида(2 О 3) и оксида(2 О 3). Остаточный раствор, содержащийи ,извлеченный из электролитической ванны 10,перемещается в другую реакционную емкость (не показана). Затем в остаточный раствор, содержащийи , добавляется избыточное количество сульфата натрия (2 О 4), как сульфата щелочного металла, и смесь нагревается. Затем только ,легкий редкоземельный металл, кристаллизуется как сульфат неодимия (2(О 4)3), который является неодимиевой солью серной кислоты, и избирательно осаждается. Затем добавляется щавелевая кислота СООН)2) к сульфату неодимия, удаленному из реакционной емкости (не показана), для получения оксалата неодимия(23),который является неодимиевой солью щавелевой кислоты. Оксалат неодимия сушится для удаления влаги. Затем оксалат неодимия смешивается с хлористым калием (КС) и хлористым литиеми температуру смеси повышают приблизительно до 500 С в нагревательной печи (не показана). Затем оксалат неодимия подвергается удалению моноокиси углерода (СО) из этой смешанной расплавленной соли, и он превращается его в оксид неодимия (23) . С другой стороны, тяжелый редкоземельный металлрастворяется в остаточном растворе с другими примесями даже после кристаллизации сульфата неодимия и его осаждения. Затем,добавляя щавелевую кислоту в остаточный раствор,содержащий , получают оксалат диспрозия(у 2(СОО)3), являющийся диспрозиевой солью щавелевой кислоты, которую осаждают и отделяют от других примесей. 3 Оксалат диспрозия сушится для удаления влаги. Затем таким же образом как и в случае этапа,упомянутого выше, оксалат диспрозия смешивается с хлористым калием (КС) и с хлористым литием и температуру смеси повышают приблизительно до 500 С в нагревательной печи (не показана). Затем оксалат диспрозия подвергают удалению моноокиси углерода (СО) из этой смешанной расплавленной соли и превращают его в оксид диспрозия (23) . Как показано на Фиг.2, электролитическая ванна 20 с первой расплавленной солью включает в себя катод 22 А, соединенный с отрицательным полюсом источника питания 21 постоянного тока, анод 23,соединенный с положительным полюсом источника питания 21 постоянного тока электролизную камеру 24, вмещающую электролит 26 А из первой расплавленной соли, и нагреватель 25, который управляет температурой электролита 26 А из первой расплавленной соли. В электролитической ванне 20 А с первой расплавленной солью,имеющей такую конфигурацию, оксид , извлеченный из раствора в электролитической ванне 10,подвергается электролизу в электролите 26 А из первой расплавленной соли, при этом приставшие компоненты удаляются из оксида . Тем самым оксидвосстанавливается на катоде 22 А так, что извлекается металлический . Кроме того в электролитической ванне 20 с первой расплавленной солью извлекается металлическийпосредством электролиза оксида, извлеченного из остаточного раствора,содержащего , вместо оксида . Аналогичным образом в электролитической ванне 20 А с первой расплавленной солью,металлический извлекается электролизом оксида , извлеченного из остаточного раствора, содержащего . Электролит 26 А из первой расплавленной соли может быть одной из нижеперечисленных смешанных солей смешанная соль из хлористого литияи оксида лития (2 О), смешанная соль из хлористого магния (МС 2) и оксида магния(МО) и смешанная соль из хлористого кальция(СаС 2) и оксида кальция (СаО). Здесь подходящим образом используется смешанная соль из хлористого лития (2) и оксида лития (2) для электролиза оксида , и смешанная соль из хлористого магния и оксида магния подходящим образом используется для электролиза оксидаи оксида . Здесь доля компонента в виде оксида металла(2,и СаО) в смешанной соли, которая образует электролит 26 А из первой расплавленной соли, составляет приблизительно 1 от всей смешанной соли. Роль, которую играет оксид металла, как компонент, будет описана с использованием случая электролиза оксида . Металлический ,получаемый реакцией на электроде по следующей формуле (3), которая протекает одновременно с реакцией на электроде по формуле (4), описанной ниже, удаляет молекулы кислорода из оксида . 4 Это может ускорить восстановление оксида ,поэтому металлическийможет быть извлечен эффективно. Катод 22 е-2 О 2(3) Между прочим, нежелательное окисление смешанной соли, которая составляет электролит 26 А из первой расплавленной соли, также продолжается и при электролизе оксида , оксидаили оксида . Если продолжение этого нежелательного оксидирования увеличивает компонент в виде оксида металла (2,и СаО) электролита 26 А из первой расплавленной соли, то процесс электролиза в электролитической ванне 20 с расплавленной солью, будет предотвращен. Поэтому с точки зрения уменьшения, количество образующихся вторичных отходов предпочтительно,чтобы часть такой оксидированной композиции из электролита 26 А с первой расплавленной солью была извлечена,восстановлена и повторно использована. Катод 22 А имеет форму корзинки, которая содержит порошок оксида , оксида , или оксида , и он делается из нержавеющей стали. Катод 22 А погружается в электролит 26 А из первой расплавленной соли и содержит один из оксидов ,и , причем этот оксид восстанавливается до металла. Анод 23 может быть сделан из такого материала,как платина или углерод, и он удаляет ионы кислорода в виде газообразного кислорода или газообразного диоксида углерода. Затем будет описана реакция на электроде в каждом случае электролиза оксида , оксидаи оксида . При реакции на аноде в качестве анода используется платина. ксидКатод 24 е-22(4) Анод 22-24 е(5) ксидКатод 236 е-23 О 2(6) Анод 3 О 2-3/226 е(7) ксидКатод 236 е-23 О 2(8) Анод 3 О 2-3/226 е(9) Процесс для получения редких металлов в соответствии с первым воплощением будет описан со ссылкой блок-схему технологических операций на Фиг.4. Сначала минерал в виде руды подвергают предварительной обработке(размельчению,концентрации, обжигу) (11) и выщелачивают кислым или щелочным раствором (12). Первичный целевой металл экстрагируют из выщелачивающего раствора (13). Остаточный раствор, который остается после экстрагирования первичного целевого металла и содержит элементарный ,элементарныйи элементарный , извлекается(14). Остаточный раствор содержится как электролитический раствор Р в катодной камере 14 электролитической ванны 10 для раствора. Оксид осаждается на катоде 12 посредством электролиза и экстрагируется (15) . Оксидизвлекается и из него удаляются внедрившиеся компоненты (6) . Оксид удерживается катодом 22 А электролитической ванны с первой расплавленной солью и подвергается электролизу (17). Затем после завершения электролиза катод 22 А удаляется из электролита, состоящего из первой расплавленной соли, так, чтобы металлическийэкстрагировался в качестве металла,как субпродукта (18). С другой стороны, после завершения этапа электролиза (15) в электролитической ванне 10 с раствором, остаточный раствор, содержащийи, который остается после экстрагирования оксидаи содержит элементарныйи элементарный, извлекается для использования (21). В этот остаточный раствор (22), содержащийи , добавляется сульфат щелочного металла(24) для кристаллизации неодимиевой соли серной кислоты (2(4)3) (23). Затем неодимиевую соль серной кислоты(2(4)3 извлекают. К ней добавляют щавелевую кислоту СООН)2) и проводят с ней реакцию (24) для получения неодимиевой соли щавелевой кислоты (23) (25). СО удаляется из этой неодимиевой соли щавелевой кислоты для получения оксида(23) (26). Оксидизвлекается и удерживается катодом 22 А электролитической ванны 20 с первой расплавленной солью, и подвергается электролизу(27). Затем после завершения электролиза катод 22 А удаляется из электролита 26 А из первой расплавленной соли так, чтобы металлическийэкстрагировался как вторичный целевой металл(28). Более того,после завершения этапа кристаллизации неодимиевой соли серной кислоты(23), остаточный раствор, содержащий ,который остается после экстрагирования неодимиевой соли серной кислоты и содержит элементарный , извлекается (31) . К этому остаточному раствору, содержащему ,добавляется щавелевая кислота СООН)2) для кристаллизациисоли щавелевой кислоты (32) и кристаллизовавшаясясоль щавелевой кислоты(23) извлекается (33). СО удаляется из этойсоли щавелевой кислоты для получения оксида(23) (34) . Этот оксидизвлекается, удерживаемый катодом 22 А электролитической ванны 20 А (35) с первой расплавленной солью, и расплавленная соль подвергается электролизу. Затем после завершения электролиза катод 22 А удаляется из электролита 26 А из первой расплавленной соли так, чтобы металлический экстрагировался как металлический субпродукт (36). В соответствии со способом для получения редких металлов в соответствии с первым воплощением настоящего изобретения количество полученных вторичных отходов составляет 500 кг/год, что является приблизительно 50(Второе воплощение) Система для получения редких металлов в соответствии со вторым воплощением настоящего изобретения включает в себя электролитическую ванну 10 с раствором (Фиг.1), электролитическую ванну 20 А с первой расплавленной солью (Фиг.2) и электролитическую ванну 20 В (Фиг.3) со второй расплавленной солью. Здесь электролитическая ванна 10 является такой же, как уже была описана, и ее описание будет исключено. Среди компонентов, описанных на Фиг.3 с электролитической ванной 20 В со второй расплавленной солью, те же самые цифровые ссылки будут даны компонентам, одинаковыми с компонентами, описанными на Фиг.2, и описание их будет исключено со ссылкой на вышеупомянутое описание. Система для получения редких металлов в соответствии со вторым воплощением, имеющая такую же конфигурацию, также разделяет и извлекает металлическийиз электролитического раствора Р сначала таким же образом, как и в случае первого воплощения. С другой стороны, в отличие от первого воплощения система для получения редких металлов в соответствии со вторым воплощением разделяет и извлекает элементарныйи элементарныйкак редкоземельные металлы из остаточного раствора после отделения . Сначала перед описанием электролитической ванны 20 В со второй расплавленной солью будет описана предварительная обработка остаточного раствора, содержащегои , выводимого из электролитической ванны 10 с раствором и подвергаемого электролизу в электролитической ванне 20 В со второй расплавленной солью. Остаточный раствор, содержащийи ,извлеченный из электролитической ванны 10 с раствором, перемещается в другую реакционную емкость (не показана) и добавляется щавелевая кислота СООН)2). Затем получают и осаждают смесь оксалата неодимия (23), который являетсясолью щавелевой кислоты, и оксалата диспрозия (23), который являетсясолью щавелевой кислоты. Соляная кислота (НС) в качестве хлорирующего агента добавляется к этим осажденным оксалату неодимия и оксалату диспрозия и температура смеси устанавливается приблизительно 90 С. Затем оксалат неодимия и оксалат диспрозия химически изменяются соответственно в хлористый неодимий(3), который является неодимиевой солью соляной кислоты, и в хлористый диспрозий (3),который является диспрозиевой солью соляной кислоты, и затем они превращаются в раствор хлоридов, в котором хлорид неодимия и хлорид диспрозия растворены в растворителе для хлоридов. Затем, когда раствор хлоридов нагревается при добавлении в него перекиси водорода,непрореагировавшая щавелевая кислота может быть разложена на хлориды и удалена. 5 Этот раствор хлоридов далее нагревается и сушится при температуре приблизительно 200 С в атмосфере инертного газа для полного удаления влаги. Таким образом получают смесь безводного хлорида неодимия и безводного хлорида диспрозия,т.е. смесьсоли хлористоводородной кислоты исоли хлористоводородной (соляной) кислоты. Выше была описана предварительная обработка остаточного раствора, содержащегои . Как показано на Фиг.3, электролитическая ванна 20 В со второй расплавленной солью включает в себя катод 22 В, соединенный с отрицательным полюсом источника питания 21 постоянного тока,анод 23, соединенный с положительным полюсом источника питания 21 постоянного тока,электролизную камеру 24 с электролитом 26 В из второй расплавленной соли, и нагреватель 25,который управляет температурой электролита 26 В из второй расплавленной соли. В электролитической ванне 20 В со второй расплавленной солью,имеющей такую конфигурацию, смесьсоли хлористоводородной кислоты исоли хлористоводородной кислоты,полученная предварительной обработкой,подвергается электролизу в электролите 26 В из второй расплавленной соли. Металлическийизбирательно осаждается на катоде 22 В и затем катод 22 В заменяется другим катодом для избирательного осаждения металлического . В качестве второй расплавленной соли электролита 26 В могут использоваться смешанные соли бинарных систем хлоридов щелочных металлов, например, такая как смешанная соль из хлорида калия (КС) и хлорида натрия ,смешанная соль из хлорида калия (КС 1) и хлорида литияи смешанная соль из хлорида натрия и хлорида цезия , или смешанные соли бинарных систем из хлоридов щелочноземельных металлов. Также может быть использована смешанная соль из фторида калия и фторида натрия. Среди ионов(3) и ионов(3),растворенных в расплавленной соли, ионы ,имеющие более высокий окислительновосстановительный потенциал, предпочтительно восстанавливаются до металлического , так что на катоде 22 В осаждается металлический . Таким образом металлическийизвлекается на катоде 22 В (формула (10) реакции). Затем катод 22 В заменяют новым катодом и между катодом 22 В и анодом 23 прикладывают напряжение. Затем ионывосстанавливают до металлического , так что на катоде 22 В осаждается металлический . Таким образом извлекается металлический(формула (11) реакции). С другой стороны, на аноде 23 ионы хлора становятся газообразным хлором,который удаляется (формула (12) реакции). Процесс для получения редких металлов в соответствии со вторым воплощением будет описан со ссылкой на блок-схему технологических операций на Фиг.5. Этапы от 11 до 18 во втором воплощении являются такими же, как и этапы в первом воплощении, и их описание будет исключено со ссылкой на уже приведенное описание. После завершения этапа электролиза (15) в электролитической ванне 10 с раствором,остаточный раствор, содержащийи , который остается после экстрагирования оксидаи содержит элементарныйи элементарный ,извлекается (41). Щавелевая кислота СООН)2) добавляется к остаточному раствору содержащемуи , и реагирует с ним для кристаллизациисоли щавелевой кислоты (23) исоли щавелевой кислоты (23) (42). Смесьсоли щавелевой кислоты (23) исоли щавелевой кислоты (2(С)3), которая таким образом была кристаллизована, извлекается (43). Затем добавляется НС 1 как хлорирующий агент в смесьсоли щавелевой кислоты исоли щавелевой кислоты для получения смешанного растворасоли хлористоводородной кислоты(3) (44). Перекись водорода добавляется к смешанному растворусоли хлористоводородной кислоты исоли хлористоводородной кислоты для удаления оставшейся щавелевой кислоты (45). Растворитель удаляется из смешанного раствора и смесьсоли хлористоводородной кислоты исоли хлористоводородной кислоты извлекается(46). Затем смесьсоли хлористоводородной кислоты исоли хлористоводородной кислоты смешивается с электролитом 26 В из второй расплавленной соли во второй электролитической ванне 20 В со второй расплавленной солью и проводится электролиз расплавленной соли (47). В результате этого металлическийизбирательно осаждается на катоде 22 В и извлекается как второй целевой металл (48) . Затем катод 22 В, на котором имеется осажденный металлический , вынимается и заменяется другим катодом (51). Затем проводится электролиз расплавленной соли изсоли хлористоводородной кислоты,которая осталась в электролите 26 В из второй расплавленной соли (52). В результате этого металлическийизбирательно осаждается на новом катоде 22 В и экстрагируется как металлический субпродукт (53) . Хотя некоторые воплощения и были описаны,они были представлены только ради примера и не предназначены для ограничения объема изобретения. Действительно, описанные здесь новые способ и система могут быть воплощены в различных других формах кроме того различные опущения, замены и изменения в форме способов и систем, описанных здесь, могут быть сделаны без отступления от смысла изобретений. Приведенные пункты формулы изобретения и их эквиваленты предназначены для охвата таких форм или модификаций, которые совпадали бы с объемом и смыслом изобретений. Например,воплощения основаны на предположении, что все из таких элементов, как элементарный и элементарныйсодержатся в электролитическом растворе Р. Однако, даже если один из этих элементов возможно будет отсутствовать, другие элементы могут быть независимо разделены и извлечены в виде металлов. Хотя извлечение редких металлов из остаточного раствора после экстрагирования первого целевого металла из рудного минерала было показано в виде примера, настоящее изобретение не будет ограничиваться таким его применением. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ получения металлического рения ,отличающийся тем, что содержит этапы электролиза электролитического раствора,содержащего, по меньшей мере, элементарный ,для экстрагирования оксидана катоде извлечение оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде. 2. Способ получения редких металлов,отличающийся тем, что содержит этапы электролиза электролитического раствора,содержащего, по меньшей мере, элементарныйи элементарный , для экстрагирования оксидана катоде извлечение оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде извлечения остаточного раствора, содержащего элементарный , после завершения этапа электролиза электролитического раствора добавления сульфата щелочного металла к остаточному раствору, содержащему , для кристаллизациисоли серной кислоты извлечениясоли серной кислоты, и проведения реакциисоли серной кислоты со щавелевой кислотой для получениясоли щавелевой кислоты обработкисоли щавелевой кислоты для получения оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде. 3. Способ получения редких металлов,отличающийся тем, что содержит этапы электролиза электролитического раствора,содержащего, по меньшей мере, элементарный ,элементарныйи элементарныйдля экстрагирования оксида е на катоде извлечения оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде извлечения остаточного раствора, содержащего элементарный,после завершения этапа электролиза электролитического раствора добавления сульфата щелочного металла к остаточному раствору, содержащему , для кристаллизациисоли серной кислоты извлечениясоли серной кислоты, и проведения реакциисоли серной кислоты со щавелевой кислотой для получениясоли щавелевой кислоты обработкисоли щавелевой кислоты для получения оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде извлечения остаточного раствора, содержащего элементарный,после завершения этапа криталлизациисоли серной кислоты извлечениясоли щавелевой кислоты,кристаллизовавшейся при добавлении щавелевой кислоты в остаточный раствор, содержащийобработкусоли щавелевой кислоты для получения оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде. 4. Способ получения редких металлов,отличающийся тем, что содержит этапы электролиза электролитического раствора,содержащего, по меньшей мере, элементарный ,элементарныйи элементарныйдля экстрагирования оксида е на катоде извлечения оксидаи проведения электролиза оксидав электролите в виде первой расплавленной соли для экстрагирования металлическогона катоде извлечения остаточного раствора, содержащего элементарныйи элементарный , после завершения этапа электролиза электролитического раствора извлечения смесисоли щавелевой кислоты исоли щавелевой кислоты, кристаллизовавшейся при добавлении щавелевой кислоты к остаточному раствору, содержащемуиизвлечения смесисоли хлористоводородной кислоты исоли хлористоводородной кислоты,полученной при добавлении хлорирующего агента к смесисоли щавелевой кислоты исоли щавелевой кислоты проведения электролиза смеси соли хлористоводородной кислоты и соли хлористоводородной кислоты в электролите в виде второй расплавленной соли для избирательного экстрагирования металлическогона катоде удаления катода, имеющего осажденный на нем металлический , и замена его другим катодом и проведения электролиза оставшейсясоли хлористоводородной кислоты в электролите в виде второй расплавленной соли для избирательного экстрагирования металлическогона замененном катоде. 7 5. Способ по п.4, отличающийся тем, что на этапе извлечения смесисоли хлористоводородной кислоты исоли хлористоводородной кислоты к смеси добавляется перекись водорода для удаления оставшейся щавелевой кислоты. 6. Способ по любому из п.п. 4-5, отличающийся тем, что в ходе проведения электролиза с использованием электролита в виде первой расплавленной соли часть оксидированной композиции электролита в виде первой расплавленной соли извлекается и восстанавливается, и повторно используется. 7. Способ по любому из п.п.4-5, отличающийся тем, что электролитический раствор является остаточным раствором после выщелачивания рудного минерала для экстрагирования первичного целевого металла, и металлический , металлическийили металлическийявляется вторичным целевым металлом.
МПК / Метки
МПК: C25C 3/34, C22B 3/44, C22B 59/00
Метки: способ, металлов, редких, получения
Код ссылки
<a href="https://kz.patents.su/10-26691-sposob-polucheniya-redkih-metallov.html" rel="bookmark" title="База патентов Казахстана">Способ получения редких металлов</a>
Предыдущий патент: Способ и система для управления локомотивом и блокировочная система для использования с транспортным средством
Следующий патент: Конструкция дренажа в плите перекрытия и способ восстановления проникающего отверстия в плите перекрытия
Случайный патент: Спусковое устройство для лука