Новые сложные боронатные эфиры и способ их синтеза (варианты)
Номер патента: 17644
Опубликовано: 15.09.2009
Авторы: ПУТХИАПРАМПИЛ, Том, Томас, СРИДХАРАН, Мадхаван, СРИНАТХ, Сумитхра, ГАНЕШ, Самбазивам
Формула / Реферат
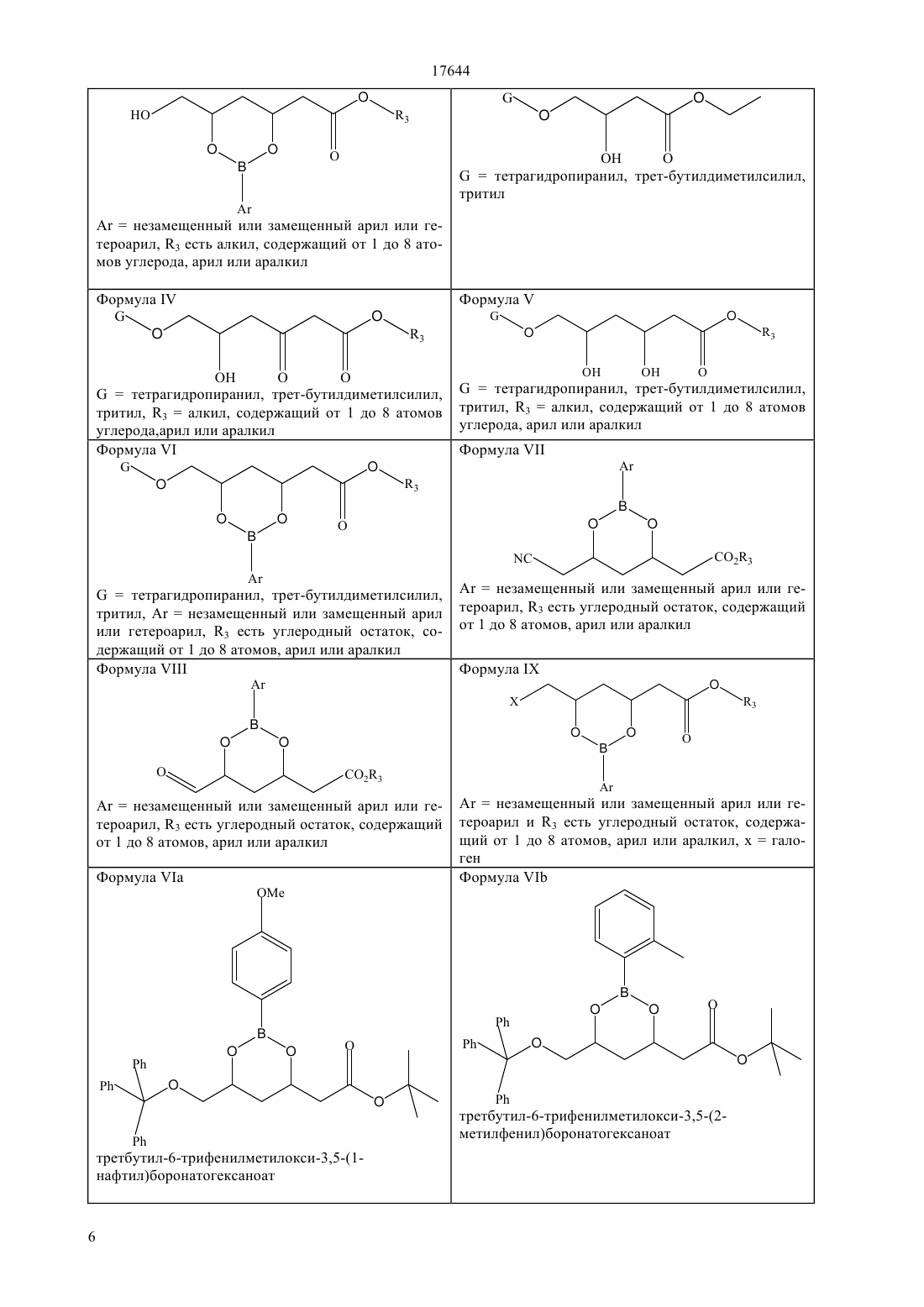
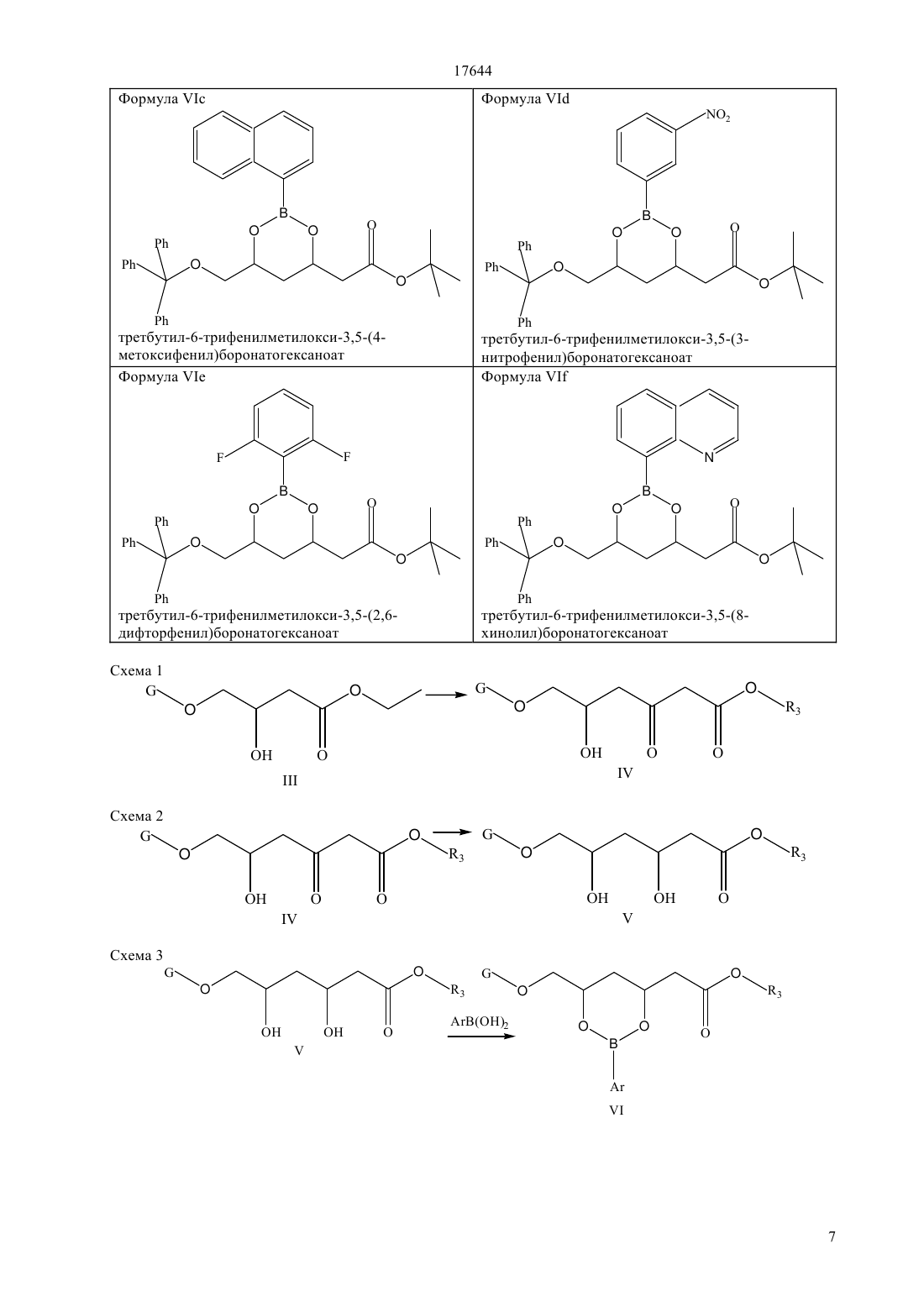
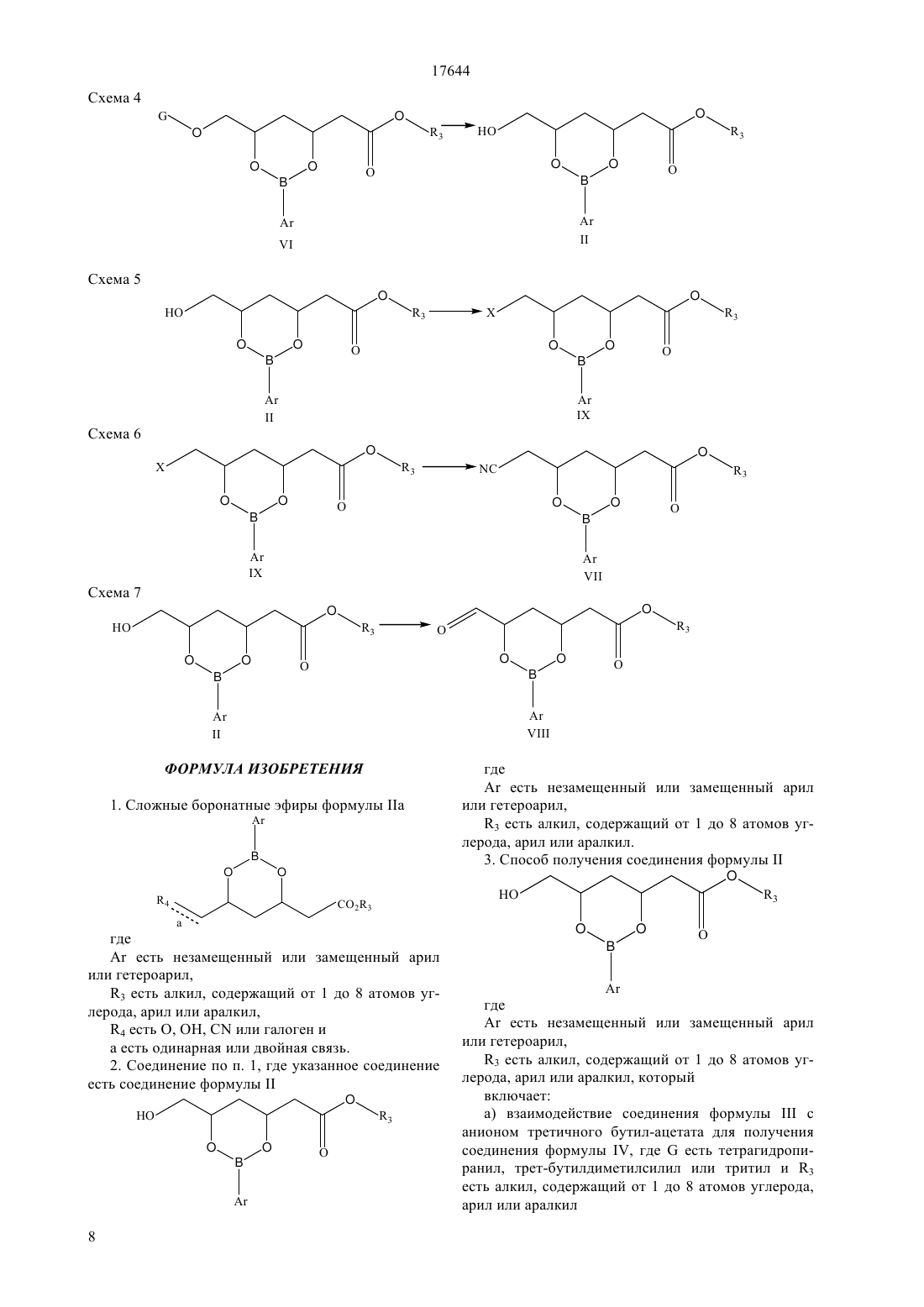
Настоящее изобретение относится к оптически активным производным дигидроксигексаноатов, сложным эфирам бороновой кислоты формулы IIа, которые являются полезными промежуточными соединениями для синтеза ингибиторов фермента HMG-CoA, таких как аторвастатин, церивастатин, розувастатин, питавастатин, флувастатин
Аr есть незамещенный или замещенный арил или гетероарил,
R3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,
R4 есть О, ОН, CN или галоген и
а есть одинарная или двойная связь.
Текст
(51) 07 5/04 (2006.01) 07 5/00 (2006.01) КОМИТЕТ ПО ПРАВАМ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ МИНИСТЕРСТВА ЮСТИЦИИ РЕСПУБЛИКИ КАЗАХСТАН ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУ сложным эфирам бороновой кислоты формулы а,которые являются полезными промежуточными соединениями для синтеза ингибиторов фермента А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,4 есть О, ОН,или галоген и а есть одинарная или двойная связь.(54) НОВЫЕ СЛОЖНЫЕ БОРОНАТНЫЕ ЭФИРЫ И СПОСОБ ИХ СИНТЕЗА (ВАРИАНТЫ)(57) Настоящее изобретение относится к оптически активным производным дигидроксигексаноатов, 17644 Настоящее изобретение относится к оптически активным производным дигидроксигексаноата формулы а, в частности, к соединениям формулы ,которые являются полезными промежуточными соединениями для синтеза ингибиторов фермента 23 , где 1 и 2 - независимо выбранные алкилы, содержащие от одного до трех атомов углерода, а 3 алкил, содержащий от 1 до 8 атомов углерода, далее, соединения формулы а 1 23 , где 1 и 2 - группы, независимо выбранные из алкилов, содержащих от одного до трех атомов углерода, и фенила, или 1 и 2, оба представляют собой -С 2)-группы, гдеравно 4 или 5, 3 является алкилом, содержащим от 1 до 8 атомов углерода,а также соединения формулы 1 ные стадии (озонирование) для получения желаемого продукта. В патенте США 5998633 описан процесс получения защищенных сложных эфиров 3,4-дигидроксибутановой кислоты из карбогидратного остатка, который превращается в желаемые производные 3,4 дигидроксибутановой кислоты примерно в 4 стадии. Производное 3,4-дигидроксибутановой кислоты преобразуется затем в соединения формулычерез процесс, включающий большое количество стадий. В патенте США 6140527 описан процесс получения производных бутановой кислоты, исходя из производного бутена, с последующей реакцией с добавлением реагента, обладающего способностью присоединения через двойную связь. Однако эта процедура не дает хиральных молекул и, следовательно, неизбежно влечет за собой необходимость стадии разделения. В европейском патенте 0104750 описан процесс получения производных гидрокси-3-оксопентановой кислоты путем алкилирования производных 3 гидроксибутирата. Упомянутые в этом патенте производные являются рацемическими молекулами и поэтому требуют стадии разделения. Целью настоящего изобретения является обеспечение простого процесса, позволяющего получать производные формулыв промышленных масштабах, исходя из коммерчески доступной и недорогой яблочной кислоты. Достижение указанной цели в настоящем изобретении обеспечивается соединением формулы а,и в особенности, соединением формулы где 1 и 2 - алкилы, содержащие 1-5 атомов углерода, а 3 является, как определено выше, полезным структурным элементом для синтеза соединений, которые известны как агенты против гиперхолестеролемии, обладающие ингибирующим действием на - редуктазу. В европейском патенте 0319847 описан процесс получения соединений формулы , исходя из-яблочной кислоты. Недостатком этого процесса является то, что он неприменим для производства в промышленных масштабах, а также имеет проблемы с очисткой, обусловленные некристаллической природой промежуточных соединений. В патенте США 5399722 описан процесс, начинающийся с коммерчески доступного этил-хлорацетоацетата или его бензилокси производного. К недостаткам этого процесса относится то,что в нем используется дорогостоящий катализатор рутений-, а желаемое соединение формулыполучают в шесть стадий. В патенте США 5481009 описан процесс, начинающийся с 4-фенил-3-бутеновой кислоты, проходя-щий примерно в 5 стадий. В этом процессе используются дорогостоящие материалы, такие как , -диметилгидроксиламин, и он включает опас где А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,4 есть О, ОН,или галоген, а а есть одинарная или двойная связь. Настоящее изобретение также относится к способу получения соединения формулы 17644 где А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,который включает а) взаимодействие соединения формулыс анионом третичного бутилацетата для получения соединения формулы , в которойесть тетрагидропиранил, трет-бутилдиметилсилил или тритил и 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил Соединение формулыдалее преобразуют в соединение формулы , где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил, А есть незамещенный или замещенный арил или гетероарил и Х есть галоген б) восстановление соединения фомулыс чтобы получить соединение формулы , гдететрагидропиранил, трет-бутилдиметилсилил тритил и 3 есть алкил, содержащий от 1 до 8 мов углерода, арил или аралкил Соединение формулыдалее преобразуют в соединение формулы , где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,А есть незамещенный или замещенный арил или гетероарил в) защиту соединения формулыс помощью АВ(ОН)2, чтобы получить соединение формулы ,где А есть незамещенный или замещенный арил или гетероарил,есть тетрагидропиранил, трет-бутилдиметилсилил или тритил и 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил и г) снятие защиты соединения формулыпутем использования мягкого кислотного катализатора,чтобы получить соединение формулы . Указанное соединение АВ(ОН)2 есть бороновая кислота. Соединение формулыокисляют до соединения формулы , где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил и А есть незамещенный или замещенный арил или гетероарил,используя пиридинийхлорхромат или Соединение формулы а и, в особенности, формулыиспользуют в синтезе аторвастатина, церивастатина, питавастатина, флувастатина или розувастатина. Соединение формулыслужит в качестве полезного промежуточного соединения для синтеза важных субстратов, используемых для синтеза статинов. Соединение формулыможет быть преобразовано в легко удаляемую группу путем обработки толуолсульфонилхлоридом, метансульфонилхлоридом, а образующееся промежуточное соединение может быть замещено цианидом для получения соединений формулы . Соединение формулыможет быть превращено в соединение формулыпутем реакции с водным раствором НВ или путем реакции с трифенилфосфином и СВ 4, которое затем превращают в соединение формулы . Путем использования стандартной процедуры соединение формулыможет быть окислено для получения соединения формулы . Настоящее изобретение относится к оптически активным производным дигидроксигексаноата формулы а, которые являются полезными промежуточными соединениями для синтеза ингибиторов фермента -СоА, таких как аторвастатин, церивастатин, розувастатин, питавастатин, флувастатин. Изобретение далее иллюстрируется примерами,его не ограничивающими. 3 17644 Пример 1. Синтез метил 4-трифенилметилокси 3-гидроксибутирата (формула ) К 25 г метил-3,4-дигидроксибутаноата добавляли до 250 мл(дихлорметил) и перемешивали до растворения, затем добавляли 19,8 г пиридина и охлаждали до 0 С. 41,4 г тритилхлорида растворяли в 50 мли добавляли при температуре 0-5 С в течение 15 минут. Раствору давали возможность нагреться до комнатной температуры и при этой температуре перемешивали в течение 17 часов. Добавляли воду и отделяли полученные слои. Слой,содержащий органические вещества, промывали раствором соли, высушивали и концентрировали. Из остатка путем добавления 25 мл циклогексана получали порошок, затем его очищали, что давало 15 г чистого продукта. ЯМР (СОС 3) 4,25 (, 1 Н), 3,6 (, 3), 3,15 (,2), 2,5 (, 2), 7,2-7,4 (, 15). Пример 2. Синтез трет-бутил-6-трифенилметилокси-5-гидрокси-3-оксогексаноата (формула ) К 125 мл(тетрагидрофуран) добавляли 24 г диизопропиламина и охлаждали до -15 С. При температуре от -15 до-5 С добавляли 168 мл 1,2(-бутиллитий) и перемешивали в течение 30 минут. 21,56 г трет-бутилацетата добавляли в 45 мл, предварительно охлажденного до -45 С, при этом температура поддерживалась в пределах от -45 до -25 С в течение 60 минут. Охлаждали реакционную смесь до -45 С и добавляли в течение 20 минут 30 г соединения примера 1 в , продолжая перемешивание при -25 С в течение 90 минут. Затем добавляли воду и слои разделялись. Водный слой экстрагировали с помощью(этилацетат), а объединенные органические слои промывали раствором соли, водой, высушивали и концентрировали, что давало целевое соединение, которое использовалось в таком виде на следующем этапе. Пример 3. Синтез трет-бутил-6-трифенилметилокси-3,5-дигидроксигексаноата (формула ) К неочищенному продукту примера 2 добавляли 150 млс последующим добавлением 15 мл МеОН (метанол) и охлаждали до -60 С. Добавляли в течение 20 минут 26 мл(метоксидиэтилборан), (50 раствор в ), в течение следующих 30 мин продолжали перемешивание. Реакционную смесь охлаждали до -80 С и порциями добавляли 5 г боргидрида натрия, после завершения добавления реакционную смесь перемешивали в течение 5 часов при -78 С. Для доведения рН до 7 добавляли уксусную кислоту, затем добавляли воду. Для получения целевого соединения образовавшийся водный слой экстрагировали с помощью , экстракты промывали солевым раствором, высушивали, концентрировали и использовали в таком виде на следующем этапе. Пример 4. Синтез трет-бутил-6-трифенилметилокси-3,5-фенилборонатогексаноата (формула ) Неочищенный продукт примера 3 растворяли в 100 мл толуола, добавляли 5,6 г фенилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и при пониженном 4 давлении удаляли толуол. Добавляли 30 мл метанола и отфильтровывали твердый осадок, в результате чего получали 10 г целевого продукта. Пример 5. Синтез трет-бутил-6-гидрокси-3,5(фенилборонато)гексаноата (формула П) К 5 г продукта примера 4 добавляли 20 мли охлаждали до 0 С. Добавляли 5 мл(трифторуксусная кислота) и перемешивали при 20 С в течение 6 часов. Отделяли воду и органический слой промывали бикарбонатом, солевым раствором, высушивали и концентрировали, что давало продукт,который затем очищали путем колоночной хроматографии. ЯМР (СВС 3) 7,7-7,8 (, 2), 7,4-7,5 (, 1),7,3-7,4 (, 2), 4,5 (, 1), 4,2 (, 1), 3,6 (, 1),3,5 (, 1), 2,55 (, 1), 2,45 (,1), 2,0 (, 1),1,7 (, 1) 1,5 (, 9). Пример 6. Синтез трет-бутил-6-циано-3,5(фенилборонато)гексаноата (формула ) 5 г продукта, полученного в примере 5, растворяли в дихлорметане (50 мл) и добавляли к нему пиридин (10 мл). Содержимое охлаждали до -10 С и по каплям добавляли к нему метансульфонилхлорид(1 экв). После 5-6 часов перемешивания при 0 С содержимое промывали бикарбонатом, водой и солевым раствором. Для получения производного Ометаносульфонила растворитель удаляли при пониженном давлении, и в таком виде он использовался на следующем этапе. К неочищенному метилсульфонилату, взятому в виде раствора в(диметилсульфоксид), (5 объемов), добавляли 1,5 эквивалента цианида калия. Содержимое выдерживали в рефлюкс-сосуде в течение 18-22 часов.удаляли при пониженном давлении, содержимое экстрагировали с помощью этилацетата, затем промывали бисульфитом, солевым раствором и при пониженном давлении удаляли растворитель для получения желаемого продукта. Пример 7. Синтез трет-бутил-6-оксо-3,5 фенилборонатогексаноата (формула ) 4,3 г диметилсульфоксида добавляли по капле к раствору 2,4 мл оксалилхлорида в 100 мл дихлорметана, находящегося при температуре -78 С. Смесь перемешивали при этой температуре в течение 15 минут и добавляли по каплям раствор в дихлорметане 5 г соединения, полученного в примере 5. После 15 минутного перемешивания добавляли 17 мл триэтиламина, и реакционную смесь оставляли нагреваться до комнатной температуры в течение 2 часов. Реакционную смесь концентрировали, остаток растворяли в воде и экстрагировали с использованием диэтилового эфира. Удаление растворителя давало целевое соединение. Пример 8. Синтез трет-бутил-6-трифенилметилокси-3,5-(1-нафтил)боронатогексаноата) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 7,1 г 1-нафтилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли 17644 толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 14 г целевого продукта. Пример 9. Синтез трет-бутил-6-трифенилметилокси-3,5-(2-метилфенил)боронатогексаноата(формула ) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 6,1 г 2 метилфенилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 12 г целевого продукта. Пример 10. Синтез трет-бутил-6-трифенилметилокси-3,5-(4-метоксифенил)боронатогексаноата(формула с) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 6,3 г 4 метоксифенилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 12 г целевого продукта. Пример 11. Синтез трет-бутил-6-трифенилметилокси-3,5-(8-хинолил)боронатогексаноата (формула) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 6,1 г 8 хинолилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 11 г целевого продукта. Пример 12. Синтез трет-бутил-6-трифенилметилокси-3,5-(3-нитрофенил)боронатогексаноата (формула ) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 6,1 г 3 нитрофенилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 10 г целевого продукта. Пример 13. Синтез трет-бутил-6-трифенилметилокси-3,5-(2,6-дифторфенил)боронатогексаноата(формула ) Неочищенный продукт примера 3 растворяли в 100 мл толуола и добавляли 6,3 г 2,6 дифторфенилбороновой кислоты. Воду удаляли путем азеотропной дистилляции в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры и удаляли толуол при пониженном давлении. Добавляли 30 мл метанола и отфильтровывали твердый осадок, что давало 12 г целевого продукта. 1 и 2 есть алкил, содержащий от 1 до 5 атомов углерода, 3 есть алкил, содержащий от 1 до 8 атомов углерода Формула 1 и 2 есть алкил, содержащий от 1 до 3 атомов углерода, или оба есть (2), гдеравно 4 или 5. 3 есть алкил, содержащий от 1 до 8 атомов углерода Анезамещенный или замещенный арил или гетероарил 3 алкил, содержащий от 1 до 8 атомов углерода,арил или аралкил 4 ОН,или Х и аодинарная связь 4 О и адвойная связь Анезамещенный или замещенный арил или гетероарил, 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил Формула тетрагидропиранил, трет-бутилдиметилсилил,тритил, 3 алкил, содержащий от 1 до 8 атомов углерода,арил или аралкил Формула тетрагидропиранил, трет-бутилдиметилсилил,тритил, 3 алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил Формула тетрагидропиранил, трет-бутилдиметилсилил,тритил, Анезамещенный или замещенный арил или гетероарил, 3 есть углеродный остаток, содержащий от 1 до 8 атомов, арил или аралкил Формула незамещенный или замещенный арил или гетероарил, 3 есть углеродный остаток, содержащий от 1 до 8 атомов, арил или аралкил Формула Анезамещенный или замещенный арил или гетероарил, 3 есть углеродный остаток, содержащий от 1 до 8 атомов, арил или аралкил Формула Анезамещенный или замещенный арил или гетероарил и 3 есть углеродный остаток, содержащий от 1 до 8 атомов, арил или аралкил, хгалоген Формула ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Сложные боронатные эфиры формулы а где А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил,4 есть О, ОН,или галоген и а есть одинарная или двойная связь. 2. Соединение по п. 1, где указанное соединение есть соединение формулы где А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил. 3. Способ получения соединения формулы где А есть незамещенный или замещенный арил или гетероарил,3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил, который включает а) взаимодействие соединения формулыс анионом третичного бутил-ацетата для получения соединения формулы , гдеесть тетрагидропиранил, трет-бутилдиметилсилил или тритил и 3 есть алкил, содержащий от 1 до 8 атомов углерода,арил или аралкил б) восстановление соединения формулыдля получения соединения формулы , гдеесть тетрагидропиранил, трет-бутилдиметилсилил или тритил и 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил и А есть незамещенный или замещенный арил или гетероарил, окислением соединения формулыс помощью придинийхлорхромата или /оксалилхлорида. 6. Способ синтеза соединения формулы в) защиту соединения формулысоединением АВ(ОН)2 для получения соединения формулы ,где А есть незамещенный или замещенный арил или гетероарил,есть тетрагидропиранил, третбутилдиметилсилил или тритил и 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил г) снятие защиты соединения формулыпутем использования мягкого кислотного катализатора,чтобы получить соединение формулы . 4. Способ по п. 3, где АВ(ОН)2 есть бороновая кислота. 5. Способ синтеза соединения формулы где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил, А есть незамещенный или замещенный арил или гетероарил, путем галогенирования соединения формулы . 7. Способ по п. 6, в котором соединение формулыпревращают в соединение формулыпутем взаимодействия соединения формулыс водным раствором НВ. 8. Способ по п. 6, в котором соединение формулыпревращают в соединение формулыпутем взаимодействия соединения формулыс трифенилфосфином и СВ 4. 9. Способ синтеза соединения формулы где 3 есть алкил, содержащий от 1 до 8 атомов углерода, арил или аралкил, А есть незамещенный или замещенный арил или гетероарил, путем взаимодействия соединения формулыс цианидом.
МПК / Метки
Метки: новые, боронатные, синтеза, варианты, сложные, эфиры, способ
Код ссылки
<a href="https://kz.patents.su/9-17644-novye-slozhnye-boronatnye-efiry-i-sposob-ih-sinteza-varianty.html" rel="bookmark" title="База патентов Казахстана">Новые сложные боронатные эфиры и способ их синтеза (варианты)</a>
Предыдущий патент: Способ получения порошка тантала
Следующий патент: Бетонная смесь для изготовления огнеупорных изделий
Случайный патент: Способ хирургического лечения варикозной болезни