Простой способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцита
Номер патента: 22834
Опубликовано: 16.08.2010
Авторы: ДЖАНГ, Джэ-Деог, ЧОЙ, Джеонг-Йонг, ЛИ, Юн-Янг, ЧАНГ, Чеонг-ХО, КО, Чанг-Квон, КИМ, Пьюнг-Мин
Формула / Реферат
Настоящее изобретение относится к терапевтическому способу трансплантации хрящей инъекционным способом.
Для устранения недостатков традиционных методов трансплантации хрящей, обеспечения возможности удобной трансплантации с использованием быстрого загустевания вводимого вещества, обеспечения полного присоединения трансплантируемых участков к смежным естественным хрящам, а также для лечение широкого диапазона хрящевых дефектов и сложных форм остеоартрита при упрощенной хирургической операции, предложен способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцита, включающей смешивание матриц, содержащих коллаген, гиалуроновую кислоту и фибрин, которые являются основными компонентами хряща животного происхождения, за счет использования шприца с перемешивающим наконечником, при этом результирующий раствор вводят непосредственно в область пораженного хряща.
Текст
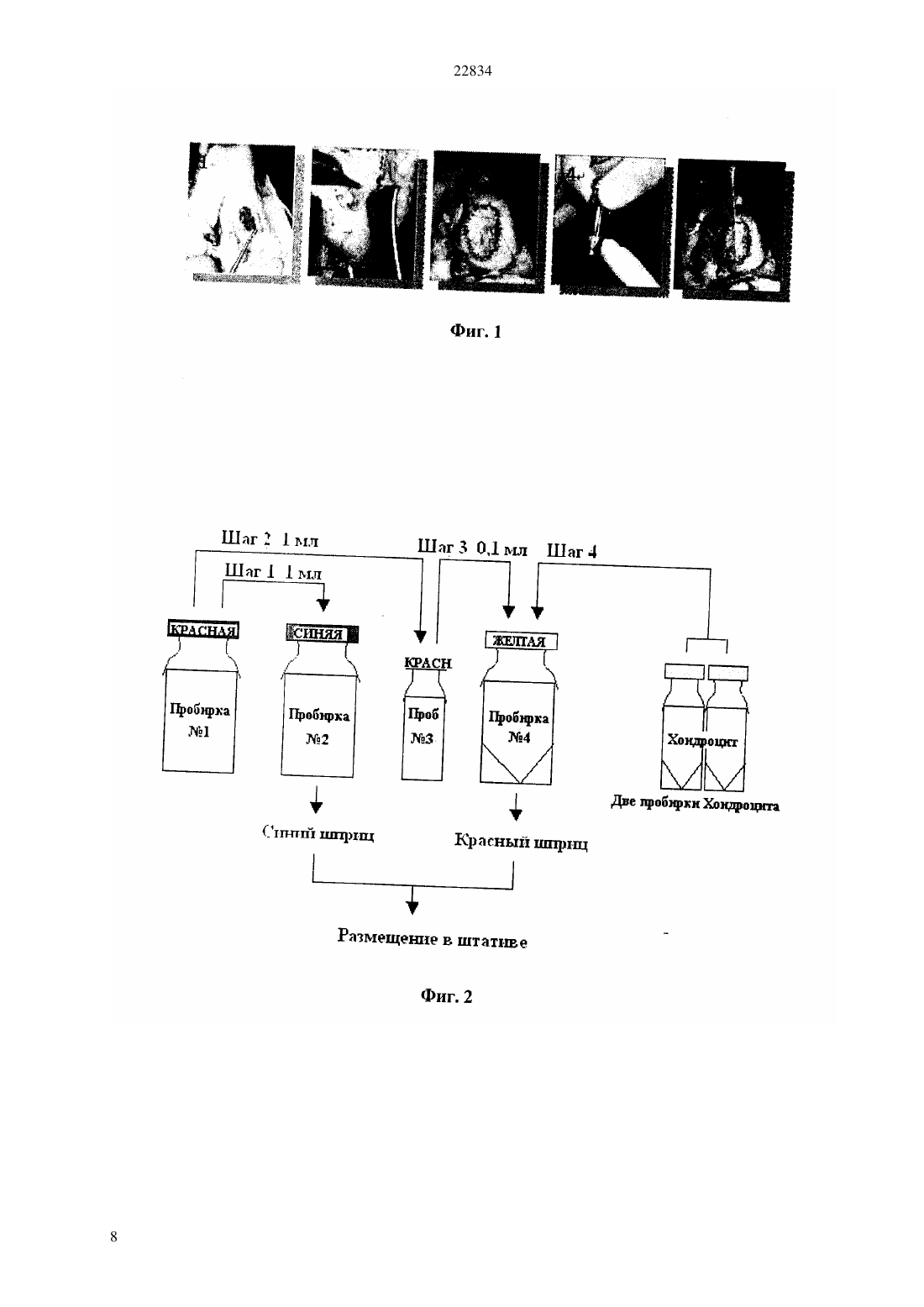
КОМИТЕТ ПО ПРАВАМ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ МИНИСТЕРСТВА ЮСТИЦИИ РЕСПУБЛИКИ КАЗАХСТАН ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУ ХОНДРОЦИТА ДЛЯ АВТОЛОГИЧЕСКОЙ ТРАНСПЛАНТАЦИИ ХОНДРОЦИТА(57) Настоящее изобретение относится к терапевтическому способу трансплантации хрящей инъекционным способом. Для устранения недостатков традиционных методов трансплантации хрящей, обеспечения возможности удобной трансплантации с использованием быстрого загустевания вводимого вещества, обеспечения полного присоединения трансплантируемых участков к смежным естественным хрящам, а также для лечение широкого диапазона хрящевых дефектов и сложных форм остеоартрита при упрощенной хирургической операции, предложен способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцита,включающей смешивание матриц, содержащих коллаген, гиалуроновую кислоту и фибрин, которые являются основными компонентами хряща животного происхождения, за счет использования шприца с перемешивающим наконечником, при этом результирующий раствор вводят непосредственно в область пораженного хряща.(74) Шабалина Галина Ивановна Шабалин Владимир Иванович(54) ПРОСТОЙ СПОСОБ ТРАНСПЛАНТАЦИИ ПРИГОДНОГО ДЛЯ ИНЪЕКЦИЙ 22834 Настоящее изобретение относится к терапевтическому способу трансплантации хрящей(хрящевые клетки) для автологической трансплантации) инъекционным способом. В частности, данное изобретение относится к терапевтическому способу трансплантации хрящей путем смешивания и трансплантации матриц,включающих фибрин, гиалуроновую кислоту и коллаген, являющихся основными компонентами хряща, при помощи которого устраняются недостатки традиционной пересадки костнонадкостничных тканей,появляется возможность лечения широкого перечня заболеваний, в том числе запущенного остеоартрита,облегчается лечение пациентов за счет применения усовершенствованного хирургического способа, что тем самым приводит к более быстрому и эффективному образованию хрящей и способствует удовлетворению запросов пациентов. В недавнем прошлом молекулярная биология,клеточная биология, эволюционная биология и технология культивирования тканей внесли свой вклад в улучшение здоровья и повышение качества жизни за счет разработки способов совершенствования, поддержания и восстановления функций поврежденных тканей и органов. Технология культивирования тканей производит тканевые вещества за счет управления неспецифической адгезией клеток, ростом и дифференциацией, а также активностью цитокинов и коэффициентов роста за счет взаимодействия с клеточной матрицей, используемой в качестве заменителя ткани,тем самым,выделяя внутриклеточные сигнальные вещества. Ранние работы в области технологии культивирования тканей были, главным образом, сосредоточены на применении клеток или клеточной терапии,использующей комплексную матрицу, образуемую клетками, тем самым, в большой степени ограничивая их применение, приводя к крайней необходимости в разработке более совершенных тканевых веществ и, следовательно, это привело к разработке хрящевой терапии, использующей хондроциты и матричные смеси. Было продемонстрировано, что нестабильность соединений и частичное повреждение мениска ускоряет истирание и повреждение суставных поверхностей. Кроме того, если суставной хрящ будет хотя бы один раз поврежден, то его невозможно восстановить в прежней мере. Регулярная стимуляция, применяемая в отношении поврежденного суставного хряща, вызывает боли в суставах и прогрессирующее ограничение подвижности сустава, приводя к неизбежному дегенеративному артриту. Хондроциты, которые не способны к пролиферации в естественных условиях,могут эффективно использоваться для восстановления суставов путем стимулирования дифференциации и пролиферации хрондоцитов за счет корректирования условий получения лабораторной культуры. В результате этого трансплантированные хондроциты приобретают 2 гистологические и механические свойства аналогичные тем, которые имеют хрящи нормальных суставов и, тем самым, отторжение трансплантации или разрушение ткани не наблюдается при положительных результатах у более чем 90 пациентов. Автологическая трансплантация хондроцитов(АТХ) является эффективной терапией для лечения поврежденного суставного хряща. Другие виды терапии, такие как абразивная артропластика,сверление и микроперелом,автологическая трансплантация надкостницы и надхрящницы предусматривают замену поврежденного хрящевого сустава на волокнистый хрящ или ткани, состоящие из волокнистого хряща без существенного образования гиалинового хряща. При этом по сравнению с другими, традиционными технологиями,самым важным преимуществом способа АТХ является производство гиалинового хряща. Несмотря на такое превосходное преимущество,автологическая трансплантация хондроцитов (АТХ) испытывает технические и теоретические трудности,как это показано на фиг. 1. Прежде всего, для технологии автологической трансплантации хондроцитов требуется осуществление большого хирургического надреза для сбора надкостницы. Такой большой надрез приводит к сильным болям, возникающим в результате хирургического вмешательства и снижению подвижности колена. Во-вторых, наложение швов на надкостничную заплату на границе дефектной области хряща требует очень сложного хирургического оперирования,которое, как было отмечено, иногда сопровождается надкостничной гипертрофией и внутрисуставной адгезией. Наложение швов на надкостницу является самым продолжительным процессом среди всех других хирургических операций для проведения автологической трансплантации хондроцитов. Кроме того, автологическая трансплантация хондроцитов является неблагоприятной при утечке хондроцитов из трансплантированных участков,которая иногда происходит во время реабилитационного процесса,такого как терапевтические физические упражнения для разработки колена после хирургической операции, а трансплантированные хондроциты, находящиеся в жидком состоянии в трансплантированных участках,локализуются с одной стороны за счет силы тяжести,тем самым,приводя к неравномерному распределению и неоднородному росту хряща/ .. . .,1996, 326, 270-283.,.. . ..,2003, , 37-47/. Для решения вышеперечисленных проблем,значительные исследования были сфокусированы на использовании рассасывающихся и биологически совместимых полимеров в качестве переносчиков или клеточного каркаса. Например, было выполнено большое количество исследований в области 22834 технологии культивирования тканей для образования хрящей в естественных и в лабораторных условиях с использованием естественных полимеров, таких как коллаген, гиалуроновая кислота и фибрин,выступающие в качестве биоматериалов, или с использованием синтетических полимеров, таких как полимолочная кислота или полигликолевая кислота. Одним из таких решений является способ,приведенный в( 2005/060987), в соответствии с которым а пораженное место вводят композицию, состоящую из смеси хондроцитов, тромбина на фибриногенной матрице. Клеточный каркас играет важную роль в поддержании пористой структуры, необходимой для роста и пролиферации клеток и фенотипов хондроцитов (хрящевых клеток). Фибрин и гиалуроновая кислота являются полимерами,удовлетворяющими требования по использованию клеточного каркаса, как это указано выше. Фибрин является естественным веществом и пригодным биологическим переносчиком при трансплантации хондроцитов. В дополнение к этому, уже отмечено,что фибрин имеет такие преимущества как биологическая совместимость, рассасываемость и способность присоединения к субхондральным костям (структурно приуроченные кости, т.е. расположены над или под хрящами). Кроме того,фибриновые структуры можно с легкостью изменить с образованием требуемых форм и использовать в виде инъекций. При этом гиалуроновая кислота представляет собой смазочное вещество,находящаяся в жидкости синовиального соединения,и регулирует содержание влаги в суставах. Тем не менее, все-таки остается одна проблема. Поскольку большинство клеточных каркасов для технологии культивирования тканей являются твердыми объектами, такими как заплатки, губчатые элементы и пластинки, то для хрящевой терапии сложно присоединить культивированные ткани к естественному хрящу. Этот факт представляет собой важный аспект в отношении того, что хрящевые средства, трансплантированные в поврежденные участки хрящей, не обеспечивают выздоровления граничных участков. Данное изобретение было создано для решения вышеуказанных проблем и представляет собой способ трансплантации хрящей путем инъекций. Следовательно,первой задачей данного изобретения является устранение недостатков традиционного наложения костно-надкостных лоскутов путем приготовления и трансплантации матриц, включающих коллаген, гиалуроновую кислоту и фибрин, которые являются основными компонентами хряща. Второй задачей данного изобретения является обеспечение возможности удобной трансплантации на месте с использованием быстрого загустевания,при котором вводимый хрящ превращается в желатиноподобную массу в течение короткого промежутка времени, т.е. примерно за 1-5 минут после трансплантации. Третей задачей данного изобретения является обеспечение полного присоединения трансплантируемых участков к смежным естественным хрящам, а также лечение широкого диапазона хрящевых дефектов и сложных форм остеоартрита. Четвертой задачей данного изобретения является предоставление пациентам облегчения за счет упрощенной хирургической операции. Пятой задачей данного изобретения является быстрое и эффективное образование хряща, тем самым удовлетворяя потребности пациентов за счет использования упрощенного способа хирургической операции. Согласно данному изобретению,вышеперечисленные и другие задачи могут быть выполнены способом трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцитов, включающим в себя смешивание матриц,включающих коллаген,гиалуроновую кислоту и фибрин, составляющих основные компоненты хряща животного происхождения, при использовании шприцов для введения полученного раствора в область пораженного хряща. Согласно другому аспекту настоящего изобретения, предлагается способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцитов,включающий в себя помещение 1 мл культуры хондроцита,содержащегося в пробирке 1 (красная) в стерильный шприц объемом 1 мл и ввод клеточной культуры в пробирку 2 (голубая), содержащую белый или светло-желтый лиофизированный порошок (фибриноген) посредством ввода шприца в пробирку 2 в вертикальном положении инъекция 1 мл клеточной культуры,содержащейся в пробирке 1 (красная) в пробирку 3 (красная, маленькая), содержащую белый лиофизированный порошок (тромбин) посредством ввода шприца в пробирку 3 в вертикальном положении, тем самым, медленно вводя красную жидкость отбор 0.1 см 3 из 1 мл, содержащегося в пробирке 3 (красная маленькая) с использованием шприца емкостью 1 мл с последующей инъекцией на дно пробирки 4 (желтая) добавление всего содержания двух пробирок,содержащих суспензию хондроцита в пробирку 4(желтая) с использованием стерильного шприца емкостью 1 мл с последующим перемешиванием содержимого (два или три раза) при помощи шприца отбор всего растворенного вещества шприцем емкостью 1 мл из пробирки 2 (голубая) после полного растворения ее содержимого отбор хорошо перемешенного клеточного терапевтического средства из пробирки 4 (желтая) в шприц емкостью 1 мл размещение двух шприцев емкостью 1 мл,заполненных веществами из пробирки 2 (голубая) и пробирки 4 (желтая), в фиксированный штатив с последующей установкой винтового наконечника на 3 22834 шприцы и перемешивание вещества шприцев с использованием их передних перемешивающих наконечников, с последующим вводом полученной смеси, подлежащей трансплантации, в поврежденные участки хряща животного. Вышеперечисленные и другие задачи, свойства и другие преимущества данного изобретения станут более понятными из нижеприведенного детального описания,подкрепленного соответствующими иллюстрациями, на которых Фиг. 1 представляет собой фотографию,отображающую традиционный способ трансплантации хрящевого вещества Фиг. 2 представляет собой фотографию,отображающую способ трансплантации пригодного для инъекций хрящевого вещества, который используется в настоящем изобретении Фиг. 3 представляет собой фотографию,отображающую способ трансплантации хрящевого вещества, который используется в настоящем изобретении Фиг. 4 представляет собой фотографию,отображающую способ трансплантации пригодного для инъекций хрящевого вещества, который используется в настоящем изобретении при помощи шприца Фиг. 5 представляет собой фотографию,отображающую физические свойства пригодного для инъекций хрящевого вещества по настоящему изобретению Фиг. 6 представляет собой фотографию, снятую через 3 месяца после регенерации хряща собаки согласно примеру по настоящему изобретению Фиг. 7 представляет собой электронную микрофотографию, выполненное через 8 недель после трансплантации хрящевого вещества по настоящему изобретению Фиг. 8 представляет собой электронную микрофотографию, выполненное через 12 недель после трансплантации хрящевого вещества по настоящему изобретению Фиг. 9 представляет собой фотографию, снятую через 12 недель после регенерации хрящевой ткани собаки согласно примеру по настоящему изобретению Фиг. 10 представляет собой фотографию,отражающую результаты гистологического обследования хрящевого вещества по настоящему изобретению и Фиг. 11 представляет собой фотографию,отражающую результаты иммуногистологического обследования хрящевого вещества по настоящему изобретению. Предпочтительный вариант осуществления настоящего изобретения будет более подробно описан со ссылкой на соответствующие фигуры чертежей. Способ трансплантации хрящевого вещества с помощью инъекций, используемый в настоящем изобретении, выполняется так, как это показано на фиг. 2-12. Что касается приведенного ниже описания настоящего изобретения, то если детальное описание 4 известных операций или устройств, используемых в настоящем изобретении, может привести к неправильному толкованию настоящего изобретения,то детальное описание опускается. Термины, содержащиеся в настоящем описании,предоставлены с учетом функций настоящего изобретения и могут быть изменены в зависимости от представлений заказчика или производителя. Следовательно, используемые термины, должны определяться с учетом содержания описания данного изобретения. Данное изобретение характеризуется смешиванием матриц, включающих коллаген,гиалуроновую кислоту и фибрин, являющихся основными компонентами хряща животного происхождения, путем использования шприцов с перемешивающим наконечником,при этом результирующий раствор вводится в область пораженного хряща. При этом настоящее изобретение обеспечивает следующее удобство трансплантации непосредственно на месте, связанное быстрым образованием желеобразной массы, при которых инъецируемое хрящевое терапевтическое средство превращается в желеобразную массу примерно в течении 1-5 минут после трансплантации полное присоединение краев трансплантируемого участка к смежному естественному хрящу возможность лечения широкого диапазона дефектов хрящей и сложных форм остеоартрита облегчение перенесения операции пациентами за счет упрощенного способа оперирования и, следовательно, стимулирование быстрой и более эффективной регенерации хрящей. Кроме того, данное изобретение относится к способу трансплантации хрящевого вещества путем инъекции в соответствии со следующим примером. Пример В данном примере были проведены эксперименты с использованием хондроцитов животного (собаки) в приведенной ниже последовательности, соответствующей фиг. 2. Оценка результатов была произведена через три месяца. 1. Границы дефектной области хряща были подрезаны и был измерен ее размер. После чего были выполнены следующие шаги. 2. Была удалена алюминиевая крышка пробирки 1 (красная), содержащейся в наборе, пробирки были промыты 70 раствором этанола. Пробирка(красная) содержит суспензию культивированных клеток красноватого цвета(культура хондроцитагиалуроновая кислотаапротинин и т.д.). 3. Удалена алюминиевая крышка пробирки 2(голубая), крышка и поверхность пробирки были промыты 70 раствором этанола. Пробирка 2(голубая) представляет собой бесцветную пробирку,содержащую белый или светло-желтый лиофизированный порошок (фибриноген). 4. Один миллилитр содержимого пробирки 1(красная) помещен в стерильный шприц емкостью 1 мл и игла шприца вставлена пробирку 2 22834 вводится на лиофилизат, а не вдоль внутренней стенки пробирки,при этом осторожно предотвращается контакт кончика иглы с лиофилизатом. После этого пробирка 2 (голубая) осторожно встряхивается руками до полного растворения лиофилизата, содержащегося в пробирке 2 (голубая). 5. Удалена алюминиевая крышка пробирки 3(красная, маленькая), крышка и поверхность пробирки были промыты 70 раствором этанола. Пробирка 3 (красная, маленькая) представляет собой бесцветную пробирку, содержащую белый лиофизированный порошок (тромбин). 6. Один миллилитр раствора, содержащегося в пробирке 1 (красная) помещен в шприц и игла шприца вставлена пробирку 3 (красная,маленькая),установленную в вертикальном положении, после чего постепенно вводится красная жидкость. 7. После удаления алюминиевой крышки пробирки 4 (желтая) и промывания крышки и поверхности пробирки 70 раствором этанола, 0.1 см 3 из 1 мл содержащегося в пробирке 3 (красная,маленькая) отбирается при помощи шприца емкостью 1 мл и вводится на дно пробирки 4(желтая). 8. Все содержимое двух пробирок, содержащих суспензию хондроцита, вводится в пробирку 4(желтая) при помощи стерильного шприца емкостью 1 мл с последующим перемешиванием (два или три раза) с использованием шприца. 9. После полного растворения содержимого пробирки 2 (голубая), весь объем растворенного вещества помещается в шприц емкостью 1 мл. 10. Хорошо перемешенный клеточный препарат из пробирки 4 (желтая) вводится шприц емкостью 1 мл. 11. Два шприца, заполненных веществами из пробирки 2 (голубая) и пробирки 4 (желтая) соответственно, устанавливаются на фиксированный штатив. 12. На шприцы устанавливается навинчивающийся кончик с последующей установкой винтового наконечника и опоры поршня. 13. После завершения сборки вводится трансплантат. Если возможно, то введение хрящевого вещества должно производиться за один раз без остановок. 14. Примерно через 5 минут после завершения трансплантации подрезают края трансплантируемого участка. Сравнение данного изобретения и традиционной автологической трансплантации хондроцитов (АТХ) показано в таблице 1 ниже. Таблица 1 Традиционная АТХ Жидкий препарат для инъекций АТХ по изобретению (инъецируемый хондрон) Препарат в виде геля (удобная трансплантация благодаря быстрому гелеобразованию в течение 1 - 5 минут после завершения трансплантации и возможность придания требуемых форм трансплантата). Хондроцитыбиологически совместимые материалы Нет необходимости в надкостнице (трансплантируется через небольшой разрез) Улучшенная возможность регенерации хряща Возможность выполнения хирургической операции через небольшой разрез (5 см). Возможность выполнения хирургической операции с использованием артроскопа. Равномерное распределение хряща (равномерное распределение благодаря свойствам быстрого образования геля в течение 1-5 минут с момента трансплантации и,следовательно, возможность однородной регенерации хряща в данном состоянии) Нет необходимости наложения швов Хондроцитысреда культивирования Необходимость наличия костнонадкостничного лоскута Прекрасная способность регенерации хряща Необходимо производить разрез на колене(надрез величиной более 15 см необходимо зашивать после забора и трансплантации надкостницы) Неравномерное распределение хряща(возможность неравномерной и локализованной регенерации хряща за счет действия силы тяжести из-за взвешенного состояния клеток в жидкой фазе) Наложение швов (самый продолжительный и сложный процесс среди всех хирургических действия) Большая продолжительность операции Малое операционное время Образование волокнистого хряща за счет Контроль за кровотечением при помощи костного воска кровотечения(главным образом образуется гиалиновый хрящ) Дополнение процесса образования колонки (смотрите состав хрящевого лекарства и его использование) Трансплантируется независимо от формы дефектов Устранение потеков клетки в связи с неполным наложением швов Сокращение времени ограничений нагрузок благодаря отсутствию швов на надкостницы 16186 При этом среда для культивирования клеток,использованная в данном изобретении, может быть представлена(модифицированная по способу Дульбекко среда Игла), -12 по способу Хэма,/-12,(среда Дульбекко,модифицированная по способу Исков), среда 5 А по способу МакКоя,(минимальная эссенциальная среда), альфа-,1640, среда -15 по способу Лейбовитца и базальная среда Игла, которые традиционно используются в данной области. Желательно, чтобы концентрация используемого лиофизированного порошка(фибриногена) находилась в диапазоне от 10 мг/мл до 200 мг/мл. Если концентрация фибриногена меньше 10 мг/мл, то этого слишком мало для использования его свойств в качестве матрицы. И наоборот, если содержание фибриногена превышает 200 мг/мл, то имеет место сложность, связанная с его растворением и его становится сложно использовать в связи с повышенной вязкостью. Поэтому, желательно использовать фибриноген в диапазоне от 10 мг/мл до 200 мг/мл. В дополнение к этому, предпочтительно, чтобы концентрация используемого белого лиофизированного порошка (тромбина) была в пределах от 1 международной единицына мл до 200 МЕ/мл. Если концентрация тромбина меньше 1 МЕ/мл, то этого слишком мало для формирования фибрина, следовательно, невозможно обеспечить гелеобразование в течение нескольких минут. И наоборот, если концентрация тромбина превышает 200 МЕ/мл, то тромбин застывает незамедлительно после его перемешивания и, следовательно, он не пригоден для использования в инъецируемом препарате. Поэтому желательно, чтобы концентрация тромбина находилась в диапазоне от 1 МЕ/мл до 200 МЕ/мл. В дополнение к этому, предпочтительно, чтобы концентрация используемого апротинина колебалась от 100 КМЕ/мл до 20000 КМЕ/мл. Если концентрация апротинина меньше 100 КМЕ/мл, то от него мало пользы для предотвращения распада фибрина. И наоборот, если концентрация апротинина превышает 20000 КМЕ/мл,то может иметь место цитотоксичность. Поэтому желательно, чтобы концентрация апротинина находилась в диапазоне от 100 КМЕ/мл до 20000 КМЕ/мл. Далее, предпочтительно, чтобы количество используемой гиалуроновой кислоты находилось в пределах от 0,01 до 2 (массовых или объемных). Если количество гиалуроновой кислоты меньше 0,01, то очень сложно использовать его свойства в качестве матрицы. И наоборот, если количество гиалуроновой кислоты превышает 2, то может иметься отрицательное воздействие на способность присоединения фибрина, тем самым, влияя на прочность и твердость матрицы. Поэтому желательно, чтобы количество гиалуроновой кислоты находилось в диапазоне от 0,01 до 2 (массовых или объемных). Кроме того, предпочтительно, чтобы количество используемого коллагена типа 2 колебалась от 50/мл до 1 мг/мл. Если количество коллагена типа 2 меньше 50/мг, то его свойства слабо выражены. И наоборот, если количество коллагена типа 2 превышает 1 мг/мл, то это отрицательно влияет на способность присоединения фибрина, тем самым,воздействуя на прочность и твердость матрицы. Поэтому желательно, чтобы количество коллагена типа 2 колебалось в диапазоне от 50/мл до 1 мг/мл. Как видно из вышесказанного,данное изобретение обеспечивает следующие преимущества разрешение проблем, относящихся к традиционным способам пересадки костно-надкостничных трансплантатов за счет смешивания и трансплантации матриц, включающих фибрин,гиалуроновую кислоту и коллаген, которые являются основными составляющими хряща в частности,удобная трансплантация по месту благодаря быстрому образованию геля, при которой вводимое хрящевое вещество превращается в желатиноподобную массу в течение короткого промежутка времени, примерно через 1 - 5 минут после трансплантации полное соединение трансплантируемых участков со смежным естественным хрящом, а также возможность лечения широкого круга дефектов хрящей и сложных форм остеоартрита облегчение последующей реабилитации пациентов за счет применения упрощенного способа хирургического вмешательства и, следовательно, ускоренное и более эффективное образование хрящей, повышающее качество лечения пациентов. Хотя для иллюстрации данного изобретения были раскрыты предпочтительные варианты его осуществления, для специалистов, работающих в данной области, ясно, что возможные модификации,дополнения и изменения не меняют сущности изобретения, раскрытого в формуле изобретения. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцита, отличающийся тем,что он включает смешивание матриц, содержащих коллаген, гиалуроновую кислоту и фибрин, которые являются основными компонентами хряща животного происхождения, за счет использования шприца с перемешивающим наконечником, при этом результирующий раствор вводят в область пораженного хряща. 2. Способ по п.1, отличающийся тем, что он включает помещение 1 мл культуры хондроцита,содержащегося в пробирке 1 (красная), в стерильный шприц емкостью 1 мл и ввод клеточной культуры в пробирку 2 (голубая), содержащую белый или светло-желтый лиофизированный порошок (фибриноген) посредством помещения шприца в пробирку 2 в вертикальном положении таким образом, чтобы концентрация фибриногена находилась в пределах от 10 мг/мл до 200 мг/мл ввод 1 мл клеточной культуры, содержащейся в пробирке 1 (красная) в пробирку 3 (красная,маленькая), содержащую белый лиофизированный 22834 порошок (тромбин) посредством помещения шприца в пробирку 3 в вертикальном положении, при медленном вводе красной жидкости отбор 0.1 см 3 из 1 мл, содержащегося в пробирке 3 (красная маленькая) с использованием шприца емкостью 1 мл с последующим вводом на дно пробирки 4 (желтая) так, чтобы концентрация тромбина находилась в пределах от 1 МЕ/мл до 200 Е/мл перенос всего содержимого двух пробирок,содержащих суспензию хондроцита в пробирку 4(желтая) с использованием стерильного шприца емкостью 1 мл с последующим перемешиванием содержимого (два или три раза) при помощи шприца отбор всего растворенного вещества шприцем емкостью 1 мл из пробирки 2 (голубая) после полного растворения ее содержимого отбор хорошо перемешенного клеточного терапевтического средства из пробирки 4 (желтая) шприцом емкостью 1 мл и размещение двух шприцев емкостью 1 мл,заполненных веществами из пробирки 2 (голубая) и пробирки 4 (желтая), в фиксированном штативе с последующей установкой винтового наконечника на шприцы и перемешивание вещества шприцев с использованием их перемешивающих наконечников,с последующим вводом полученной смеси,подлежащей трансплантации, в поврежденные области хряща животного. 3. Способ по п.2, отличающийся тем, что ввод вещества путем введения иглы шприца осуществляют посредством введения вещества,содержащегося в шприце, непосредственно на лиофилизат, при этом предотвращая контакт кончика иглы с лиофилизатом. 4. Способ по п.2, отличающийся тем, что клеточная культура пробирки,1 (красная) содержит 0.01 - 2 гиалуроновой кислоты, 10020,000 КМЕ/мл апротинина, 50/мл - 1 мг/мл коллагена типа 2 или их смесь.
МПК / Метки
МПК: A61K 35/32, A61F 2/30, A61L 27/00
Метки: пригодного, хондроцита, способ, трансплантации, автологической, простой, инъекций
Код ссылки
<a href="https://kz.patents.su/12-22834-prostojj-sposob-transplantacii-prigodnogo-dlya-inekcijj-hondrocita-dlya-avtologicheskojj-transplantacii-hondrocita.html" rel="bookmark" title="База патентов Казахстана">Простой способ трансплантации пригодного для инъекций хондроцита для автологической трансплантации хондроцита</a>